Clear Sky Science · ru
Молочная кислота стимулирует активацию инфламмасомы NLRP3 и расщепление цитокинов, похожих на каспазу‑1, через внутриклеточное закисление
Когда молекула, знакомая по тренировкам, оборачивается против нас
Молочная кислота известна по «жжению» в мышцах после интенсивного забега, но она также накапливается при тяжелых инфекциях, таких как сепсис. Это исследование показывает, что молочная кислота — не просто продукт отходов: внутри иммунных клеток она способствует включению мощного воспалительного механизма и даже может самостоятельно химически расщеплять ключевые иммунные сигналы. Понимание этой двойной роли молочной кислоты может изменить наше представление о воспалении при сепсисе, раке и других серьезных заболеваниях. 
Как иммунные клетки чувствуют опасность
Наша первая линия защиты от инфекции опирается на врожденные иммунные клетки, такие как макрофаги, которые быстро улавливают угрозу и выпускают сигналы тревоги. Центральный узел управления в этих клетках, называемый инфламмасомой NLRP3, реагирует на широкий спектр угроз и активирует фермент, который расщепляет неактивные предшественники цитокинов до их активных форм. Эти активные фрагменты, особенно IL‑1β и IL‑18, затем секретируются, чтобы мобилизовать другие иммунные клетки. Хотя такая реакция помогает устранять инфекции, при чрезмерной активации она способствует жизнеугрожающим состояниям, таким как септический шок.
Использование топлива, кислотность клетки и иммунный переключатель
Чтобы запитать эту быструю систему тревоги, макрофаги смещают свой метаболизм в сторону гликолиза — быстрого способа разложения сахара, в ходе которого образуется молочная кислота. Исследователи показали, что при активации NLRP3 иммунные клетки быстро увеличивают производство молочной кислоты и удерживают её внутри. Это накопление закисляет внутреннюю среду клетки и, в свою очередь, сильно усиливает сборку инфламмасомы, активацию фермента и выброс IL‑1β. Кислая внешняя среда мешает выходу молочной кислоты, ещё глубже сдвигая внутреннюю кислотность и усиливая реакцию. Повышение pH окружающей жидкости до слегка Щелочного предотвращало это закисление и почти полностью отключало активность инфламмасомы, не останавливая при этом само производство молочной кислоты.
Внутри клетки: цепная реакция к воспалению
При более детальном рассмотрении команда обнаружила, что закисление, вызванное молочной кислотой, нарушает работу митохондрий — энергетических станций клетки, — и увеличивает образование реактивных видов кислорода, типа химического стресс‑сигнала. Одновременно активируется чувствительный к стрессу фермент PKR и усиливается его физическое взаимодействие с механизмом NLRP3. И митохондриальный стресс, и активация PKR оказались необходимыми для полной функции инфламмасомы. Блокирование синтеза молочной кислоты или повышение щёлочности окружения снижало эти стресс‑сигналы, ослабляло партнёрство PKR–NLRP3 и тормозило формирование комплекса инфламмасомы. 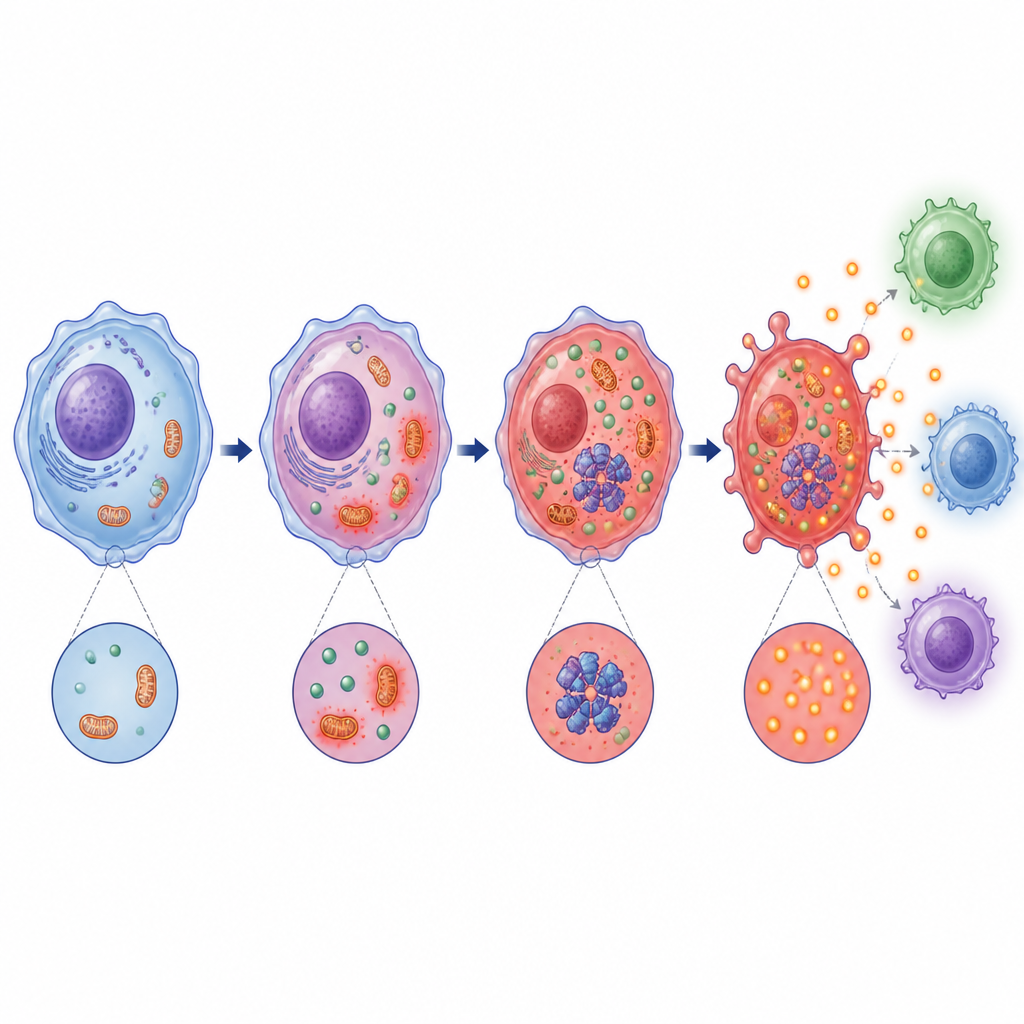
Молочная кислота как химический «скальпель»
Удивительно, но молочная кислота имела и вторую, независимую роль. В клеточных экстрактах, лишённых целой инфламмасомы, простое добавление молочной кислоты было достаточным, чтобы расщепить предшественники IL‑1β и IL‑18 до зрелых фрагментов, совпадавших по размеру с продуктами обычного ферментного расщепления. Это химическое расщепление требовало кислой, недиссоциированной формы молочной кислоты и зависело от конкретного сайта в IL‑1β — того же, который обычно использует фермент. Другие органические кислоты с похожими химическими группами могли вызывать это в меньшей степени, тогда как сильная минеральная кислота была значительно менее эффективна, что указывает на то, что собственная структура молочной кислоты способствует точному расщеплению при выраженной кислотности.
Что это значит для сепсиса и других заболеваний
Чтобы проверить эти идеи в живой системе, исследователи использовали модель полимикробного сепсиса у мышей — тяжёлой системной инфекции. Повышение уровня лактата в крови септических мышей увеличивало содержание IL‑1β в крови и брюшной полости, привлекало больше нейтрофилов на место инфекции, снижало температуру тела и ухудшало выживаемость. Лечение животных препаратом, блокирующим NLRP3, во многом обращало эти вредные эффекты, подчёркивая, что всплеск молочной кислоты подпитывает воспаление в основном через этот путь. В сумме результаты указывают, что молочная кислота действует двояко: она перестраивает клеточный метаболизм в пользу активации инфламмасомы и при экстремальной кислотности напрямую обрабатывает ключевые цитокины.
Почему эти выводы важны
Для непрофессионала ключевое сообщение таково: молочная кислота — не просто безвредный побочный продукт упражнений или болезни. Внутри стрессированных иммунных клеток она превращается в сигнал «подожги огонь», усиливая воспаление и делая его труднее контролируемым. При состояниях вроде сепсиса, когда повышаются и лактат, и кислотность, это может переломить баланс от полезной защиты к опасному системному повреждению. Раскрывая, как молочная кислота втягивает иммунные клетки в это сверхактивное состояние и как она может напрямую формировать воспалительные медиаторы, работа указывает на новые стратегии охлаждения вредного воспаления через модуляцию внутриклеточной кислотности и систему NLRP3.
Цитирование: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
Ключевые слова: молочная кислота, инфламмасома, IL-1β, сепсис, иммунный метаболизм