Clear Sky Science · fr
Lactate entraîne l’activation de l’inflammasome NLRP3 et la clivage de cytokines de type caspase‑1 via l’acidification intracellulaire
Quand une molécule de l’effort se retourne contre nous
L’acide lactique est célèbre pour la sensation de brûlure dans les muscles après un effort intense, mais il s’accumule aussi lors d’infections sévères comme la septicémie. Cette étude révèle que l’acide lactique n’est pas seulement un simple déchet : à l’intérieur des cellules immunitaires, il contribue à activer une machinerie inflammatoire puissante et peut même cliver chimiquement des messagers immunitaires clés par lui‑même. Comprendre cette double facette de l’acide lactique pourrait changer notre perception de l’inflammation dans la septicémie, le cancer et d’autres maladies graves. 
Comment les cellules immunitaires détectent le danger
Notre première ligne de défense contre l’infection repose sur des cellules immunitaires innées, comme les macrophages, qui détectent rapidement le danger et libèrent des signaux d’alerte. Un centre de contrôle dans ces cellules, appelé inflammasome NLRP3, répond à une grande variété de menaces et active une enzyme qui coupe les précurseurs inactifs des cytokines pour les transformer en formes actives. Ces fragments actifs, en particulier l’IL‑1β et l’IL‑18, sont ensuite sécrétés pour mobiliser d’autres cellules immunitaires. Si cette réponse aide à éliminer les infections, lorsqu’elle est excessive elle contribue à des états menaçant le pronostic vital, comme le choc septique.
Utilisation du carburant, acidité cellulaire et un basculement immunitaire
Pour alimenter ce système d’alarme rapide, les macrophages réorientent leur métabolisme vers la glycolyse, une voie rapide de dégradation du glucose qui produit de l’acide lactique. Les chercheurs montrent que lorsque NLRP3 est activé, les cellules immunitaires augmentent rapidement la production d’acide lactique et en retiennent davantage à l’intérieur. Cette accumulation acidifie l’intérieur cellulaire et, à son tour, renforce nettement l’assemblage de l’inflammasome, l’activation de l’enzyme et la libération d’IL‑1β. Des conditions externes acides empêchent la sortie de l’acide lactique, approfondissant encore ce décalage interne et amplifiant la réponse. Élever légèrement le pH du milieu environnant a empêché cette acidification et a presque totalement éteint l’activité de l’inflammasome sans interrompre la production d’acide lactique elle‑même.
À l’intérieur de la cellule : une réaction en chaîne vers l’inflammation
En approfondissant le mécanisme, l’équipe a constaté que l’acidification induite par l’acide lactique perturbe les mitochondries, les centrales énergétiques de la cellule, et augmente les espèces réactives de l’oxygène, un type de signal de stress chimique. Parallèlement, elle active une enzyme détectrice de stress appelée PKR et favorise son interaction physique avec la machinerie NLRP3. Tant le stress mitochondrial que l’activation de PKR se sont révélés nécessaires au fonctionnement complet de l’inflammasome. Bloquer la production d’acide lactique ou rendre l’environnement plus alcalin a réduit ces signaux de stress, affaibli le partenariat PKR–NLRP3 et limité la formation du complexe inflammasome. 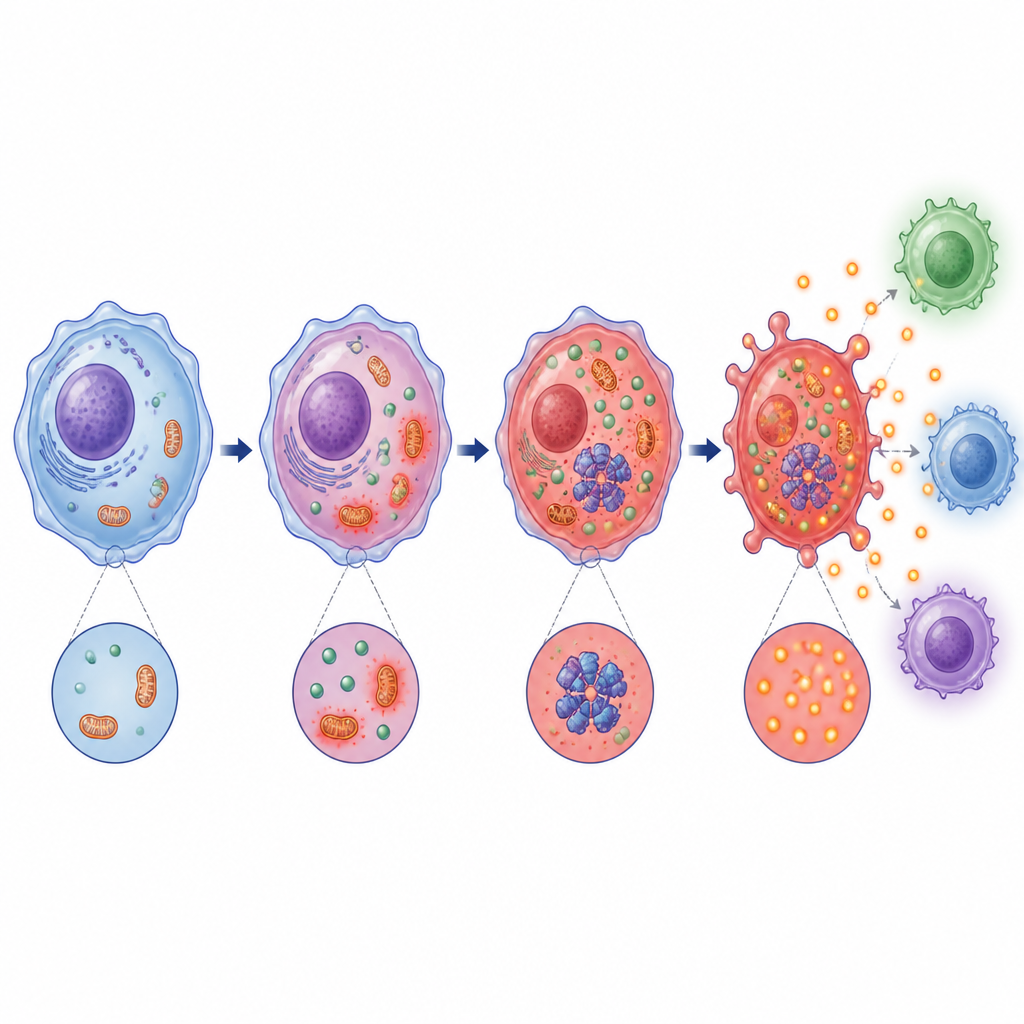
L’acide lactique comme « scalpel » chimique
De façon surprenante, l’acide lactique joue aussi un second rôle indépendant. Dans des extraits cellulaires dépourvus de l’inflammasome intact, l’ajout d’acide lactique suffisait à cliver les précurseurs de l’IL‑1β et de l’IL‑18 en fragments de taille mature identiques à ceux produits par l’enzyme habituelle. Ce clivage chimique nécessitait la forme acide non dissociée de l’acide lactique et dépendait d’un site spécifique dans l’IL‑1β, le même site utilisé normalement par l’enzyme. D’autres acides organiques présentant des groupes chimiques similaires pouvaient provoquer ce phénomène dans une moindre mesure, tandis qu’un acide minéral fort était beaucoup moins efficace, ce qui suggère que la structure même de l’acide lactique favorise cette découpe précise sous des conditions très acides.
Ce que cela implique pour la septicémie et d’autres maladies
Pour tester ces idées in vivo, les chercheurs ont utilisé un modèle murin de septicémie polymicrobienne, une infection sévère et généralisée. Augmenter le taux de lactate sanguin chez les souris septiques a élevé l’IL‑1β dans le sang et la cavité abdominale, attiré davantage de neutrophiles sur le site d’infection, abaissé la température corporelle et réduit la survie. Traiter les souris avec un médicament bloquant NLRP3 a en grande partie inversé ces effets délétères, soulignant que la flambée de l’acide lactique alimente l’inflammation principalement par cette voie. Globalement, ces résultats suggèrent que l’acide lactique est un moteur d’inflammation à double effet : en remodelant le métabolisme cellulaire pour favoriser l’activation de l’inflammasome et en traitant directement les cytokines clés lorsque l’acidité est extrême.
Pourquoi ces découvertes sont importantes
Pour un lecteur non spécialiste, le message essentiel est que l’acide lactique n’est pas simplement un produit inoffensif de l’exercice ou de la maladie. Dans les cellules immunitaires stressées, il devient un signal qui dit « montez le feu », renforçant et rendant plus difficilement contrôlable l’inflammation. Dans des états comme la septicémie, où l’acide lactique et l’acidité augmentent simultanément, cela peut faire basculer la réponse d’une défense utile vers un dommage systémique dangereux. En révélant comment l’acide lactique pousse les cellules immunitaires vers cet état hyperactif, et comment il peut directement façonner les messagers inflammatoires, ce travail ouvre la voie à de nouvelles stratégies pour freiner l’inflammation nocive en ciblant la gestion de l’acidité cellulaire et le système NLRP3.
Citation: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
Mots-clés: acide lactique, inflammasome, IL-1β, septicémie, métabolisme immunitaire