Clear Sky Science · es
El ácido láctico impulsa la activación del inflamasoma NLRP3 y el corte tipo caspasa-1 de citocinas mediante acidificación intracelular
Cuando una molécula del ejercicio se vuelve contra nosotros
El ácido láctico es conocido por la quemadura que sientes en los músculos tras una carrera intensa, pero también se acumula durante infecciones graves como la sepsis. Este estudio revela que el ácido láctico puede funcionar como algo más que un simple residuo: dentro de las células inmunitarias ayuda a activar poderosas maquinarias inflamatorias e incluso puede cortar químicamente mensajeros inmune clave por sí solo. Comprender esta doble vida del ácido láctico podría cambiar nuestra visión de la inflamación en la sepsis, el cáncer y otras enfermedades graves. 
Cómo las células inmunitarias detectan peligro
Nuestra primera línea de defensa frente a la infección depende de células inmunitarias innatas, como los macrófagos, que detectan rápidamente el peligro y liberan señales de alarma. Un centro de control dentro de estas células, llamado inflamasoma NLRP3, responde a una amplia gama de amenazas y activa una enzima que corta precursores inactivos de citocinas en sus formas activas. Estos fragmentos activos, especialmente IL-1β e IL-18, se secretan para movilizar otras células inmunitarias. Aunque esta respuesta puede ayudar a eliminar infecciones, cuando se desboca contribuye a condiciones potencialmente mortales como el shock séptico.
Uso de combustible, acidez celular y un interruptor inmunitario
Para alimentar este sistema de alarma rápido, los macrófagos desplazan su metabolismo hacia la glucólisis, una vía veloz de descomposición del azúcar que produce ácido láctico. Los investigadores demostraron que cuando se activa NLRP3, las células inmunitarias aumentan rápidamente la producción de ácido láctico y retienen más de éste en su interior. Esta acumulación acidifica el interior celular y, a su vez, potencia fuertemente el ensamblaje del inflamasoma, la activación enzimática y la liberación de IL-1β. Condiciones ácidas fuera de la célula impiden la salida del ácido láctico, profundizando aún más el cambio ácido interno y amplificando la respuesta. Elevar ligeramente el pH del líquido circundante impidió esta acidificación y casi desactivó por completo la actividad del inflamasoma sin detener la propia producción de ácido láctico.
Dentro de la célula: una reacción en cadena hacia la inflamación
Al profundizar, el equipo halló que la acidificación inducida por ácido láctico altera las mitocondrias, las centrales energéticas de la célula, y aumenta las especies reactivas de oxígeno, un tipo de señal química de estrés. Al mismo tiempo, activa una enzima sensora de estrés llamada PKR y favorece su interacción física con la maquinaria NLRP3. Tanto el estrés mitocondrial como la activación de PKR resultaron necesarios para la función completa del inflamasoma. Bloquear la producción de ácido láctico o alcalinizar el entorno redujo estas señales de estrés, debilitó la asociación PKR–NLRP3 y frenó la formación del complejo del inflamasoma. 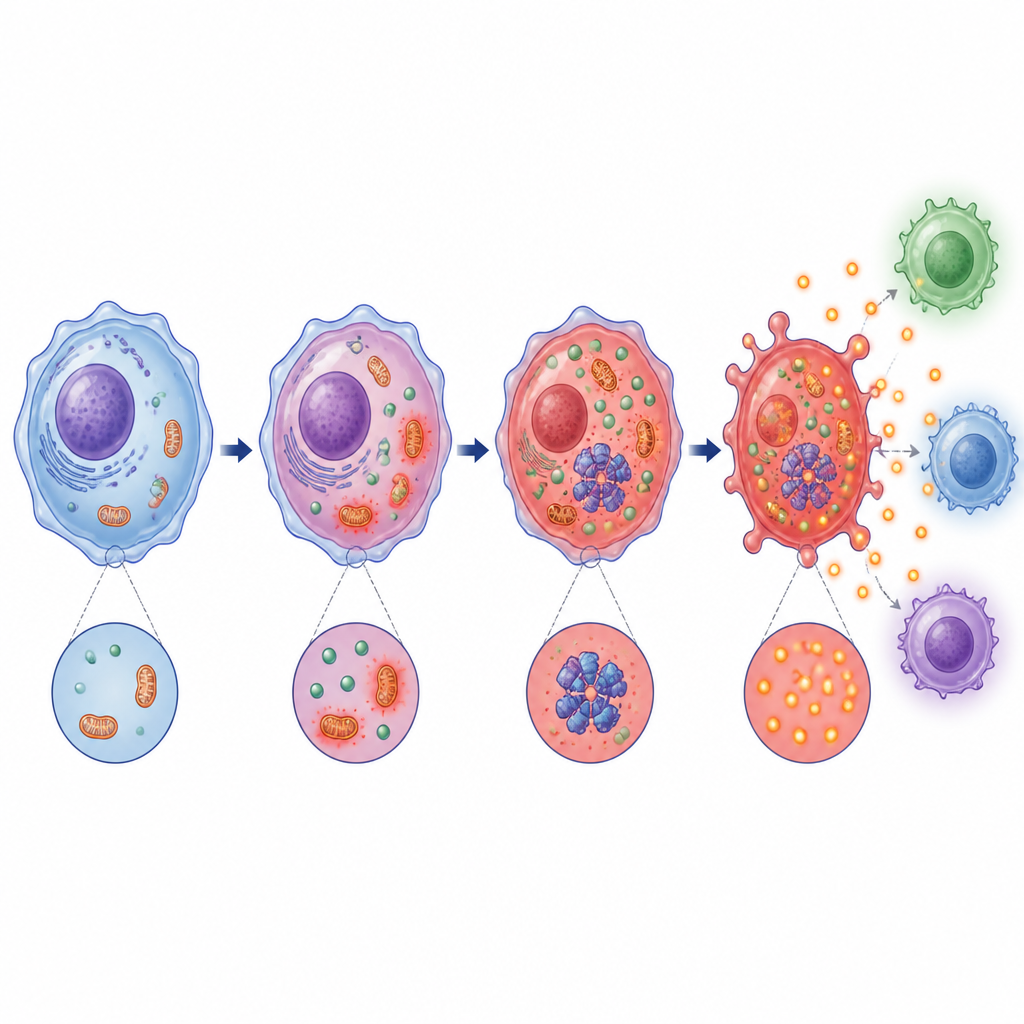
El ácido láctico como “bisturí” químico
Sorprendentemente, el ácido láctico también desempeñó un segundo papel, independiente. En extractos celulares carentes de la maquinaria intacta del inflamasoma, la simple adición de ácido láctico fue suficiente para cortar los precursores de IL-1β e IL-18 en fragmentos de tamaño maduro que coincidían con los producidos por la enzima habitual. Este corte químico requirió la forma ácida, no disociada, del ácido láctico y dependió de un sitio específico dentro de IL-1β, el mismo sitio usado normalmente por la enzima. Otros ácidos orgánicos con grupos químicos similares pudieron hacerlo en menor medida, mientras que el ácido mineral fuerte por sí solo fue mucho menos eficaz, lo que sugiere que la propia estructura del ácido láctico contribuye a impulsar esta reacción de escisión precisa en condiciones muy ácidas.
Qué significa esto para la sepsis y otras enfermedades
Para probar estas ideas en un sistema vivo, los investigadores utilizaron un modelo murino de sepsis polimicrobiana, una infección grave y de todo el cuerpo. Elevar los niveles de lactato en sangre de los ratones sépticos aumentó IL-1β en la sangre y en la cavidad abdominal, atrajo más neutrófilos al foco de infección, bajó la temperatura corporal y empeoró la supervivencia. Tratar a los ratones con un fármaco que bloquea NLRP3 revirtió en gran medida estos efectos nocivos, lo que destaca que el aumento de ácido láctico alimenta la inflamación principalmente a través de esta vía. En conjunto, los hallazgos sugieren que el ácido láctico es un impulsor de la inflamación con dos frentes: remodela el metabolismo celular para favorecer la activación del inflamasoma y procesa directamente citocinas clave cuando la acidez es extrema.
Por qué importan estos hallazgos
Para un lector no especializado, el mensaje clave es que el ácido láctico no es solo un subproducto inocuo del ejercicio o la enfermedad. Dentro de las células inmunitarias estresadas, se convierte en una señal que dice “sube el fuego”, haciendo la inflamación más intensa y difícil de controlar. En condiciones como la sepsis, donde aumentan tanto el ácido láctico como la acidez, esto puede inclinar la balanza desde una defensa útil hacia un daño sistémico peligroso. Al revelar cómo el ácido láctico empuja a las células inmunitarias hacia este estado sobreactivado y cómo puede moldear directamente los mensajeros inflamatorios, este trabajo apunta a nuevas estrategias para enfriar la inflamación perjudicial atacando el manejo de la acidez celular y el sistema NLRP3.
Cita: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
Palabras clave: ácido láctico, inflamasoma, IL-1β, sepsis, metabolismo inmune