Clear Sky Science · ar
الحمض اللاكتيكي يحفّز تنشيط إنفلَمازوم NLRP3 وقطع السيتوكينات المشابهة للكاسبيز-1 عبر تحمض داخل الخلايا
عندما يتحول جزيء التمرين ضدنا
يشتهر الحمض اللاكتيكي بالاحتراق الذي تشعر به في عضلاتك بعد جري شاق، لكنه يتراكم أيضاً أثناء العدوى الشديدة مثل الإنتان. تكشف هذه الدراسة أن الحمض اللاكتيكي يمكن أن يكون أكثر من نفاية بسيطة: داخل الخلايا المناعية يساعد في تشغيل آلية التهابية قوية ويمكنه حتى قطع رسائل مناعية رئيسية كيميائياً بمفرده. قد يعيد فهم هذا الازدواج في دور الحمض اللاكتيكي تشكيل نظرتنا للالتهاب في الإنتان والسرطان وأمراض خطيرة أخرى. 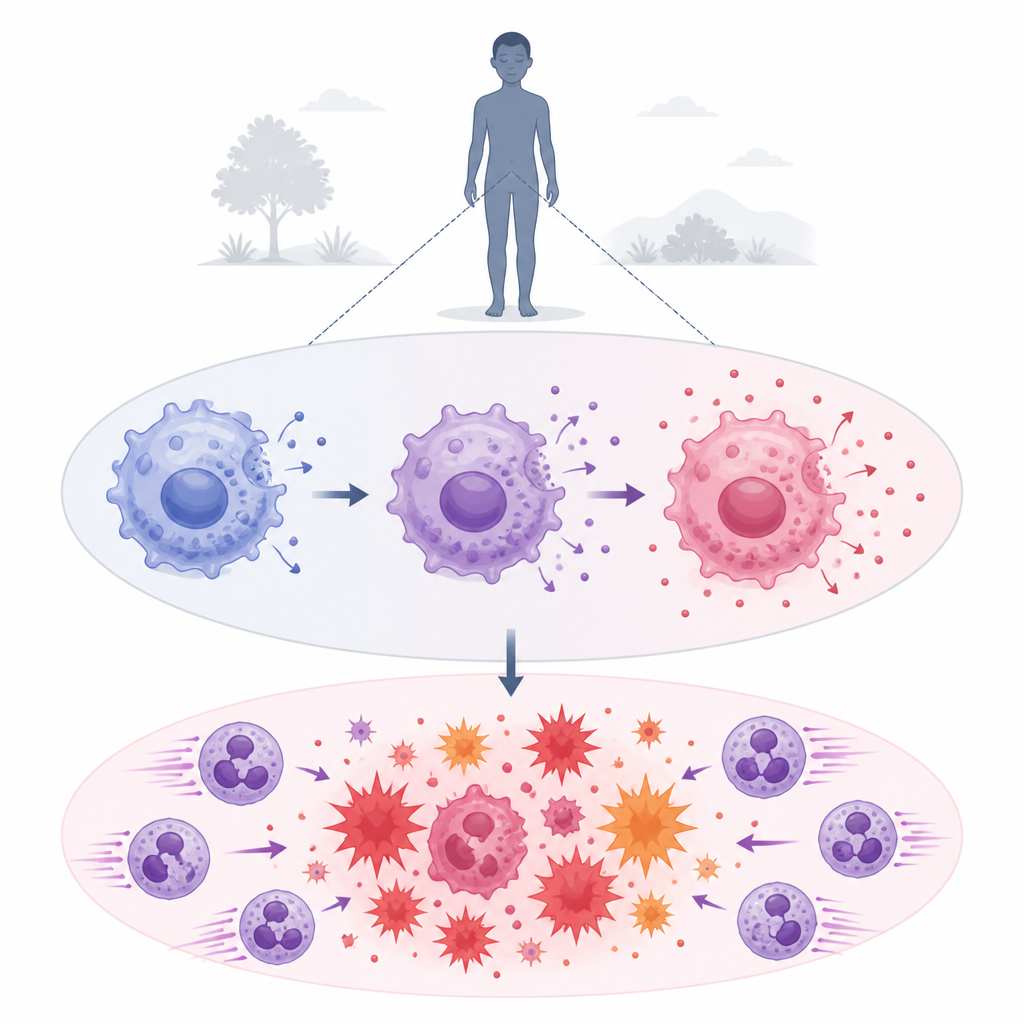
كيف تكتشف الخلايا المناعية الخطر
يعتمد خط دفاعنا الأول ضد العدوى على خلايا المناعة الفطرية، مثل البلعمات، التي تكتشف الخطر بسرعة وتطلق إشارات إنذار. يوجد محور تحكم مركزي داخل هذه الخلايا يُسمى إنفلَمازوم NLRP3، يستجيب لمجموعة واسعة من التهديدات ويُفعّل إنزيمًا يقطع مقدّمات السيتوكينات غير النشطة إلى أشكالها النشطة. تُفرَز هذه القطع النشطة، لا سيما IL-1β وIL-18، بعد ذلك لتجنيد خلايا مناعية أخرى. ورغم أن هذا الاستجابة قد تساعد في إزالة العدوى، فإن فرط نشاطها يساهم في حالات تهدد الحياة مثل الصدمة الإنتانية.
استخدام الوقود، حمضية الخلايا، ومفتاح مناعي
لتشغيل نظام الإنذار السريع هذا، تحول البلعمات استقلابها نحو التحلل السكري، وهو طريق سريع لتفكيك السكر ينتج الحمض اللاكتيكي. أظهر الباحثون أنه عند تحفيز NLRP3، تزيد الخلايا المناعية بسرعة من إنتاج الحمض اللاكتيكي وتحبس كميات أكبر منه داخلها. يؤدي هذا التراكم إلى تحمض داخل الخلية ويعزز بدوره بقوة تجميع الإنفلَمازوم، وتنشيط الإنزيم، وإطلاق IL-1β. الظروف الحمضية خارج الخلية تمنع خروج الحمض اللاكتيكي، مما يعمق التحول الداخلي في الحموضة ويضخم الاستجابة. رفع قلوية السائل المحيط قليلاً حال دون هذا التحمض وأوقف تقريباً نشاط الإنفلَمازوم دون أن يوقف إنتاج الحمض اللاكتيكي نفسه.
داخل الخلية: تفاعل سلسلي يؤدي إلى الالتهاب
عند الغوص أعمق، وجد الفريق أن التحَمّض الناجم عن الحمض اللاكتيكي يُعطّل الميتوكوندريا، محطات طاقة الخلية، ويزيد من أنواع الأكسجين التفاعلية، وهي نوع من إشارات الضغوط الكيميائية. في الوقت نفسه، ينشط إنزيم استشعار الإجهاد المسمى PKR ويعزز تفاعله الفيزيائي مع آلية NLRP3. اتضح أن كلاً من إجهاد الميتوكوندريا وتنشيط PKR ضروريان لوظيفة الإنفلَمازوم الكاملة. قلّل حجب إنتاج الحمض اللاكتيكي أو جعل البيئة أكثر قلوية من هذه الإشارات الضاغطة، وضعف شراكة PKR–NLRP3، وكبح تشكيل مركب الإنفلَمازوم. 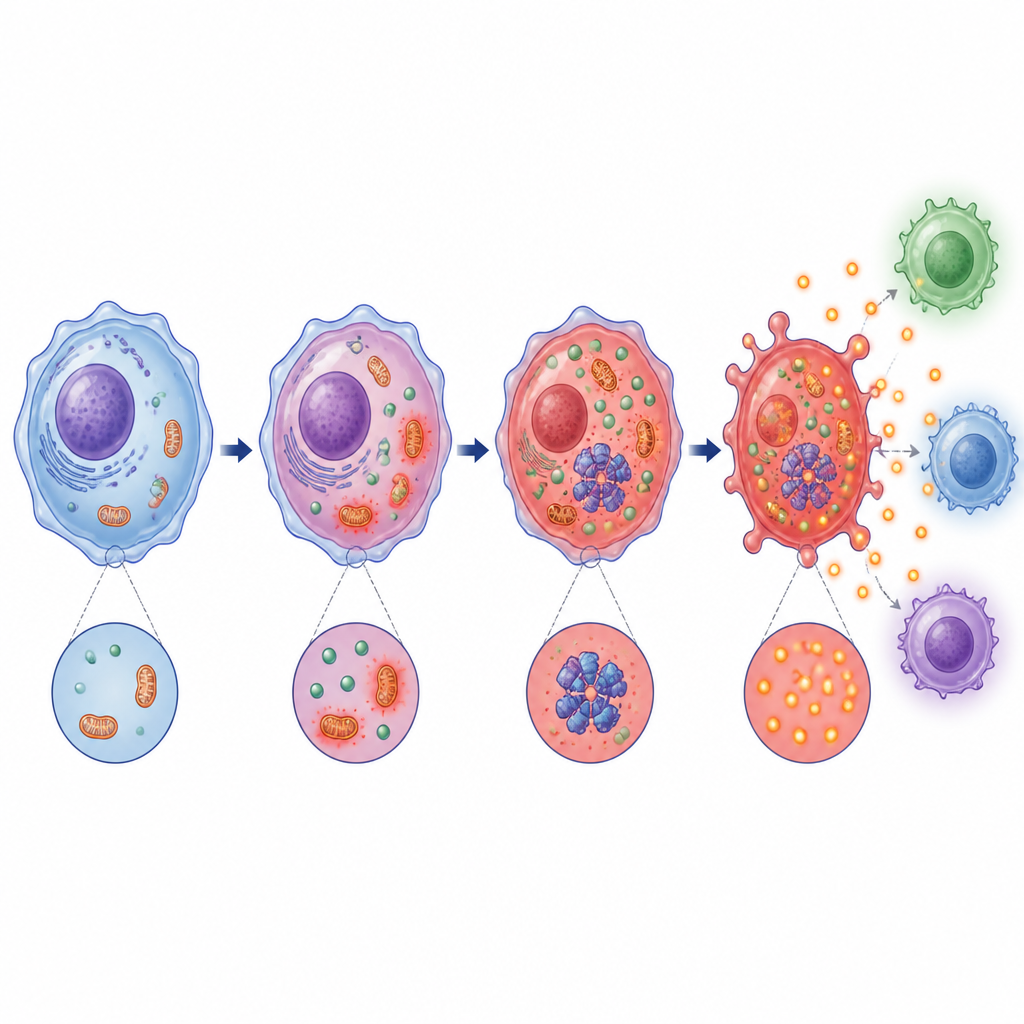
الحمض اللاكتيكي كـ "مشرط" كيميائي
على نحو مفاجئ، لعب الحمض اللاكتيكي دورًا ثانياً ومستقلاً. في مستخلصات خلوية تفتقر إلى آلية إنفلَمازوم سليمة، كان إضافة الحمض اللاكتيكي وحده كافياً لقطع مقدمات IL-1β وIL-18 إلى قطع بحجم ناضج تطابق تلك التي ينتجها الإنزيم المعتاد. تطلّب هذا القطع الكيميائي الشكل الحمضي غير المتأين للحمض اللاكتيكي واعتمد على موقع محدد داخل IL-1β، وهو نفس الموقع الذي يستخدمه الإنزيم عادة. يمكن لأحماض عضوية أخرى ذات مجموعات كيميائية مشابهة أن تفعل ذلك بدرجة أقل، بينما كان الحمض المعدني القوي وحده أقل فعالية بكثير، مما يوحي بأن بُنْية الحمض اللاكتيكي نفسها تساعد في دفع هذا التفاعل الدقيق للقطع تحت ظروف حمضية شديدة.
ماذا يعني ذلك للإنتان وأمراض أخرى
لاختبار هذه الأفكار في نظام حي، استخدم الباحثون نموذج فأر للإنتان المتعدد الميكروبات، وهو عدوى شديدة بالجسم كله. زيادة مستويات اللاكتات في الدم لدى الفئران المصابة بالإنتان رفعت مستويات IL-1β في الدم وتجويف البطن، وجذبت المزيد من العدلات إلى موقع العدوى، وخفضت درجة حرارة الجسم، وساءت النجاة. عالجت الفئران بعقار يثبط NLRP3 فقلّل إلى حد كبير هذه الآثار الضارة، مما يبرز أن موجة الحمض اللاكتيكي تغذي الالتهاب أساساً عبر هذا المسار. تقترح النتائج معاً أن الحمض اللاكتيكي محرك ذو وجهين للالتهاب، سواء عبر إعادة تشكيل استقلاب الخلية لصالح تنشيط الإنفلَمازوم أو عبر معالجة السيتوكينات الرئيسية مباشرة عندما تكون الحموضة شديدة.
لماذا تهم هذه النتائج
بالنسبة للمشاهد العام، الرسالة الرئيسية هي أن الحمض اللاكتيكي ليس مجرد ناتج جانبي غير مؤذ للتمرين أو المرض. داخل الخلايا المناعية المتوترة، يصبح إشارة تقول "زدوا النار"، مما يقوّي الالتهاب ويجعله أصعب في السيطرة. في حالات مثل الإنتان، حيث يرتفع كل من الحمض اللاكتيكي والحموضة، يمكن أن يقلب ذلك التوازن من دفاع مفيد إلى تلف خطير بالجسم. من خلال الكشف عن كيفية دفع الحمض اللاكتيكي الخلايا المناعية إلى هذا الوضع المفرط النشاط، وكيف يمكنه تشكيل الرسل الالتهابية بشكل مباشر، يشير هذا العمل إلى استراتيجيات جديدة لتبريد الالتهاب الضار عبر استهداف تعامل الخلايا مع الحموضة ونظام NLRP3.
الاستشهاد: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
الكلمات المفتاحية: الحمض اللاكتيكي, إنفلَمازوم, IL-1β, الإنتان, استقلاب المناعة