Clear Sky Science · pl
Kwas mlekowy napędza aktywację inflamasomu NLRP3 i cięcie cytokin podobne do kaspazy-1 poprzez zakwaszenie wewnątrzkomórkowe
Kiedy cząsteczka znana z ćwiczeń odwraca się przeciw nam
Kwas mlekowy słynie z pieczenia w mięśniach po intensywnym biegu, ale gromadzi się też podczas ciężkich zakażeń, takich jak sepsa. Badanie ujawnia, że kwas mlekowy może pełnić rolę wykraczającą poza zwykły produkt uboczny: wewnątrz komórek odpornościowych pomaga uruchomić potężne mechanizmy zapalne, a nawet samodzielnie chemicznie rozcina kluczowe przekaźniki układu odpornościowego. Zrozumienie tej podwójnej roli kwasu mlekowego może zmienić sposób, w jaki postrzegamy stan zapalny w sepsie, nowotworach i innych poważnych chorobach. 
Jak komórki odpornościowe wyczuwają zagrożenie
Nasza pierwsza linia obrony przed zakażeniem opiera się na komórkach odpornościowych wrodzonych, takich jak makrofagi, które szybko wykrywają zagrożenie i uwalniają sygnały alarmowe. Centralnym węzłem kontrolnym w tych komórkach jest inflamasom NLRP3, reagujący na szerokie spektrum zagrożeń i uruchamiający enzym, który przecina nieaktywne prekursory cytokin do ich aktywnych form. Te aktywne fragmenty, zwłaszcza IL-1β i IL-18, są następnie wydzielane, aby zmobilizować inne komórki odpornościowe. Choć ta odpowiedź może pomóc w zwalczaniu zakażeń, gdy wymyka się spod kontroli, przyczynia się do stanów zagrażających życiu, takich jak wstrząs septyczny.
Wykorzystanie paliwa, kwasowość komórki i przełącznik zapalny
Aby zasilić ten szybki system alarmowy, makrofagi przesuwają swój metabolizm w stronę glikolizy — szybkiego sposobu rozkładu cukru, który produkuje kwas mlekowy. Naukowcy wykazali, że po uruchomieniu NLRP3 komórki odpornościowe szybko zwiększają produkcję kwasu mlekowego i zatrzymują go wewnątrz. To nagromadzenie zakwasza wnętrze komórki i z kolei silnie wzmacnia składanie inflamasomu, aktywację enzymu i uwalnianie IL-1β. Kwaśne warunki na zewnątrz komórki blokują opuszczanie kwasu mlekowego, jeszcze bardziej pogłębiając wewnętrzne zakwaszenie i wzmacniając odpowiedź. Podniesienie pH otaczającego płynu do lekko zasadowego zapobiegało temu zakwaszeniu i niemal całkowicie wyłączało aktywność inflamasomu, nie zatrzymując przy tym samej produkcji kwasu mlekowego.
Wewnątrz komórki: reakcja łańcuchowa prowadząca do zapalenia
Idąc głębiej, zespół odkrył, że zakwaszenie wywołane kwasem mlekowym zaburza mitochondria — elektrownie komórki — i zwiększa ilość reaktywnych form tlenu, rodzaju chemicznego sygnału stresowego. Równocześnie aktywuje enzym czujny na stres o nazwie PKR i sprzyja jego fizycznej interakcji z mechanizmem NLRP3. Zarówno stres mitochondrialny, jak i aktywacja PKR okazały się niezbędne do pełnej funkcji inflamasomu. Blokowanie produkcji kwasu mlekowego lub uczynienie otoczenia bardziej zasadowym zmniejszało te sygnały stresowe, osłabiało partnerstwo PKR–NLRP3 i ograniczało formowanie kompleksu inflamasomu. 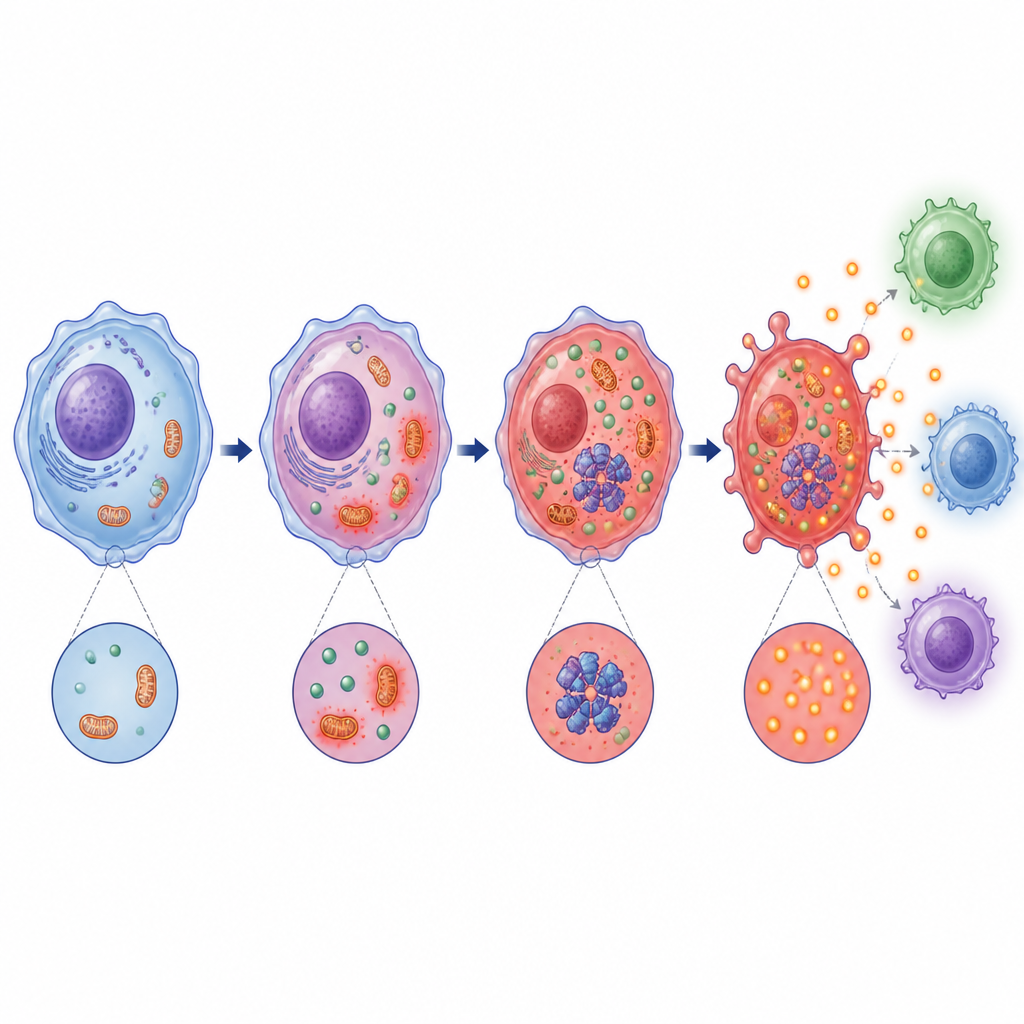
Kwas mlekowy jako chemiczny „skalpel”
Niespodziewanie kwas mlekowy pełnił też drugą, niezależną rolę. W ekstraktach komórkowych pozbawionych nienaruszonego mechanizmu inflamasomu samo dodanie kwasu mlekowego wystarczało, by rozciąć prekursory IL-1β i IL-18 do rozmiarów odpowiadających dojrzałym formom produkowanym przez zwykły enzym. To chemiczne cięcie wymagało kwaśnej, niezjonizowanej formy kwasu mlekowego i zależało od konkretnego miejsca w IL-1β, tego samego miejsca, którego normalnie używa enzym. Inne kwasy organiczne o podobnych grupach chemicznych mogły to robić w mniejszym stopniu, natomiast sam silny kwas mineralny był znacznie mniej skuteczny, co sugeruje, że specyficzna struktura kwasu mlekowego sprzyja temu precyzyjnemu procesowi-cięcia w bardzo kwaśnych warunkach.
Co to oznacza dla sepsy i innych chorób
Aby sprawdzić te pomysły in vivo, badacze użyli mysiego modelu sepsy polimikrobowej, ciężkiego, ogólnoustrojowego zakażenia. Podniesienie poziomu mleczanu we krwi u septycznych myszy zwiększyło IL-1β w krwi i jamie brzusznej, przyciągnęło więcej neutrofili do miejsca zakażenia, obniżyło temperaturę ciała i pogorszyło przeżywalność. Leczenie myszy lekiem blokującym NLRP3 w dużej mierze odwróciło te szkodliwe efekty, podkreślając, że skok kwasu mlekowego napędza zapalenie głównie przez tę ścieżkę. Razem te ustalenia sugerują, że kwas mlekowy jest dwutorowym motorem zapalenia — zarówno przez przekształcanie metabolizmu komórkowego na rzecz aktywacji inflamasomu, jak i przez bezpośrednie przetwarzanie kluczowych cytokin przy skrajnej kwasowości.
Dlaczego te odkrycia mają znaczenie
Dla laika kluczowy przekaz jest prosty: kwas mlekowy to nie tylko nieszkodliwy produkt uboczny wysiłku czy choroby. W zestresowanych komórkach odpornościowych staje się sygnałem „podkręć ogień”, wzmacniając i utrudniając kontrolę stanu zapalnego. W warunkach takich jak sepsa, gdzie rosną zarówno poziomy kwasu mlekowego, jak i kwasowość, może to przesunąć równowagę od pomocnej obrony do niebezpiecznego, ogólnoustrojowego uszkodzenia. Ujawniając, jak kwas mlekowy popycha komórki odpornościowe do tego nadaktywnego stanu i jak może bezpośrednio kształtować przekaźniki zapalne, praca ta wskazuje nowe strategie łagodzenia szkodliwego zapalenia przez celowanie w gospodarkę kwasowo-zasadową komórek i system NLRP3.
Cytowanie: Lin, HA., Lin, HC., Tsai, MH. et al. Lactic acid drives NLRP3 inflammasome activation and caspase-1–like cytokine cleavage via intracellular acidification. Cell Death Dis 17, 450 (2026). https://doi.org/10.1038/s41419-026-08708-y
Słowa kluczowe: kwas mlekowy, inflamasom, IL-1β, sepsa, metabolizm odpornościowy