Clear Sky Science · zh
软骨细胞中二聚体PKM2在骨关节炎中损害线粒体稳态
为何关节磨损值得关注
许多人忍受着骨关节炎带来的疼痛和僵硬,这是一种常见的关节疾病,会逐渐磨损我们骨骼之间的光滑软骨垫。一旦软骨损伤严重,主要的治疗选择往往是关节置换手术。本研究探讨了软骨细胞内一个隐藏的能量开关,该开关似乎能够加速或减缓这种损坏。通过理解并调控这一开关,研究指向了可能保护关节、延缓甚至避免手术的新型治疗策略。
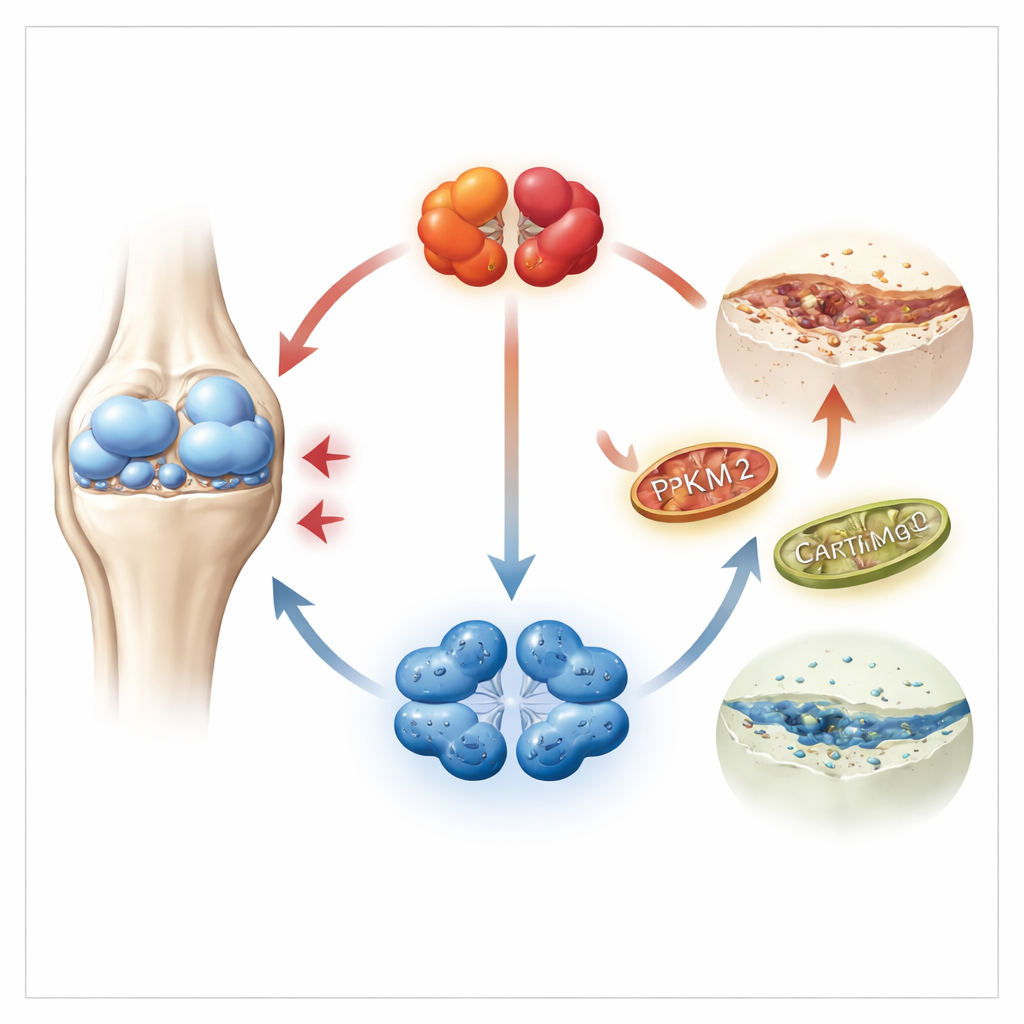
深入观察疼痛软骨内部
软骨由软骨细胞构建和维持,这类专门的细胞生活在低氧环境中,主要依赖糖酵解获得能量。研究者将注意力集中在这一过程中的关键酶PKM2上,PKM2可以存在两种构象:一个紧密的四聚体和一个较松散的二聚体。通过分析来自人类软骨的大型基因组数据集以及来自患者和小鼠的样本,他们发现骨关节炎软骨中PKM2水平显著升高,而其同源体PKM1几乎不可检测。重要的是,病变软骨中向二聚体形式的PKM2转变更为明显,而二聚体型PKM2更为人所知的是调控细胞行为,而非直接用于产生能量。
将破坏性循环转为保护性循环
研究团队接着探究降低PKM2或将其保持在四聚体状态会产生何种影响。在体外培养的软骨细胞中,降低PKM2水平或使用一种名为TEPP-46的小分子将PKM2锁定为四聚体,会使细胞更倾向于合成软骨而非分解软骨。细胞产生更多赋予软骨强度的结构蛋白,且分解组织的酶减少。在一种通过膝关节不稳定诱发骨关节炎的小鼠模型中,注射降低PKM2或稳定其四聚体形式的处理能够保留软骨结构,降低损伤评分,并改善行走模式及与疼痛相关的反应。
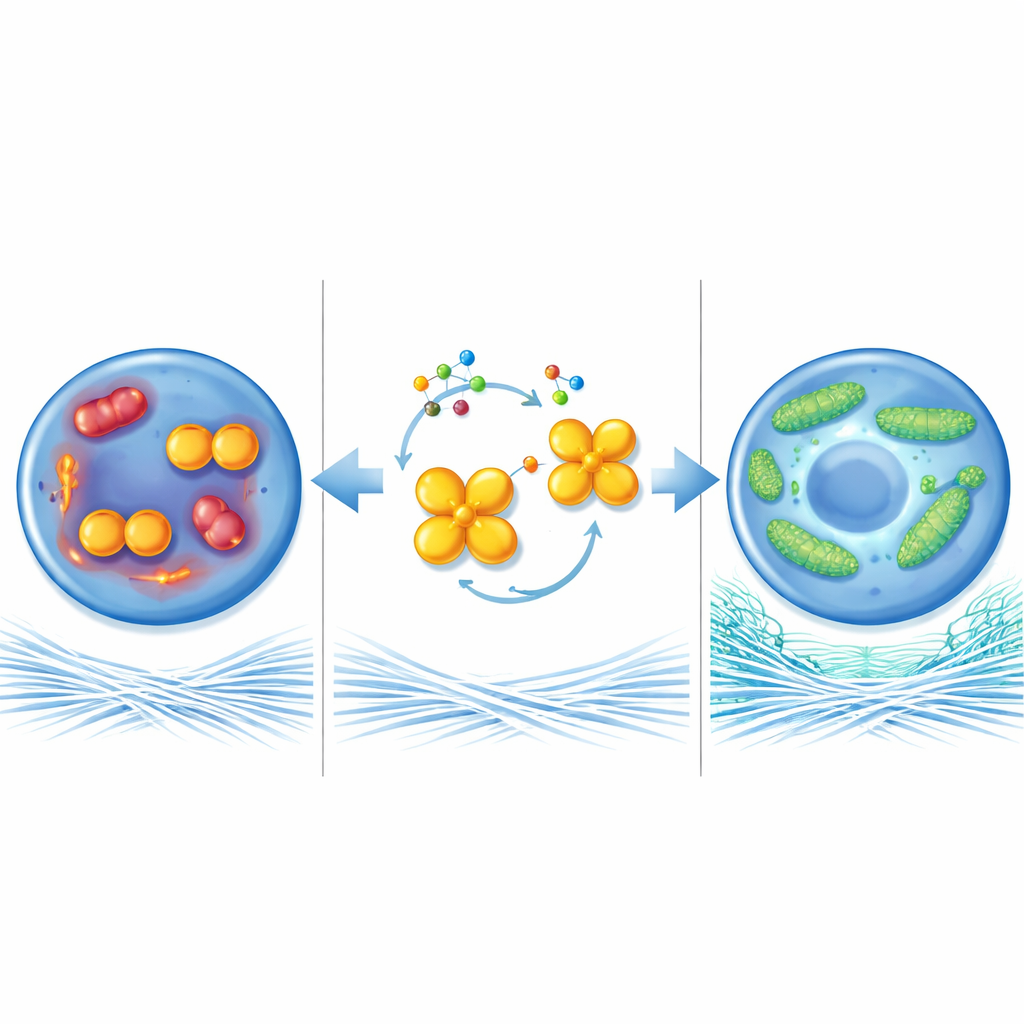
保护细胞的能量工厂
为理解该酶如何影响软骨健康,研究者们考察了线粒体——细胞内微小的能量工厂。在类骨关节炎条件下,软骨细胞的线粒体变得短小、破碎,产生更多有害的活性分子且能量产出减少。当去除PKM2或迫使其形成四聚体时,线粒体反而形成长而连通的网络,更有效地燃烧底物并生成更多高能分子。这种线粒体“融合”在很大程度上依赖于另一种蛋白MFN1,它有助于将线粒体连接在一起。病变软骨中MFN1水平较低,但当PKM2二聚体水平下降时,MFN1会上升。在PKM2缺失小鼠关节中阻断MFN1会抹去保护作用并使软骨损伤继续发展,表明MFN1在这一通路中起关键作用。
切断有害的信号链
研究进一步揭示了一条将PKM2与线粒体变化相连的信号链。松散的二聚体PKM2与ERK发生物理相互作用,ERK是一种对压力和炎症作出响应的著名信号蛋白。在类骨关节炎的刺激下,这种相互作用增强,ERK活性上升,进而抑制MFN1并促使线粒体走向破碎、不健康的状态。降低PKM2二聚化或将PKM2锁定为四聚体会削弱PKM2–ERK相互作用,降低ERK活性并恢复MFN1水平。有趣的是,相关的融合蛋白MFN2受影响的方式不同,提示MFN1在维持软骨细胞及其线粒体平衡方面具有独特且不可替代的作用。
对未来关节护理的意义
简而言之,研究表明,当PKM2以二聚体形式在软骨细胞内累积时,会扰乱细胞的能量系统,削弱合成软骨的机制并加速骨关节炎进程。将PKM2偏向四聚体形式或以其他方式减少二聚体,有助于维持线粒体健康并促进软骨修复。在小鼠中,这一策略不仅保留了关节组织,还减轻了与疼痛相关的行为反应。尽管在这些方法进入临床之前仍需更多研究,针对PKM2二聚化的干预提供了一条有前景的新途径,可能帮助患者在需要手术之前享有更长时间的无痛活动能力。
引用: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
关键词: 骨关节炎, 软骨, 线粒体, PKM2, 融合蛋白1(mitofusin 1)