Clear Sky Science · pl
Dimeryczne PKM2 w chondrocytach zaburza homeostazę mitochondrialną w chorobie zwyrodnieniowej stawów
Dlaczego zużyte stawy mają znaczenie
Wiele osób żyje z bólem i sztywnością spowodowaną chorobą zwyrodnieniową stawów — powszechnym schorzeniem, które stopniowo ściera gładką chrząstkę amortyzującą kości. Gdy chrząstka jest poważnie uszkodzona, główną opcją leczenia pozostaje wymiana stawu. Badanie to odkrywa ukryty przełącznik energetyczny w komórkach chrząstki, który zdaje się przyspieszać lub spowalniać to niszczenie. Zrozumienie i kontrola tego przełącznika wskazują drogę do nowych terapii, które mogą chronić stawy i opóźnić lub nawet zapobiec konieczności operacji.
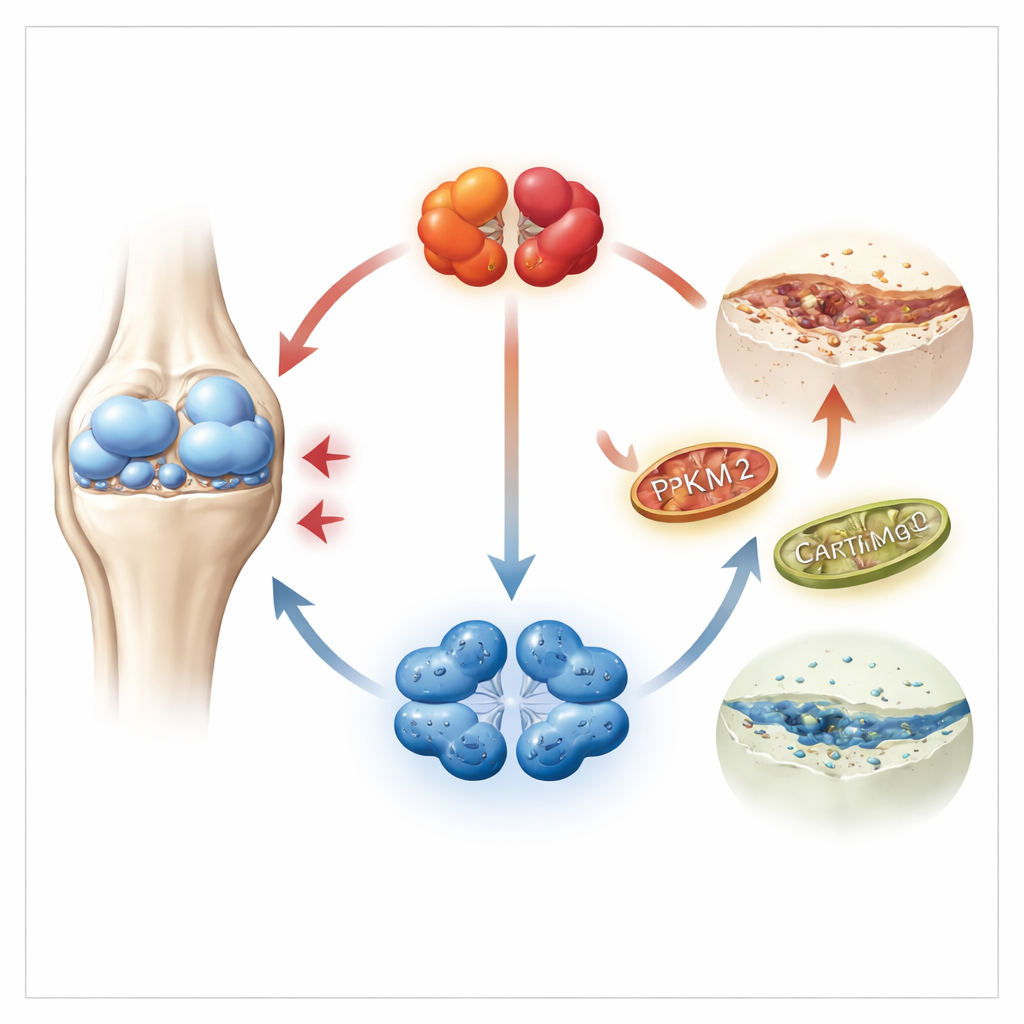
Uważniejsze spojrzenie do wnętrza bolącej chrząstki
Chrząstkę budują i utrzymują chondrocyty — wyspecjalizowane komórki żyjące w niskotlenowym środowisku, które głównie polegają na spalaniu cukrów jako źródle energii. Badacze skupili się na kluczowym enzymie tego procesu, PKM2, który może występować w dwóch konformacjach: ściśle upakowanej formie tetrameru i luźniejszej formie dimeru. Wykorzystując duże zbiory genetyczne z ludzkiej chrząstki oraz próbki od pacjentów i myszy, stwierdzili, że poziomy PKM2 były silnie podwyższone w chrząstce chorej na chorobę zwyrodnieniową, podczas gdy jego bliźniaczy izoenzym PKM1 był praktycznie nieobecny. Co istotne, w tkance chorobowo zmienionej występował przesuw w kierunku formy dimerowej PKM2, lepiej znanej z regulowania zachowania komórek niż z produkcji energii.
Przekształcenie cyklu destrukcji w cykl ochronny
Zespół następnie zapytał, co się stanie, gdy poziom PKM2 zostanie obniżony lub utrzymany w formie tetrameru. W komórkach chrząstki hodowanych w laboratorium obniżenie poziomu PKM2 lub użycie małocząsteczkowego związku TEPP-46, który blokuje PKM2 w stanie tetrameru, przesunęło równowagę w stronę budowy chrząstki zamiast jej rozpadu. Komórki wytwarzały więcej białek strukturalnych nadających chrząstce wytrzymałość i mniej enzymów rozkładających tkankę. W modelu myszy, w którym choroba zwyrodnieniowa była wywołana niestabilnym stawem kolanowym, iniekcje zmniejszające PKM2 lub stabilizujące jego formę tetrameru chroniły strukturę chrząstki, obniżały oceny uszkodzeń oraz poprawiały wzorce chodu i reakcje związane z bólem.
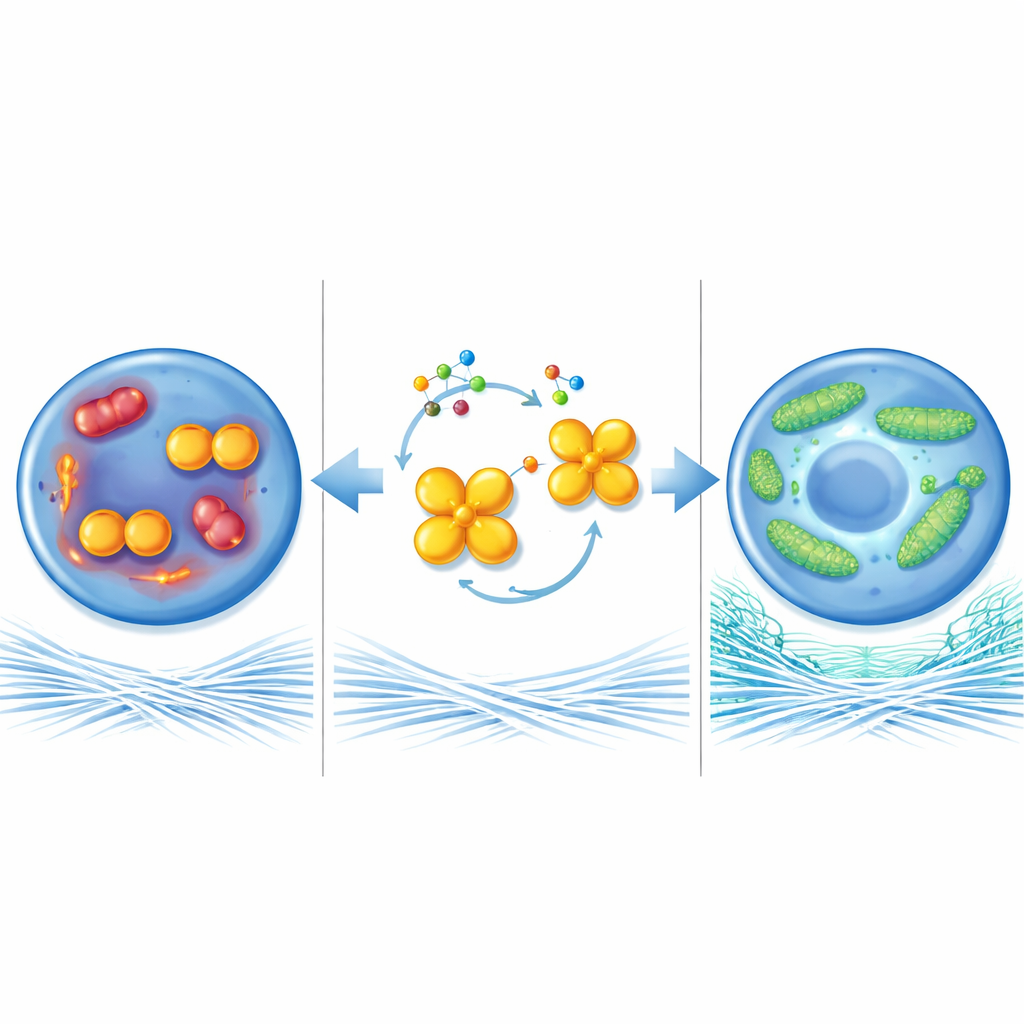
Ochrona elektrowni komórkowych
Aby zrozumieć, jak ten enzym wpływa na zdrowie chrząstki, badacze przyjrzeli się mitochondriom — drobnym elektrowniom w komórkach. W warunkach przypominających chorobę zwyrodnieniową mitochondria w chondrocytach stawały się małe i pofragmentowane, produkowały więcej szkodliwych reaktywnych cząsteczek i wytwarzały mniej energii. Gdy PKM2 został usunięty lub wymuszono jego tetramerową postać, mitochondria tworzyły długie, połączone sieci, bardziej efektywnie spalały substraty i wytwarzały więcej wysokoenergetycznych cząsteczek. Ta mitochondrialna „fuzja” zależała w dużej mierze od innego białka, MFN1, które pomaga łączyć mitochondria. Poziomy MFN1 były niskie w chorej chrząstce, ale wzrastały, gdy spadała ilość dimerów PKM2. Zablokowanie MFN1 w stawach myszy pozbawionych PKM2 znosiło efekty ochronne i umożliwiało postęp uszkodzeń chrząstki, co pokazuje, że MFN1 jest kluczowym elementem tej ścieżki.
Przerwanie szkodliwego łańcucha sygnałowego
Badanie dodatkowo odsłoniło łańcuch sygnałowy łączący PKM2 ze zmianami mitochondrialnymi. Luźna, dimerowa forma PKM2 fizycznie wchodziła w interakcję z ERK — dobrze znanym białkiem sygnalizacyjnym reagującym na stres i zapalenie. W warunkach podobnych do choroby zwyrodnieniowej ta interakcja się wzmacniała, a ERK stawał się bardziej aktywny, co z kolei tłumiło MFN1 i przesuwało mitochondria w kierunku stanu pofragmentowanego i niezdrowego. Zmniejszenie dimeryzacji PKM2 lub zablokowanie PKM2 w postaci tetrameru osłabiało interakcję PKM2–ERK, obniżało aktywność ERK i przywracało poziomy MFN1. Co interesujące, pokrewne białko fuzyjne MFN2 było regulowane inaczej, co sugeruje, że MFN1 pełni unikalną, nieredundantną rolę w utrzymaniu równowagi chondrocytów i ich mitochondriów.
Co to oznacza dla przyszłej opieki nad stawami
Mówiąc prosto, praca pokazuje, że gdy PKM2 gromadzi się w formie dimeru w komórkach chrząstki, zaburza ona systemy energetyczne komórki, osłabia mechanizmy budujące chrząstkę i przyspiesza postęp choroby zwyrodnieniowej stawów. Przesunięcie PKM2 w stronę tetrameru lub w inny sposób zmniejszenie ilości dimeru pomaga mitochondriom pozostać zdrowymi i sprzyja naprawie chrząstki. U myszy ta strategia nie tylko chroniła tkankę stawową, ale także łagodziła zachowania związane z bólem. Choć przed wprowadzeniem takich podejść do praktyki klinicznej potrzebne są dalsze badania, celowanie w dimeryzację PKM2 otwiera obiecującą nową drogę do spowolnienia lub zapobiegania zużyciu stawów, co potencjalnie zapewni pacjentom więcej lat komfortowego poruszania się przed koniecznością operacji.
Cytowanie: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
Słowa kluczowe: choroba zwyrodnieniowa stawów, chrząstka, mitochondria, PKM2, mitofuzyna 1