Clear Sky Science · nl
Dimerisch PKM2 in chondrocyten verstoort mitochondriale homeostase bij artrose
Waarom versleten gewrichten ertoe doen
Veel mensen leven met de pijn en stijfheid van artrose, een veelvoorkomende gewrichtsziekte die het gladde kraakbeen dat onze botten dempt langzaam afslijt. Zodra dat kraakbeen ernstig beschadigd is, is de belangrijkste optie vaak gewrichtsvervanging. Deze studie onderzoekt een verborgen energieschakelaar in kraakbeencellen die de schade lijkt te versnellen of te vertragen. Door die schakelaar te begrijpen en te beheersen, wijzen de bevindingen op nieuwe behandelingen die gewrichten kunnen beschermen en de noodzaak van operaties kunnen uitstellen of mogelijk voorkomen.
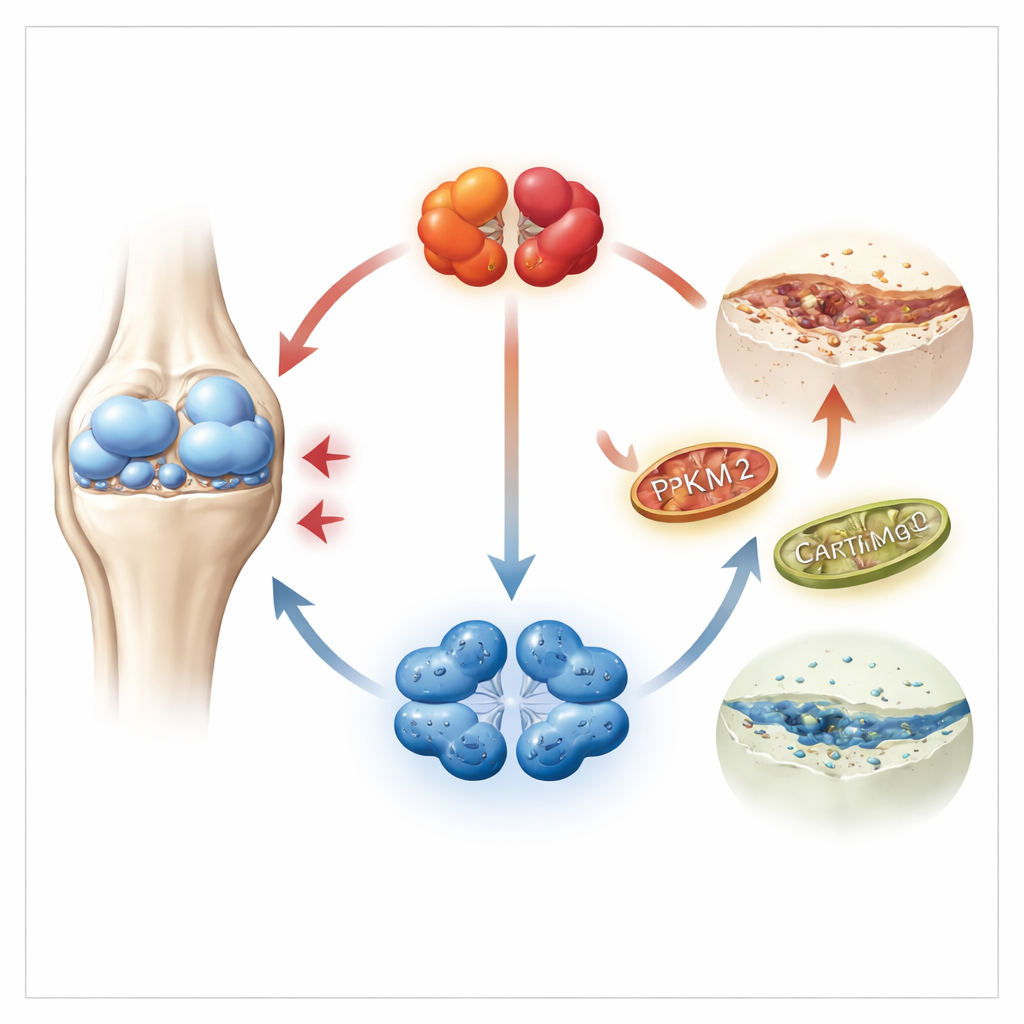
Een nadere blik in pijnlijk kraakbeen
Kraakbeen wordt opgebouwd en onderhouden door chondrocyten, gespecialiseerde cellen die in een laag-zuurstofomgeving leven en vooral op suikerverbranding vertrouwen voor energie. De onderzoekers richtten zich op een sleutelenzym in dit proces, PKM2, dat in twee vormen kan voorkomen: een strak verpakte vierdelige vorm en een lossere tweedelige vorm. Met behulp van grote genetische datasets van menselijk kraakbeen en monsters van patiënten en muizen vonden ze dat PKM2 sterk verhoogd was in artrotisch kraakbeen, terwijl het zusterenzym PKM1 nauwelijks detecteerbaar was. Belangrijk was dat ziek kraakbeen een verschuiving vertoonde naar de tweedelige (dimeer) versie van PKM2, die vaker geassocieerd wordt met het regelen van celgedrag dan met het produceren van energie.
Een destructieve cyclus ombuigen naar bescherming
Het team vroeg zich vervolgens af wat er gebeurt als PKM2 wordt verminderd of in zijn vierdelige vorm gehouden. In in-vitro gekweekte kraakbeencellen zorgde verlaging van PKM2, of het gebruik van een klein molecuul genaamd TEPP-46 dat PKM2 in de vierdelige toestand vergrendelt, voor een verschuiving naar opbouw van kraakbeen in plaats van afbraak. Cellen produceerden meer structurele eiwitten die kraakbeen sterkte geven en minder enzymen die het weefsel afbreken. In een muismodel waarin artrose werd veroorzaakt door een onstabiele knie, zorgden injecties die PKM2 verlaagden of de vierdelige vorm stabiliseerden voor behoud van de kraakbeenstructuur, lagere schade-scores en verbeterde looppatronen en pijnachtige reacties.
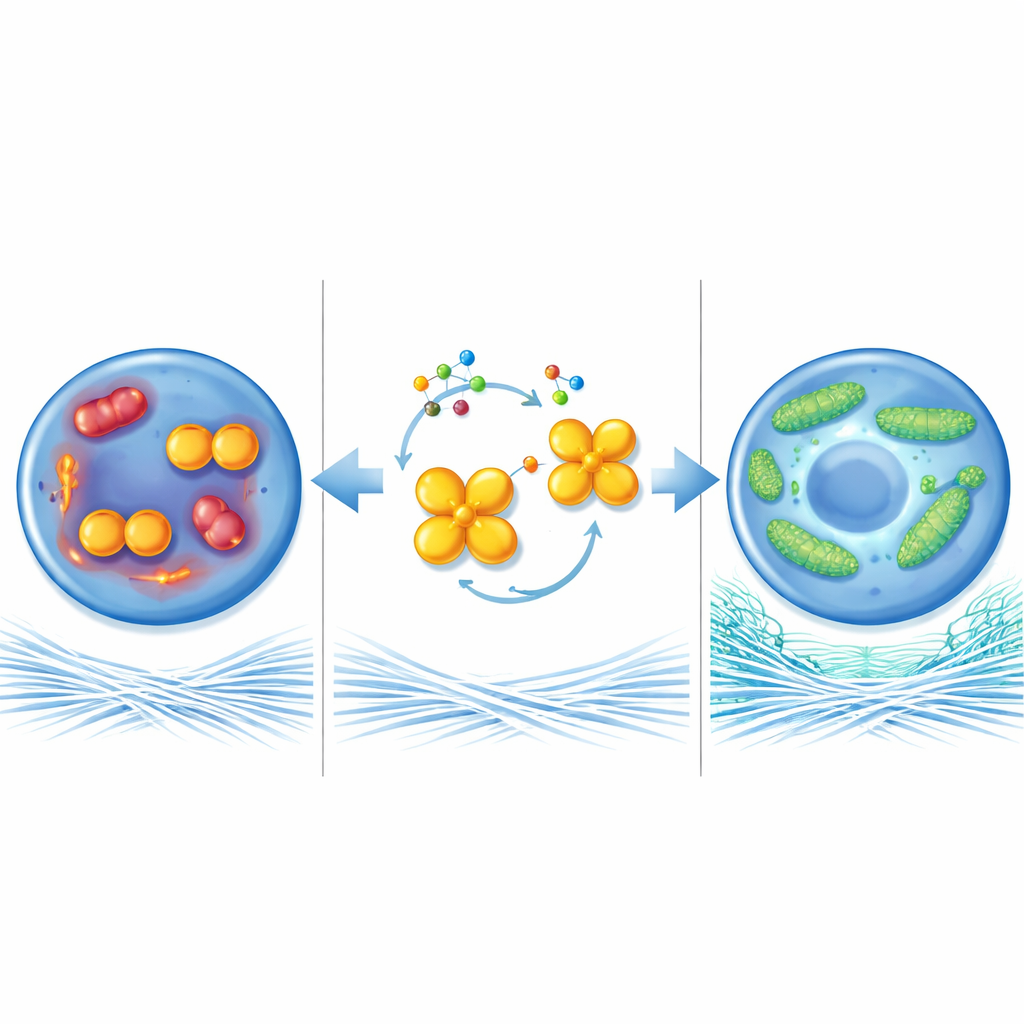
De energiefabriekjes van de cel beschermen
Om te begrijpen hoe dit enzym de gezondheid van kraakbeen beïnvloedt, onderzochten de onderzoekers mitochondriën, de kleine energiefabriekjes in cellen. Onder artroseachtige omstandigheden werden mitochondriën in chondrocyten klein en gefragmenteerd, produceerden ze meer schadelijke reactieve moleculen en genereerden ze minder energie. Wanneer PKM2 werd verwijderd of geforceerd in zijn vierdelige vorm werd gehouden, vormden mitochondriën lange, verbonden netwerken, verbrandden brandstof efficiënter en maakten meer energierijke moleculen. Deze mitochondriale "fusie" bracht grotendeels afhing van een ander eiwit, MFN1, dat helpt mitochondriën met elkaar te verbinden. MFN1-niveaus waren laag in ziek kraakbeen maar stegen toen de PKM2-dimeerniveaus daalden. Het blokkeren van MFN1 in de gewrichten van PKM2-deficiënte muizen wist de beschermende effecten uit en liet kraakbeenschade voortschrijden, wat aantoont dat MFN1 een sleutelrol speelt in dit pad.
De schadelijke signaalketen doorbreken
De studie onthulde verder een signaalketen die PKM2 verbindt met mitochondriale veranderingen. De losse, tweedelige PKM2 ging fysiek in interactie met ERK, een bekend signaureiwit dat reageert op stress en ontsteking. Onder artroseachtige stimulatie werd deze interactie sterker en werd ERK actiever, wat op zijn beurt MFN1 onderdrukte en mitochondriën naar een gefragmenteerde, ongezonde staat duwde. Het verminderen van PKM2-dimerisatie of het vergrendelen van PKM2 in tetrameren verzwakte deze PKM2–ERK-interactie, verminderde ERK-activiteit en herstelde MFN1-niveaus. Interessant was dat een gerelateerd fusie-eiwit, MFN2, anders werd beïnvloed, wat suggereert dat MFN1 een unieke, niet-redundante rol heeft in het in balans houden van chondrocyten en hun mitochondriën.
Wat dit betekent voor toekomstige zorg van gewrichten
Kort gezegd toont het werk aan dat wanneer PKM2 zich ophoopt in zijn tweedelige vorm in kraakbeencellen, het de energiehuishouding van de cel verstoort, de kraakbeenopbouw verzwakt en artrose versnelt. Het verschuiven van PKM2 naar zijn vierdelige vorm, of het op andere wijze verminderen van de tweedelige versie, helpt mitochondriën gezond te blijven en bevordert kraakbeenherstel. Bij muizen beschermde deze strategie niet alleen het gewrichtsweefsel maar verzachtte ook pijnlijk gedrag. Hoewel meer onderzoek nodig is voordat zulke benaderingen de kliniek bereiken, biedt het richten op PKM2-dimerisatie een veelbelovende nieuwe manier om slijtage van gewrichten te vertragen of te voorkomen, waardoor patiënten mogelijk meer jaren comfortabel kunnen bewegen voordat een operatie nodig wordt.
Bronvermelding: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
Trefwoorden: artrose, kraakbeen, mitochondriën, PKM2, mitofusine 1