Clear Sky Science · fr
La PKM2 dimérique dans les chondrocytes compromet l’homéostasie mitochondriale dans l’arthrose
Pourquoi les articulations usées comptent
Beaucoup de personnes vivent avec la douleur et la raideur de l’arthrose, une maladie articulaire fréquente qui use progressivement le cartilage lisse qui amortit nos os. Une fois ce cartilage gravement endommagé, la principale option reste la prothèse articulaire. Cette étude explore un commutateur énergétique caché à l’intérieur des cellules du cartilage qui semble accélérer ou ralentir cette dégradation. En comprenant et en contrôlant ce commutateur, ce travail ouvre la voie à de nouveaux traitements susceptibles de protéger les articulations et de retarder, voire d’éviter, la nécessité d’une intervention chirurgicale.
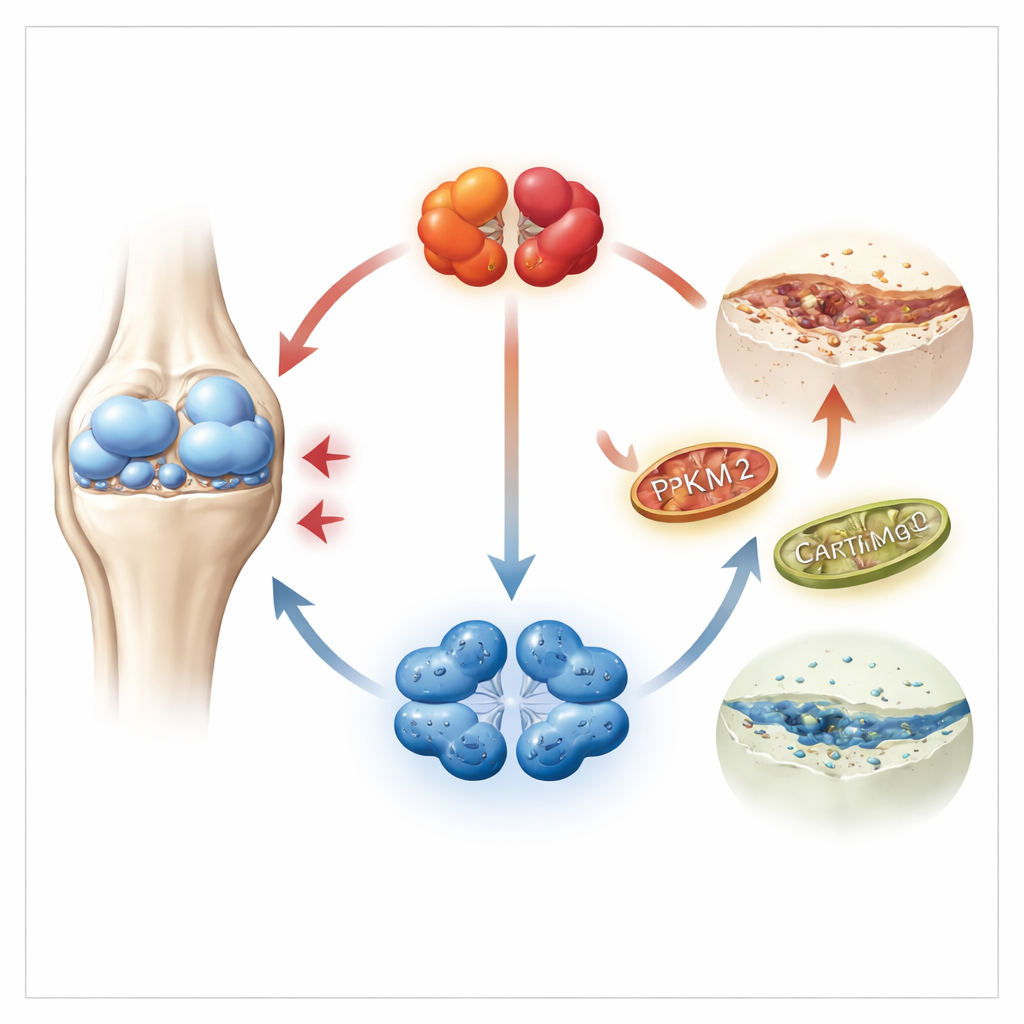
Un examen approfondi du cartilage douloureux
Le cartilage est construit et maintenu par les chondrocytes, des cellules spécialisées qui vivent dans un environnement pauvre en oxygène et s’appuient principalement sur la glycolyse pour produire de l’énergie. Les chercheurs se sont concentrés sur une enzyme clé de ce processus, la PKM2, qui peut exister sous deux formes : une forme tétramérique compactée et une forme dimérique plus lâche. En utilisant de larges jeux de données génétiques issus de cartilage humain, ainsi que des échantillons de patients et de souris, ils ont constaté que les niveaux de PKM2 étaient fortement augmentés dans le cartilage arthrosique, tandis que sa forme sœur PKM1 était à peine détectable. De façon importante, le cartilage malade montrait un basculement vers la forme dimérique de PKM2, mieux connue pour réguler le comportement cellulaire que pour produire de l’énergie.
Transformer un cercle vicieux en mécanisme protecteur
L’équipe a ensuite demandé ce qui se passe si l’on réduit la PKM2 ou si on la maintient sous sa forme tétramérique. Dans des chondrocytes cultivés en laboratoire, la diminution de PKM2, ou l’utilisation d’une petite molécule nommée TEPP-46 qui verrouille PKM2 en tétramères, a favorisé la construction du cartilage plutôt que sa dégradation. Les cellules produisaient davantage des protéines structurales conférant leur résistance au cartilage et moins d’enzymes qui dégradent le tissu. Dans un modèle murin d’arthrose induite par une instabilité du genou, des injections réduisant PKM2 ou stabilisant sa forme tétramérique ont préservé la structure du cartilage, abaissé les scores de lésions et amélioré la mobilité et les réponses liées à la douleur.
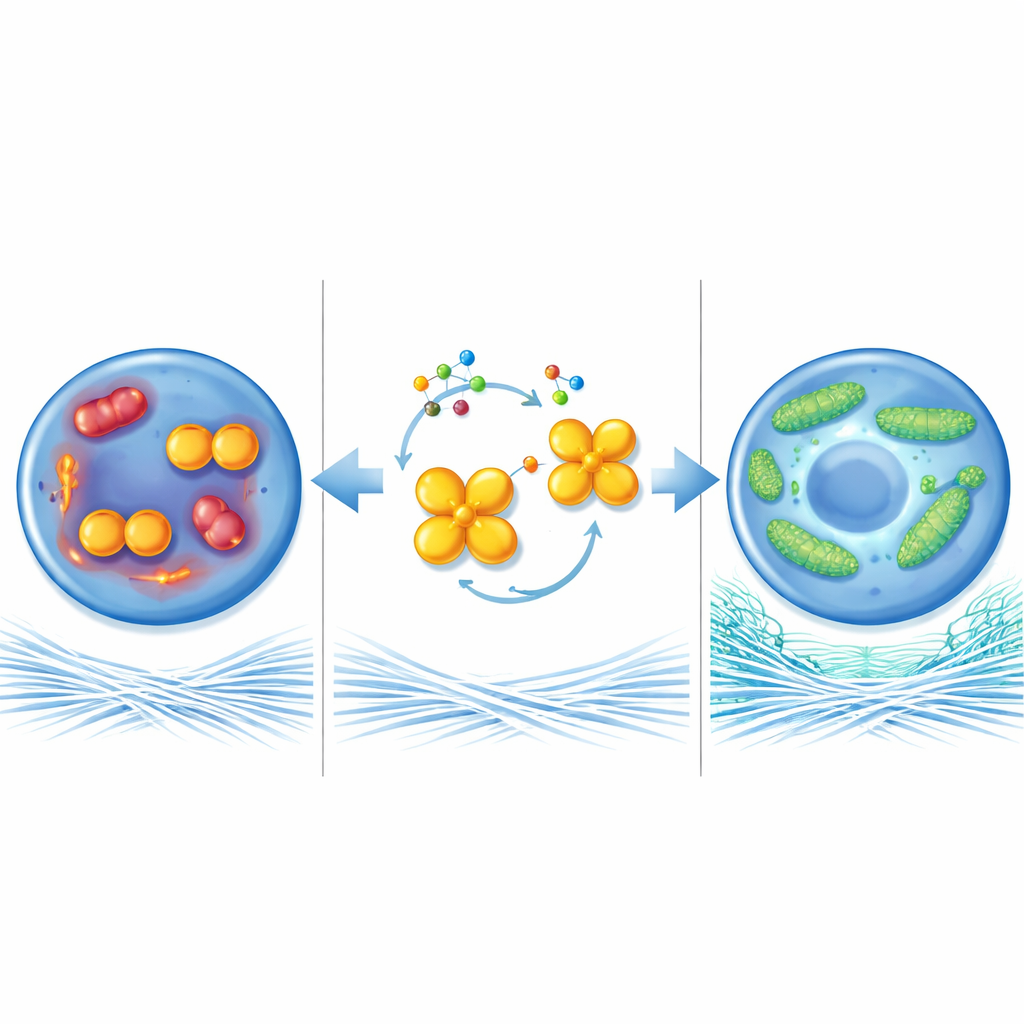
Protéger les centrales énergétiques de la cellule
Pour comprendre comment cette enzyme influence la santé du cartilage, les chercheurs ont examiné les mitochondries, les petites centrales énergétiques à l’intérieur des cellules. Dans des conditions rappelant l’arthrose, les mitochondries des chondrocytes devenaient petites et fragmentées, produisaient davantage d’espèces réactives nocives et généraient moins d’énergie. Lorsque PKM2 était supprimée ou contrainte à sa forme tétramérique, les mitochondries formaient au contraire de longs réseaux connectés, utilisaient le carburant plus efficacement et produisaient davantage de molécules riches en énergie. Cette « fusion » mitochondriale dépendait en grande partie d’une autre protéine, MFN1, qui aide à relier les mitochondries entre elles. Les niveaux de MFN1 étaient faibles dans le cartilage malade mais augmentaient lorsque les niveaux de dimères de PKM2 diminuaient. Bloquer MFN1 dans les articulations de souris déficientes en PKM2 annulait les effets protecteurs et permettait la progression des lésions cartilagineuses, montrant que MFN1 joue un rôle clé dans cette voie.
Rompre la chaîne de signal nocive
L’étude a en outre mis au jour une chaîne de signalisation reliant PKM2 aux changements mitochondriaux. La PKM2 dimérique interagissait physiquement avec ERK, une protéine de signalisation bien connue qui répond au stress et à l’inflammation. Sous une stimulation de type arthrosique, cette interaction se renforçait et ERK devenait plus actif, ce qui, à son tour, supprimait MFN1 et poussait les mitochondries vers un état fragmenté et délétère. Réduire la dimérisation de PKM2 ou verrouiller PKM2 en tétramères affaiblissait cette interaction PKM2–ERK, diminuait l’activité d’ERK et rétablissait les niveaux de MFN1. Fait intéressant, une protéine de fusion apparentée, MFN2, était influencée différemment, ce qui suggère que MFN1 a un rôle unique et non redondant pour maintenir l’équilibre des chondrocytes et de leurs mitochondries.
Ce que cela signifie pour la prise en charge future des articulations
En résumé, ce travail montre que lorsque PKM2 s’accumule sous sa forme dimérique dans les chondrocytes, elle perturbe les systèmes énergétiques de la cellule, affaiblit la machinerie de construction du cartilage et accélère l’arthrose. Bascule r PKM2 vers sa forme tétramérique, ou réduction de la forme dimérique, aide les mitochondries à rester saines et favorise la réparation du cartilage. Chez la souris, cette stratégie a non seulement préservé le tissu articulaire mais aussi atténué les comportements liés à la douleur. Bien que des recherches supplémentaires soient nécessaires avant que de telles approches n’atteignent la clinique, cibler la dimérisation de PKM2 offre une voie prometteuse pour ralentir ou prévenir l’usure articulaire, permettant potentiellement aux patients de conserver des années de mobilité confortable avant que la chirurgie ne devienne nécessaire.
Citation: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
Mots-clés: arthrose, cartilage, mitochondries, PKM2, mitofusine 1