Clear Sky Science · de
Dimerisches PKM2 in Chondrozyten stört die mitochondriale Homöostase bei Osteoarthritis
Warum abgenutzte Gelenke wichtig sind
Viele Menschen leben mit den Schmerzen und der Steifigkeit der Arthrose, einer weit verbreiteten Gelenkerkrankung, die langsam den glatten Knorpel, der unsere Knochen polstert, abbaut. Sobald dieser Knorpel stark beschädigt ist, bleibt oft nur noch ein Gelenkersatz. Diese Studie untersucht einen verborgenen Energieschalter in Knorpelzellen, der offenbar das Fortschreiten dieser Schädigung beschleunigen oder verlangsamen kann. Durch das Verständnis und die Kontrolle dieses Schalters weisen die Arbeiten auf neue Therapien hin, die Gelenke schützen und das Auffinden einer Operation verzögern oder sogar verhindern könnten.
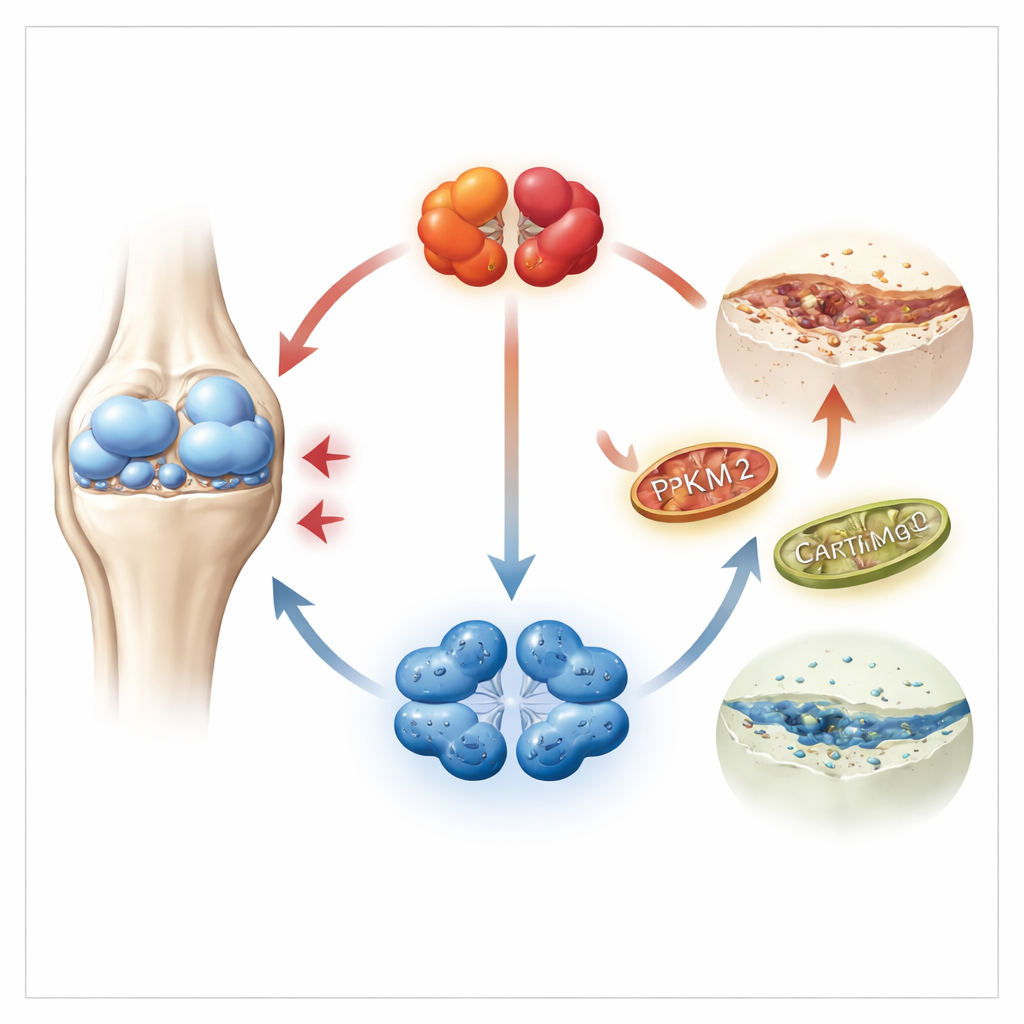
Ein genauerer Blick in schmerzenden Knorpel
Knorpel wird von und durch Chondrozyten aufgebaut und erhalten — spezialisierte Zellen, die in einer sauerstoffarmen Umgebung leben und vorwiegend auf Zuckerverbrennung als Energiequelle angewiesen sind. Die Forschenden konzentrierten sich auf ein Schlüsselenzym dieses Prozesses namens PKM2, das in zwei Gestalten vorkommen kann: eine eng gepackte vierteilige Form und eine lockerere zweiteilige Form. Anhand großer genetischer Datensätze aus menschlichem Knorpel sowie Proben von Patienten und Mäusen stellten sie fest, dass die PKM2-Spiegel in arthrotischem Knorpel stark erhöht waren, während die Schwesterform PKM1 kaum nachweisbar war. Wichtig ist, dass kranker Knorpel eine Verschiebung zugunsten der zweiteiligen (Dimer-)Version von PKM2 zeigte, die eher für die Steuerung des Zellverhaltens als für die Energiegewinnung bekannt ist.
Aus einem zerstörerischen Kreislauf einen schützenden machen
Das Team fragte dann, was passiert, wenn PKM2 reduziert oder in seiner vierteiligen Form gehalten wird. In im Labor kultivierten Knorpelzellen verschob das Herabsetzen von PKM2 oder der Einsatz eines kleinen Moleküls namens TEPP-46, das PKM2 in seinem tetrameren Zustand fixiert, das Gleichgewicht zugunsten des Aufbaus von Knorpel statt seines Abbaus. Die Zellen produzierten mehr der Strukturproteine, die dem Knorpel Festigkeit verleihen, und weniger der Enzyme, die das Gewebe abbauen. In einem Mausmodell, in dem Arthrose durch ein instabiles Knie ausgelöst wird, bewahrten Injektionen, die PKM2 reduzierten oder seine vierteilige Form stabilisierten, die Knorpelstruktur, senkten Schadenswerte und verbesserten Gangmuster sowie schmerzbezogene Reaktionen.
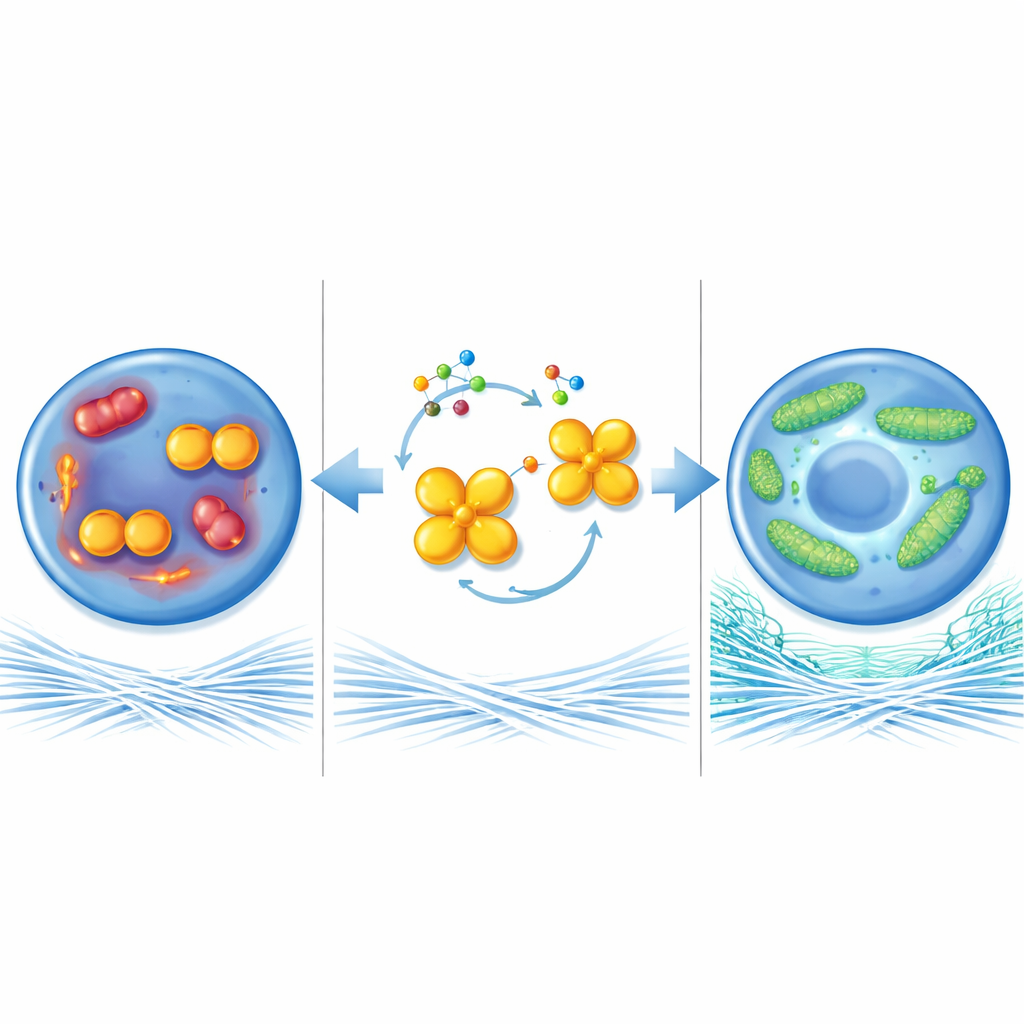
Die Kraftwerke der Zelle schützen
Um zu verstehen, wie dieses Enzym die Knorpelgesundheit beeinflusst, betrachteten die Forschenden die Mitochondrien, die winzigen Kraftwerke in den Zellen. Unter arthroseähnlichen Bedingungen wurden die Mitochondrien in Chondrozyten klein und fragmentiert, produzierten mehr schädliche reaktive Moleküle und erzeugten weniger Energie. Wenn PKM2 entfernt oder in seine vierteilige Form gezwungen wurde, bildeten die Mitochondrien stattdessen lange, verbundene Netzwerke, verstoffwechselten Brennstoff effizienter und stellten mehr energiereiche Moleküle her. Diese mitochondriale „Fusion“ hing größtenteils von einem anderen Protein, MFN1, ab, das dabei hilft, Mitochondrien zu verbinden. MFN1-Spiegel waren in krankem Knorpel niedrig, stiegen aber, als die PKM2-Dimer-Spiegel sanken. Das Blockieren von MFN1 in den Gelenken PKM2-defizienter Mäuse beseitigte die schützenden Effekte und ließ den Knorpelschaden fortschreiten — ein Hinweis darauf, dass MFN1 eine Schlüsselrolle in dieser Signalkette spielt.
Die schädliche Signalkette durchbrechen
Die Studie legte darüber hinaus eine Signalkaskade offen, die PKM2 mit mitochondrialen Veränderungen verbindet. Die lockere, zweiteilige PKM2 wechselwirkte physisch mit ERK, einem bekannten Signalmolekül, das auf Stress und Entzündung reagiert. Unter arthroseähnlicher Stimulation verstärkte sich diese Interaktion und ERK wurde aktiver, was wiederum MFN1 unterdrückte und die Mitochondrien in einen fragmentierten, ungesunden Zustand drängte. Die Verringerung der PKM2-Dimerisierung oder das Fixieren von PKM2 in Tetrameren schwächte diese PKM2–ERK-Interaktion, reduzierte die ERK-Aktivität und stellte die MFN1-Spiegel wieder her. Interessanterweise wurde ein verwandtes Fusionsprotein, MFN2, anders beeinflusst, was darauf hindeutet, dass MFN1 eine einzigartige, nicht redundante Rolle bei der Aufrechterhaltung des Gleichgewichts von Knorpelzellen und ihren Mitochondrien hat.
Was das für die künftige Gelenkversorgung bedeutet
Kurz gesagt zeigen die Ergebnisse, dass sich PKM2 in seiner zweiteiligen Form in Knorpelzellen ansammelt, die Energiewirtschaft der Zelle stört, die knorpelaufbauenden Mechanismen schwächt und die Arthrose beschleunigt. Eine Verschiebung von PKM2 hin zur vierteiligen Form oder anderweitige Reduktion der dimeren Version unterstützt die mitochondriale Gesundheit und fördert die Knorpelreparatur. Bei Mäusen bewahrte diese Strategie nicht nur das Gelenkgewebe, sondern linderte auch schmerzbezogenes Verhalten. Obwohl weitere Forschung nötig ist, bevor solche Ansätze klinisch eingesetzt werden können, bietet die gezielte Beeinflussung der PKM2-Dimerisierung einen vielversprechenden neuen Weg, das Gelenkverschleißs zu verlangsamen oder zu verhindern und Patienten potenziell mehr Jahre schmerzfreier Bewegung vor einer Operation zu ermöglichen.
Zitation: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
Schlüsselwörter: Arthrose, Knorpel, Mitochondrien, PKM2, Mitofusin 1