Clear Sky Science · he
צורת דימר של PKM2 בכונדרוציטים פוגעת בהומאוסטזיס המיטוכונדריאלי באוסטאוארתריטיס
מדוע פרקים שחוקים חשובים
רבים חיים עם הכאב והנוקשות של אוסטאוארתריטיס, מחלת מפרקים שכיחה שמלבינה בהדרגה את הסחוס החלק שמרפד את העצמות. ברגע שהסחוס ניזוק בצורה חמורה, האופציה העיקרית היא ניתוח החלפת מפרק. המחקר הזה בוחן מתג אנרגיה נסתר בתוך תאי הסחוס שנראה שמאיץ או מאט את ההרס. באמצעות הבנה ושליטה על מתג זה, העבודה מצביעה על כיווני טיפול חדשים שעשויים להגן על המפרקים ולעכב או אפילו למנוע את הצורך בניתוח.
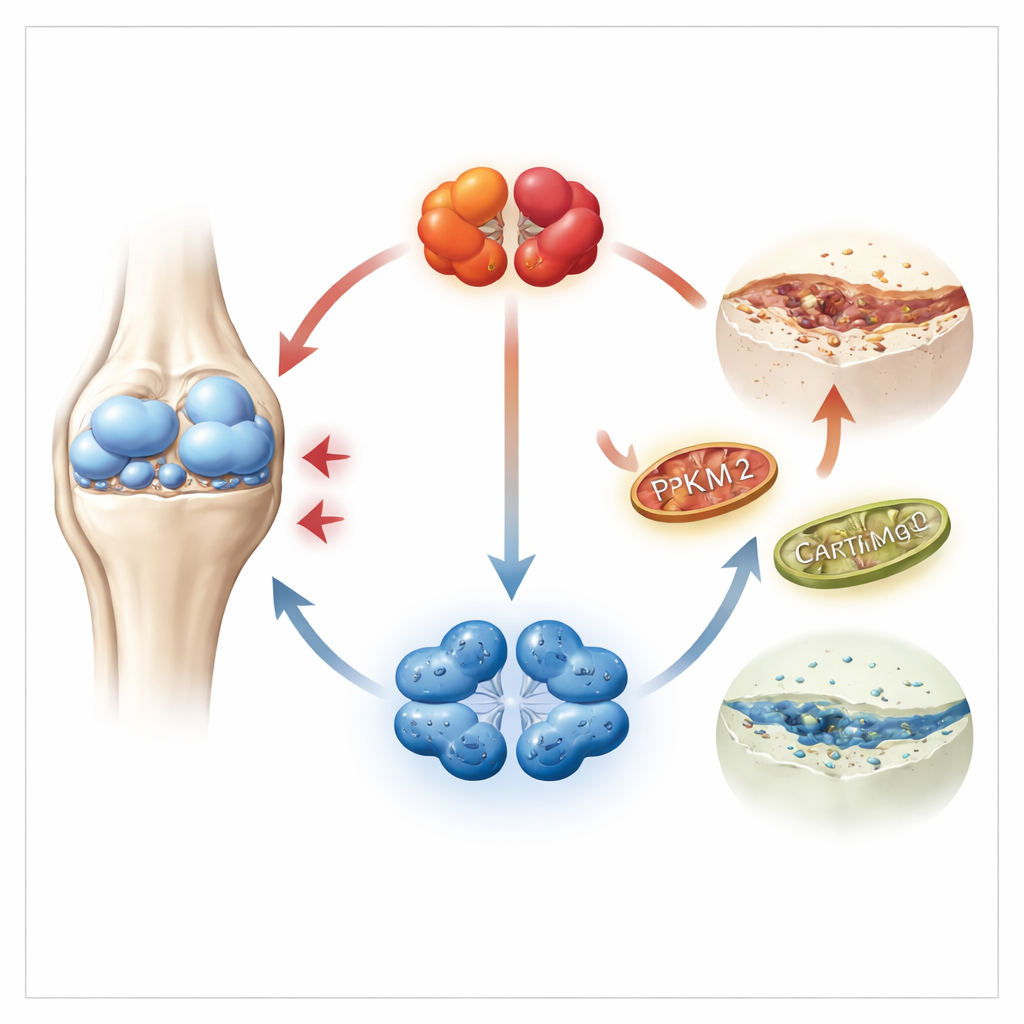
מבט מעמיק לתוך סחוס כואב
הסחוס נבנה ומתחזק על ידי כונדרוציטים, תאים מתמחים החיים בסביבה דלה בחמצן ותלויים בעיקר בשריפה של סוכרים כדי לייצר אנרגיה. החוקרים התמקדו באנזים מרכזי בתהליך הזה שנקרא PKM2, שיכול להימצא בשתי צורות: צורה צפופה בארבעה יחידות וצורה רפויה בשתי יחידות. באמצעות מאגרי נתונים גנטיים גדולים מסחוס אנושי, וכן דגימות מחולים ומעכברים, הם מצאו שרמות PKM2 עלו באופן משמעותי בסחוס אוסטאוארתריטי, בעוד שהצורה המקבילה PKM1 הייתה כמעט בלתי ניתנת לזיהוי. חשוב מזה, הסחוס החולה הראה שינוי לעבר גרסת ה‑dimer (שתי היחידות) של PKM2, שהיא ידועה יותר כבקרה של התנהגות תאית מאשר כייצור אנרגיה.
מעתיקים מעגל הרס להגנה
הצוות לאחר מכן בדק מה קורה אם מורידים את PKM2 או מקבעים אותו בצורתו בעלת ארבעת היחידות. בכונדרוציטים שגדלו במעבדה, הורדת רמות PKM2, או שימוש במולקולה קטנה בשם TEPP-46 שמנעת PKM2 בצורת הטטראמר, הטה את האיזון לבניית סחוס במקום לפרק אותו. התאים ייצרו יותר חלבוני מבנה המעניקים לסחוס את חוזקו ופחות אנזימים שמפרקים את הרקמה. במודל עכבר שבו האוסטאוארתריטיס הושרה על ידי ברך לא יציבה, הזרקות שהפחיתו PKM2 או ייצבו את צורתו בארבע יחידות שמרו על מבנה הסחוס, הורידו ציוני נזק ושיפרו דפוסי הליכה ותגובות הקשורות לכאב.
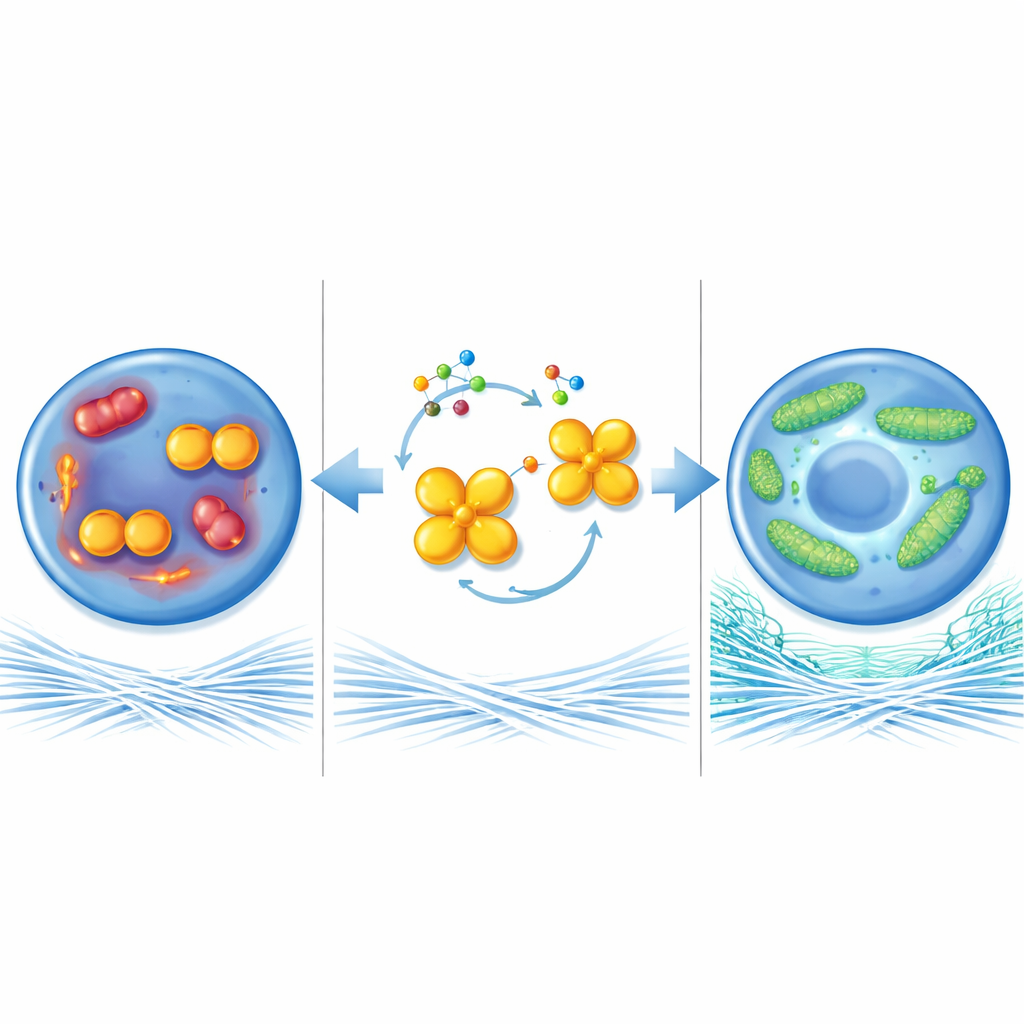
מגינים על תחנות הכוח של התא
כדי להבין כיצד אנזים זה משפיע על בריאות הסחוס, החוקרים בחנו את המיטוכונדריות — תחנות הכוח הזעירות שבתוך התאים. בתנאים דמויי אוסטאוארתריטיס, המיטוכונדריות בכונדרוציטים התקצרו והתפצלו, ייצרו יותר מולקולות תגובתיות מזיקות וייצרו פחות אנרגיה. כאשר PKM2 הוסר או נכפה לצורתו בארבע יחידות, המיטוכונדריות במקום זאת יצרו רשתות ארוכות ומחוברות, שרפו דלק ביעילות רבה יותר וייצרו יותר מולקולות עשירות באנרגיה. "מיזוג" מיטוכונדריאלי זה היה תלוי במידה רבה בחלבון אחר, MFN1, המסייע לקשר בין מיטוכונדריות. רמות MFN1 היו נמוכות בסחוס החולה אך עלו כאשר רמות דימר PKM2 ירדו. חסימת MFN1 במפרקים של עכברים חסרי PKM2 מחקה את ההשפעות המגנות ואיפשרה להתקדם בנזק לסחוס, מה שמצביע על כך ש‑MFN1 הוא שחקן מפתח במסלול הזה.
שבירת שרשרת האותות המזיקה
המחקר חשף גם שרשרת איתות שמחברת את PKM2 לשינויים מיטוכונדריאליים. PKM2 הצורה הרופפת, הדימרית, נטלה אינטראקציה פיזית עם ERK, חלבון איתות ידוע המגיב ללחץ ודלקת. תחת גירוי דמוי אוסטאוארתריטיס, אינטראקציה זו הוחזקה וה‑ERK הופעל יותר, מה שעקף את MFN1 ודחף את המיטוכונדריות למצב מפורק ולא בריא. הפחתת דימריזציה של PKM2 או קיבוע PKM2 בטטראמר החלישה את האינטראקציה הזו בין PKM2 ל‑ERK, הורידה את פעילות ERK והשיבה את רמות MFN1. באופן מעניין, חלבון מיזוג קרוב, MFN2, הושפע באופן שונה, מה שמרמז של‑MFN1 תפקיד ייחודי ולא חלופי בשמירה על איזון הכונדרוציטים והמיטוכונדריות שלהם.
מה משמעות הדבר לטיפול עתידי במפרקים
פשוטו כמשמעו, העבודה מראה שכאשר PKM2 מצטבר בצורה של דימר בתוך תאי סחוס, הוא מערער את מערכות הכוח של התא, מחליש את המנגנון הבונה את הסחוס ומאיץ את האוסטאוארתריטיס. הזזת PKM2 לעבר צורתו החרטומית של ארבע יחידות, או הפחתת הגרסה הדימרית בכל דרך אחרת, מסייעת לשמור על המיטוכונדריות בריאות ומעודדת תיקון סחוס. בעכברים, אסטרטגיה זו לא רק שמרה על רקמת המפרק אלא גם הקלה על התנהגויות הקשורות לכאב. בעוד שדרוש מחקר נוסף לפני שגישות כאלה יגיעו לקליניקה, מיקוד בדימריזציה של PKM2 מציע דרך מבטיחה להאט או למנוע שחיקה של מפרקים, ולתת למטופלים שנים נוספות של תנועה נוחה לפני שתידרש ניתוחית החלפה.
ציטוט: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
מילות מפתח: אוסטאוארתריטיס, סחוס, מיטוכונדריה, PKM2, מיטופוזין 1