Clear Sky Science · it
PKM2 dimerico nei condrociti compromette l'omeostasi mitocondriale nell'osteoartrite
Perché le articolazioni usurate contano
Molte persone convivono con il dolore e la rigidità dell'osteoartrite, una comune malattia articolare che gradualmente consuma la liscia cartilagine che ammortizza le ossa. Quando questa cartilagine è gravemente danneggiata, l'opzione principale è la sostituzione articolare. Questo studio esplora un interruttore energetico nascosto all'interno delle cellule della cartilagine che sembra accelerare o rallentare questo deterioramento. Capirne il funzionamento e saperlo modulare indica possibili nuovi trattamenti in grado di proteggere le articolazioni e ritardare o persino evitare la necessità dell'intervento chirurgico.
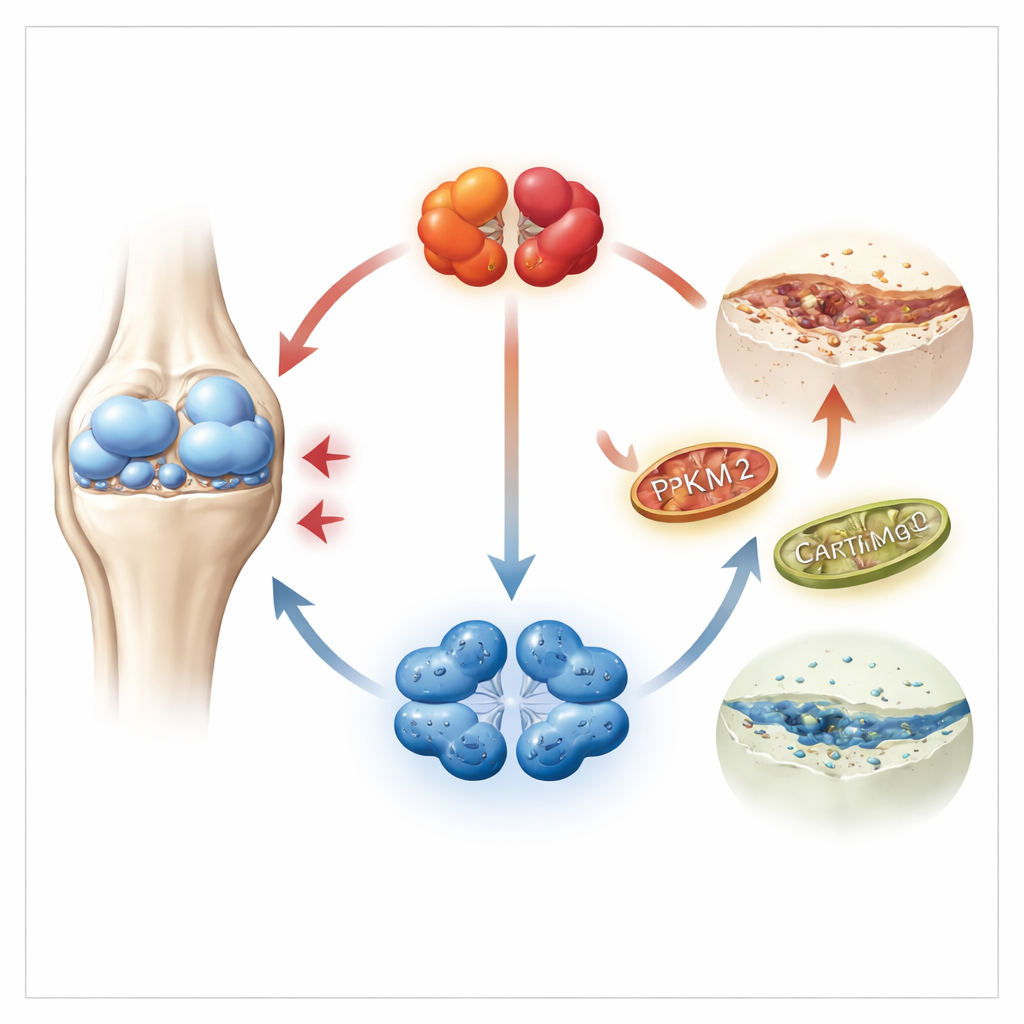
Uno sguardo più ravvicinato nella cartilagine dolorante
La cartilagine è costruita e mantenuta dai condrociti, cellule specializzate che vivono in un ambiente a basso contenuto di ossigeno e si affidano in gran parte alla glicolisi per ottenere energia. I ricercatori si sono concentrati su un enzima chiave in questo processo chiamato PKM2, che può esistere in due conformazioni: una forma tetramerica compatta e una forma dimerica più lassa. Utilizzando ampi dataset genetici di cartilagine umana, oltre a campioni di pazienti e di topi, hanno riscontrato che i livelli di PKM2 erano fortemente aumentati nella cartilagine osteoartritica, mentre la forma correlata PKM1 era quasi assente. In modo importante, la cartilagine malata mostrava uno spostamento verso la versione dimerica di PKM2, nota più per il suo ruolo nella regolazione del comportamento cellulare che per la produzione di energia.
Trasformare un ciclo distruttivo in uno protettivo
Il team ha poi esaminato cosa succede quando PKM2 viene ridotto o mantenuto nella sua forma tetramerica. In condrociti coltivati in laboratorio, abbassare i livelli di PKM2, oppure usare una piccola molecola chiamata TEPP-46 che blocca PKM2 nello stato tetramerico, spostava l'equilibrio verso la costruzione della cartilagine anziché la sua degradazione. Le cellule producevano più proteine strutturali che conferiscono resistenza alla cartilagine e meno enzimi che degradano il tessuto. In un modello murino in cui l'osteoartrite è indotta da un ginocchio instabile, iniezioni che riducevano PKM2 o stabilizzavano la forma tetramerica preservavano la struttura cartilaginea, abbassavano i punteggi di danno e miglioravano i modelli di deambulazione e le risposte correlate al dolore.
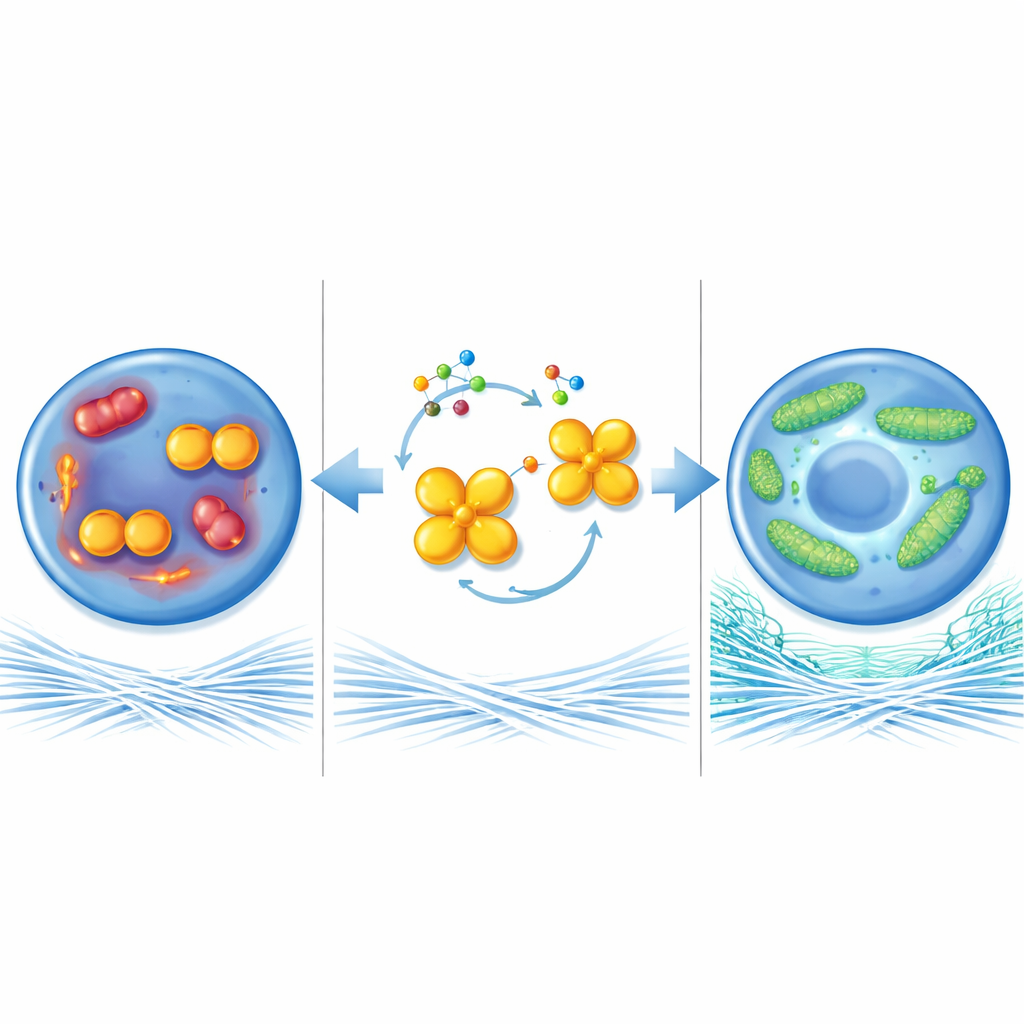
Proteggere le centrali energetiche della cellula
Per capire come questo enzima influenzi la salute della cartilagine, i ricercatori hanno esaminato i mitocondri, le piccole centrali energetiche all'interno delle cellule. In condizioni simili all'osteoartrite, i mitocondri dei condrociti diventavano piccoli e frammentati, producevano più specie reattive dannose e generavano meno energia. Quando PKM2 veniva rimosso o forzato nella sua forma tetramerica, i mitocondri invece formavano lunghe reti connesse, bruciavano il combustibile in modo più efficiente e producevano più molecole ricche di energia. Questa «fusione» mitocondriale dipendeva in larga parte da un'altra proteina, MFN1, che aiuta a collegare i mitocondri tra loro. I livelli di MFN1 erano bassi nella cartilagine malata ma aumentavano quando i livelli di dimeri di PKM2 calavano. Bloccare MFN1 nelle articolazioni di topi privi di PKM2 annullava gli effetti protettivi e permetteva la progressione del danno cartilagineo, dimostrando che MFN1 è un elemento chiave di questa via.
Interrompere la catena di segnalazione dannosa
Lo studio ha poi scoperto una catena di segnalazione che collega PKM2 ai cambiamenti mitocondriali. La forma dimerica di PKM2 interagiva fisicamente con ERK, una nota proteina di segnalazione che risponde a stress e infiammazione. Sotto stimoli simili all'osteoartrite, questa interazione si rafforzava ed ERK diventava più attivo, il che a sua volta sopprimeva MFN1 e spingeva i mitocondri verso uno stato frammentato e malsano. Ridurre la dimerizzazione di PKM2 o bloccare PKM2 in tetrameri indeboliva l'interazione PKM2–ERK, diminuiva l'attività di ERK e ripristinava i livelli di MFN1. È interessante che una proteina di fusione correlata, MFN2, fosse influenzata in modo differente, suggerendo che MFN1 ha un ruolo unico e non ridondante nel mantenere l'equilibrio dei condrociti e dei loro mitocondri.
Cosa significa per la cura delle articolazioni in futuro
In termini semplici, il lavoro mostra che quando PKM2 si accumula nella sua forma dimerica all'interno dei condrociti, disturba i sistemi energetici della cellula, indebolisce i meccanismi di costruzione della cartilagine e accelera l'osteoartrite. Spostare PKM2 verso la sua forma tetramerica, o comunque ridurre la versione dimerica, aiuta i mitocondri a restare sani e favorisce la riparazione della cartilagine. Nei topi, questa strategia non solo ha preservato il tessuto articolare ma ha anche alleviato i comportamenti correlati al dolore. Sebbene siano necessarie ulteriori ricerche prima che tali approcci possano arrivare in clinica, mirare alla dimerizzazione di PKM2 rappresenta una nuova e promettente via per rallentare o prevenire l'usura articolare, potenzialmente offrendo ai pazienti più anni di movimento confortevole prima che l'intervento chirurgico diventi necessario.
Citazione: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
Parole chiave: osteoartrite, cartilagine, mitocondri, PKM2, mitofusina 1