Clear Sky Science · sv
Dimerisk PKM2 i kondrocyter försämrar mitokondriell homeostas vid artros
Varför utslitna leder är viktiga
Många lever med smärta och stelhet från artros, en vanlig ledsjukdom som gradvis nöter bort det släta brosk som dämpar våra ben. När detta brosk är kraftigt skadat är det huvudsakliga alternativet ofta ledprotesoperation. Denna studie undersöker en dold energiknapp inne i broskceller som verkar kunna påskynda eller bromsa denna skada. Genom att förstå och kontrollera denna brytare pekar arbetet mot nya behandlingar som kan skydda leder och fördröja eller till och med undvika behovet av operation.
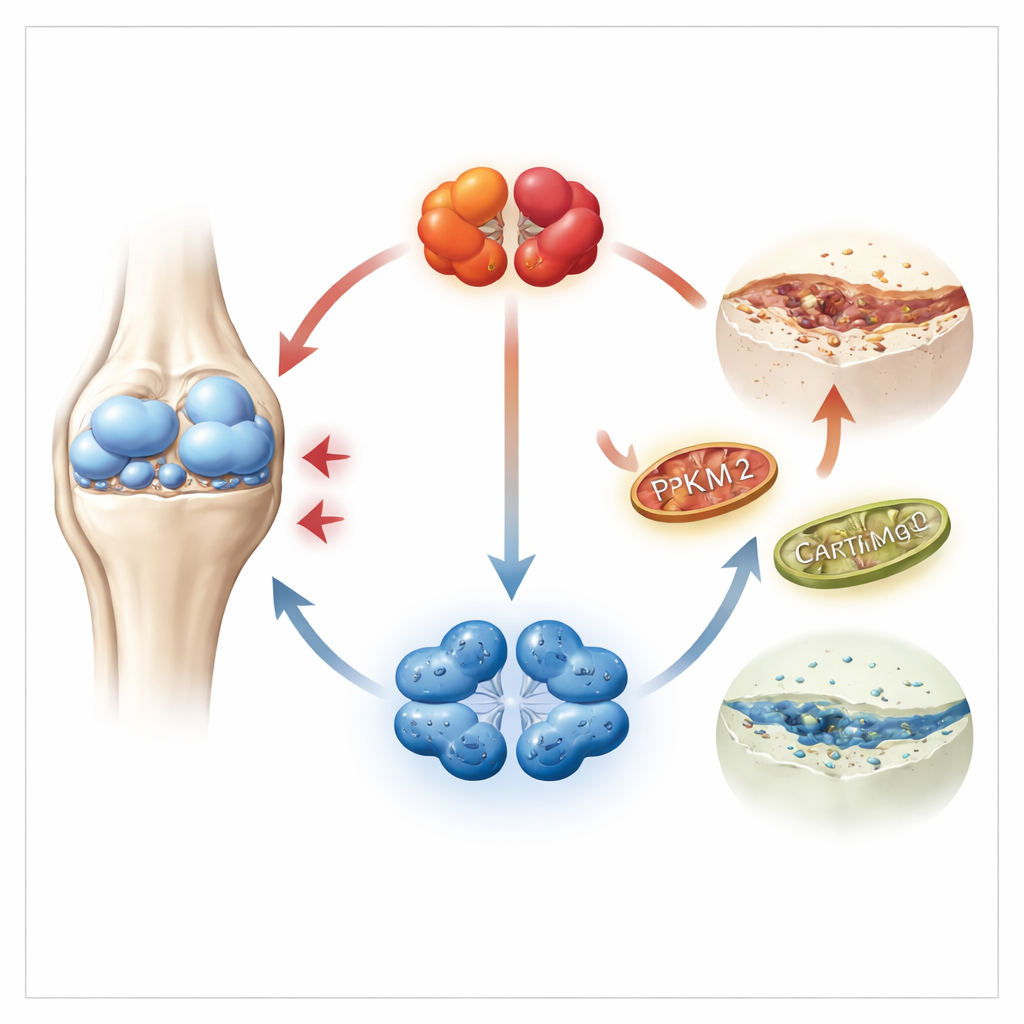
Närmare in i det värkande brosket
Brosk byggs upp och underhålls av kondrocyter, specialiserade celler som lever i en låg-oxygenmiljö och främst förlitar sig på glykolys för energi. Forskarna fokuserade på ett nyckelenzym i denna process kallat PKM2, som kan förekomma i två former: en tätt packad fyrdelad form och en lösare tvådelad form. Genom att använda stora genetiska dataset från mänskligt brosk, samt prover från patienter och möss, fann de att PKM2-nivåerna var kraftigt ökade i artrotiskt brosk, medan systerformen PKM1 var nästintill obefintlig. Viktigt var att sjukt brosk visade en förskjutning mot den tvådelade (dimer) versionen av PKM2, som mer är känd för att kontrollera cellbeteende än för att producera energi.
Att vända en destruktiv cykel till en skyddande
Teamet undersökte sedan vad som händer om PKM2 minskas eller hålls i sin fyrdelade form. I broskceller odlade i labbet ledde sänkta nivåer av PKM2, eller användning av ett litet molekylärt ämne kallat TEPP-46 som låser PKM2 i dess fyrdelade tillstånd, till en förskjutning mot uppbyggnad av brosk snarare än nedbrytning. Cellerna producerade mer av de strukturella proteiner som ger brosket dess styrka och färre av de enzymer som bryter ner vävnaden. I en musemodell där artros utlöses av en instabil knäled bevarade injektioner som minskade PKM2 eller stabiliserade dess fyrdelade form broskets struktur, sänkte skadescorer och förbättrade gångmönster och smärtrelaterade responser.
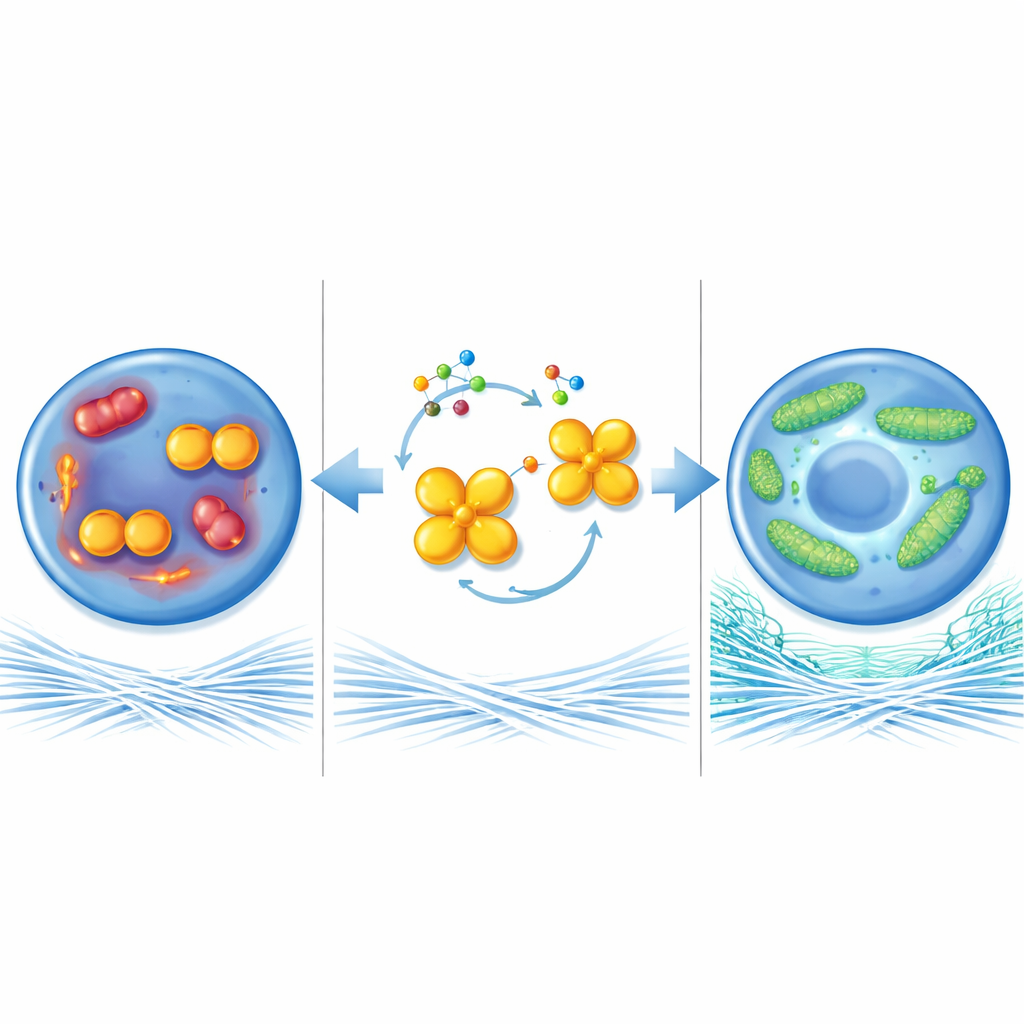
Skydda cellernas kraftstationer
För att förstå hur detta enzym påverkar broskets hälsa undersökte forskarna mitokondrierna, de små kraftstationerna inne i cellerna. Under artroslika förhållanden blev mitokondrierna i kondrocyterna små och fragmenterade, producerade fler skadliga reaktiva molekyler och genererade mindre energi. När PKM2 togs bort eller tvingades in i sin fyrdelade form bildade mitokondrierna istället långa, förgrenade nätverk, förbrände bränsle mer effektivt och skapade fler energirika molekyler. Denna mitokondriella "fusion" berodde till stor del på ett annat protein, MFN1, som hjälper till att länka mitokondrier ihop. MFN1-nivåerna var låga i sjukt brosk men ökade när PKM2-dimernivåerna sjönk. Att blockera MFN1 i lederna hos PKM2-defekta möss raderade de skyddande effekterna och tillät brosksskada att fortskrida, vilket visar att MFN1 är en nyckelspelare i denna väg.
Bryta den skadliga signalskedjan
Studien avslöjade vidare en signalskedja som länkar PKM2 till mitokondriella förändringar. Den lösa, tvådelade PKM2 interagerade fysiskt med ERK, ett välkänt signalprotein som svarar på stress och inflammation. Under artroslika stimuleringar blev denna interaktion starkare och ERK blev mer aktiv, vilket i sin tur undertryckte MFN1 och pressade mitokondrierna mot ett fragmenterat, ohälsosamt tillstånd. Att minska PKM2-dimerisering eller låsa PKM2 i tetramerer försvagade denna PKM2–ERK-interaktion, minskade ERK-aktiviteten och återställde MFN1-nivåerna. Intressant nog påverkades det relaterade fusionsproteinet MFN2 på ett annat sätt, vilket tyder på att MFN1 har en unik, icke-ersättningsbar roll i att bibehålla balans i kondrocyter och deras mitokondrier.
Vad detta betyder för framtida ledvård
Enkelt uttryckt visar arbetet att när PKM2 ackumuleras i sin tvådelade form inne i broskceller störs cellens energisystem, broskets uppbyggande maskineri försvagas och artrosen framskrider snabbare. Att förskjuta PKM2 mot dess fyrdelade form, eller på annat sätt minska den tvådelade versionen, hjälper mitokondrierna att förbli friska och främjar broskreparation. Hos möss bevarade denna strategi inte bara ledvävnad utan lindrade också smärtrelaterat beteende. Även om mer forskning behövs innan sådana angreppssätt når kliniken, erbjuder riktning mot PKM2-dimerisering ett lovande nytt sätt att bromsa eller förebygga ledslitage och kan potentiellt ge patienter fler år av bekväm rörelse innan operation blir nödvändig.
Citering: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
Nyckelord: artros, brosk, mitokondrier, PKM2, mitofusin 1