Clear Sky Science · ar
PKM2 ثنائي الوحدات في الخلايا الغضروفية يخل بتوازن الميتوكوندريا في هشاشة العظام
لماذا تهم المفاصل المتآكلة
يعاني الكثيرون من ألم وتصلب ناجمين عن هشاشة العظام، وهو مرض مفصلي شائع ينهش تدريجياً الغضروف الأملس الذي يوسّط بين عظامنا. عندما يتضرر هذا الغضروف بشدة، يصبح الخيار الرئيسي هو جراحة استبدال المفصل. تستكشف هذه الدراسة مفتاح طاقة خفي داخل خلايا الغضروف يبدو أنه يسرع أو يبطئ هذا التلف. من خلال فهم هذا المفتاح والسيطرة عليه، يشير العمل إلى علاجات جديدة قد تحمي المفاصل وتؤخر أو تمنع الحاجة للجراحة.
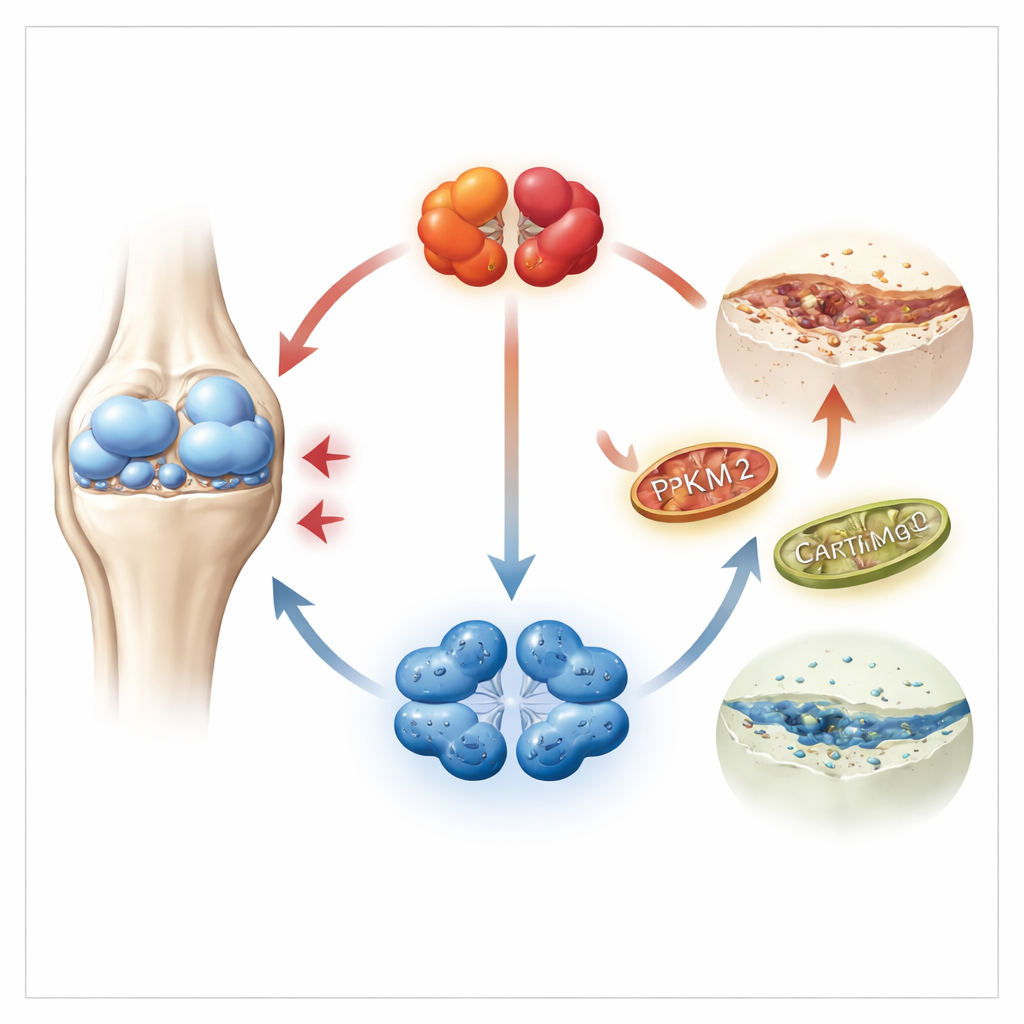
نظرة أقرب داخل الغضروف المتألم
يبني الغضروف ويحافظ عليه الخلايا الغضروفية (الخلايا الغضروفية)، وهي خلايا متخصصة تعيش في بيئة منخفضة الأكسجين وتعتمد غالباً على حرق السكر للحصول على الطاقة. ركز الباحثون على إنزيم رئيسي في هذه العملية يُدعى PKM2، الذي يمكن أن يوجد في شكلين: شكل رباعي متماسك وشكل ثنائي أكثر رخاوة. باستخدام مجموعات بيانات جينية كبيرة من غضروف الإنسان، بالإضافة إلى عينات من مرضى وفئران، وجدوا أن مستويات PKM2 ارتفعت بشدة في الغضروف المصاب بهشاشة العظام، في حين أن أشقُّه PKM1 كان بالكاد قابلاً للكشف. والأهم أن الغضروف المريض أظهر تحوّلاً نحو النسخة ثنائية الوحدات من PKM2، المعروفة أكثر بتنظيم سلوك الخلايا منها بصنع الطاقة.
تحويل حلقة مدمرة إلى حل وقائي
سأل الفريق بعد ذلك ماذا يحدث إذا خُفِّضت مستويات PKM2 أو أُبقيت في شكلها الرباعي. في خلايا الغضروف المزروعة في المختبر، أدى خفض PKM2، أو استخدام جزيء صغير يدعى TEPP-46 الذي يثبت PKM2 في شكله الرباعي، إلى ميل التوازن نحو بناء الغضروف بدلاً من تكسيره. أنتجت الخلايا مزيداً من البروتينات البنائية التي تمنح الغضروف قوته، وأنتجت عدداً أقل من الإنزيمات التي تهدم النسيج. في نموذج فأري حيث تُثار هشاشة العظام بواسطة ركبة غير مستقرة، أدت الحقن التي خفّضت PKM2 أو ثبّتت شكله الرباعي إلى الحفاظ على بنية الغضروف، وخفضت درجات التلف، وحسّنت أنماط المشي والاستجابات المرتبطة بالألم.
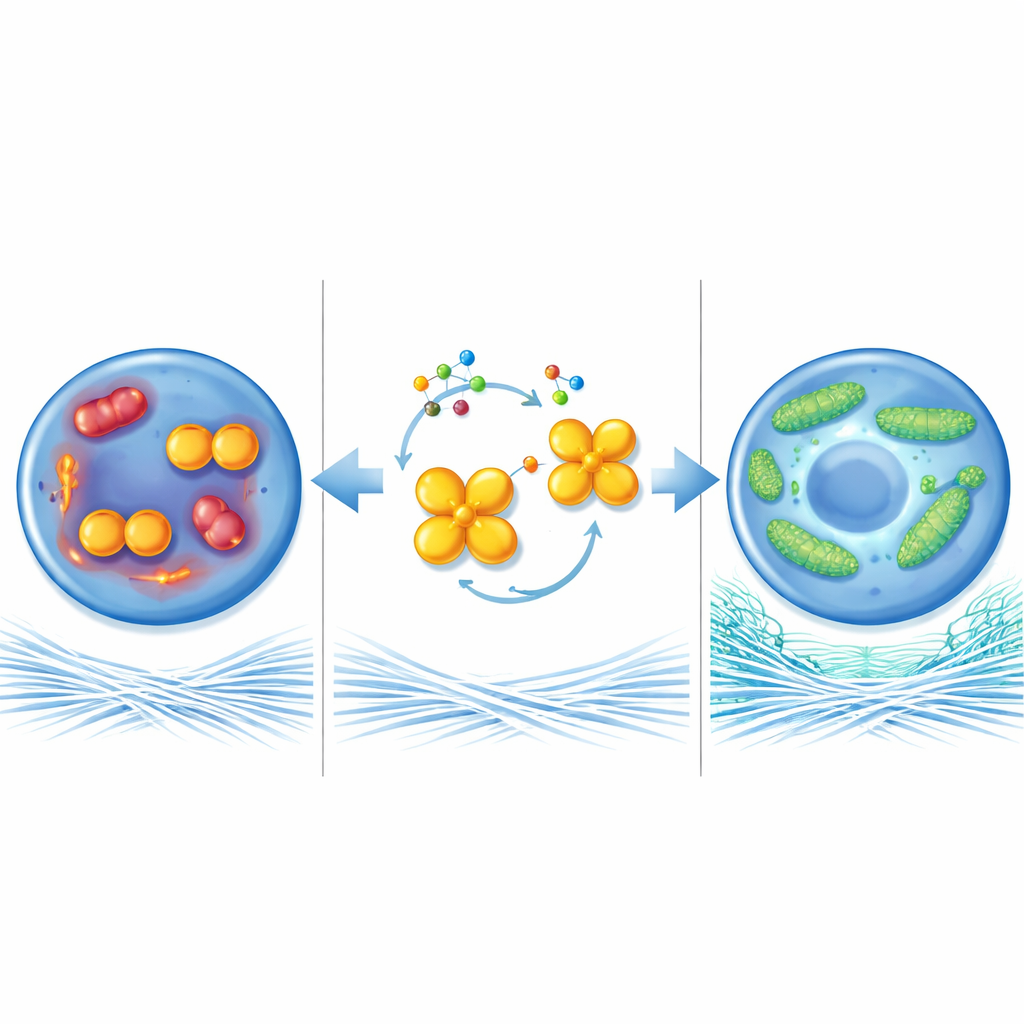
حماية محطات طاقة الخلية
لفهم كيف يؤثر هذا الإنزيم في صحة الغضروف، نظر الباحثون إلى الميتوكوندريا، محطات الطاقة الصغيرة داخل الخلايا. في ظروف شبيهة بهشاشة العظام، أصبحت الميتوكوندريا في الخلايا الغضروفية صغيرة ومجزأة، أنتجت المزيد من الجزيئات التفاعلية الضارة، وولّدت طاقة أقل. عندما أزيل PKM2 أو أُجبر على شكله الرباعي، كوّنت الميتوكوندريا بدلاً من ذلك شبكات طويلة ومرتبطة، أحرق الوقود بكفاءة أكبر، وأنتج مزيداً من الجزيئات الغنية بالطاقة. اعتمد هذا الاندماج الميتوكوندري إلى حد كبير على بروتين آخر هو MFN1، الذي يساعد على ربط الميتوكوندريا معاً. كانت مستويات MFN1 منخفضة في الغضروف المريض لكنها ارتفعت عندما انخفضت مستويات ثنائي PKM2. أدى تعطيل MFN1 في مفاصل الفئران الناقصة PKM2 إلى مسح التأثيرات الوقائية وسمح بتقدّم تلف الغضروف، مما يبيّن أن MFN1 لاعب رئيسي في هذا المسار.
كسر سلسلة الإشارات الضارة
كشفت الدراسة أيضاً عن سلسلة إشارية تربط PKM2 بالتغيرات الميتوكوندرية. تفاعل PKM2 الفضفاض ثنائي الوحدات جسدياً مع ERK، بروتين إشارتي معروف يستجيب للضغط والالتهاب. تحت التحفيز الشبيه بهشاشة العظام، أصبحت هذه التفاعلات أقوى ونشطت ERK أكثر، مما قمع MFN1 ودفع الميتوكوندريا إلى حالة مجزأة وغير صحية. أدى تقليل ثنائيات PKM2 أو قفل PKM2 في حالة الرباعيات إلى إضعاف تفاعل PKM2–ERK، وخفض نشاط ERK، واستعادة مستويات MFN1. ومن المثير للاهتمام أن بروتين اندماج ذي صلة، MFN2، تأثر بطريقة مختلفة، ما يشير إلى أن MFN1 له دور فريد وغير قابل للاستبدال في الحفاظ على توازن خلايا الغضروف وميتوكوندرياتها.
ماذا يعني هذا لرعاية المفاصل المستقبلية
ببساطة، يوضح هذا العمل أنه عندما يتراكم PKM2 في شكله ثنائي الوحدات داخل خلايا الغضروف، يخل هذا بأنظمة طاقة الخلية، ويضعف آليات بناء الغضروف، ويسرع هشاشة العظام. إن تحويل PKM2 نحو شكله الرباعي، أو خفض النسخة ثنائية الوحدات بطرق أخرى، يساعد الميتوكوندريا على البقاء صحية ويشجع إصلاح الغضروف. في الفئران، لم تحفظ هذه الاستراتيجية نسيج المفصل فحسب، بل خففت أيضاً سلوكيات مرتبطة بالألم. ورغم الحاجة لمزيد من البحث قبل أن تصل هذه المقاربات إلى العيادات، فإن استهداف ثنائيات PKM2 يقدم طريقة واعدة لإبطاء أو منع تآكل المفصل، مما قد يمنح المرضى سنوات إضافية من الحركة المريحة قبل أن تصبح الجراحة ضرورية.
الاستشهاد: Liu, B., Liang, Y., Wang, C. et al. Dimeric PKM2 in chondrocytes impairs mitochondrial homeostasis in osteoarthritis. Cell Death Dis 17, 370 (2026). https://doi.org/10.1038/s41419-026-08621-4
الكلمات المفتاحية: هشاشة العظام, الغضروف, الميتوكوندريا, PKM2, ميتوفيوزين 1