Clear Sky Science · zh
在皮质-纹状体突触处的亨廷顿蛋白及其伙伴
为何这种脑蛋白很重要
亨廷顿病最为人所知的是导致抽动样动作和记忆问题,但其核心是一种脑细胞之间通讯受损的疾病。本文探讨了单一蛋白质——亨廷顿蛋白及其在神经细胞连接处的众多“盟友”——如何维持脑回路的正常运行,以及该蛋白发生改变如何破坏这些回路,特别是在连接思维与运动的关键通路上。理解这张隐秘的线路图为减缓或预防该病提供了新的思路。
连接思维与运动的大脑交通枢纽
作者关注两大脑区之间的联系:负责思考的外层(皮质)与帮助控制动作和习惯的深层结构(纹状体)。皮质神经元将长长的轴突投向纹状体,在那里形成成千上万个微小接触点——突触。皮质-纹状体突触是亨廷顿病中最先出现功能衰退的结构之一,远早于多数神经元的死亡。脑成像与动物研究表明,当这一路径变弱时,症状会加重。综述认为,问题不仅出现在接受信息的纹状体细胞(如早期认为的那样),也出现在发送信息的皮质端,后者可能在很大程度上推动了损伤的发生。
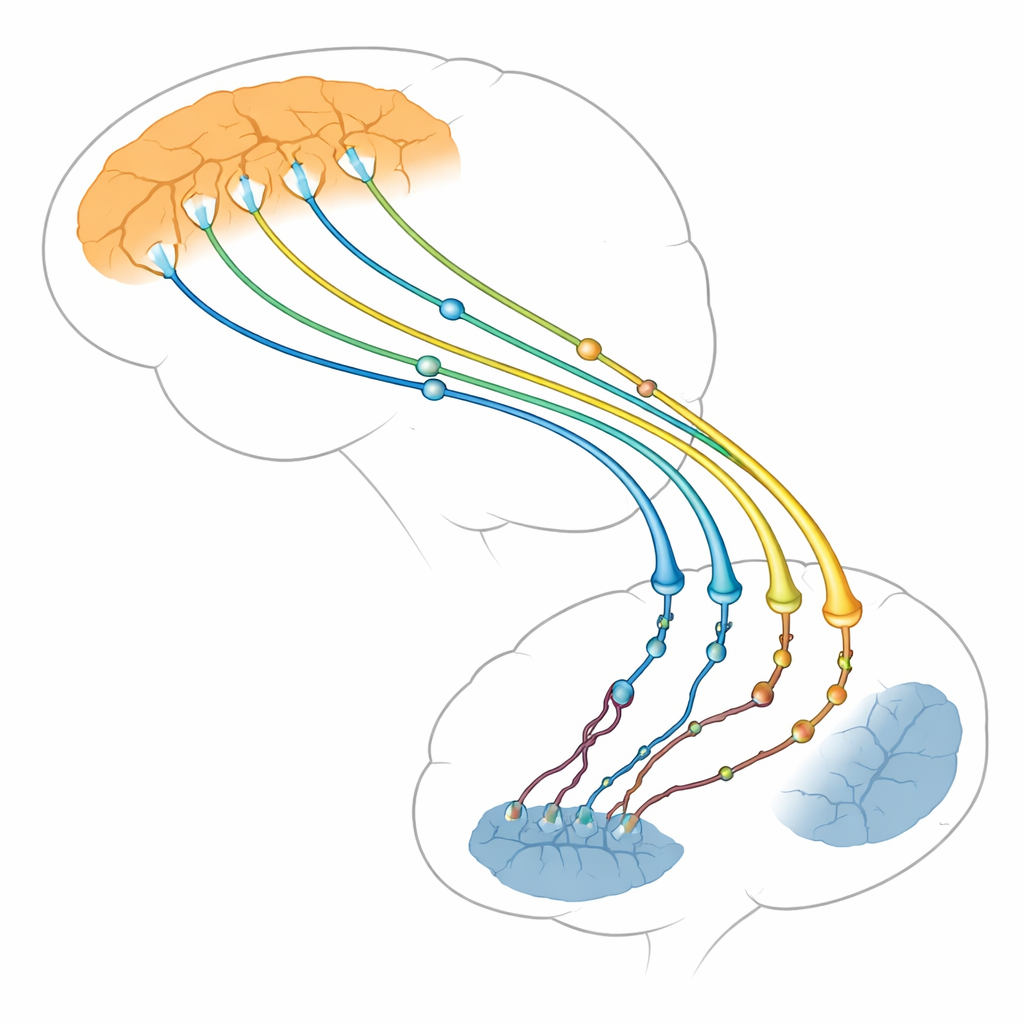
作为神经末梢主控者的亨廷顿蛋白
亨廷顿蛋白是一种分布于整个神经元的大分子,但在突触处尤为丰富,它像支架或停靠站一样与3000多种伙伴蛋白相互作用。在突触的发送侧,它帮助沿着内部轨道运输货物——例如产生能量的线粒体、装有神经递质的小泡,以及被称为BDNF的生长因子囊泡——到达神经末梢。它还协助将囊泡定位以便释放,促成囊泡与膜的融合以排放内容物,并回拉膜以回收新囊泡。文章展示了亨廷顿蛋白通过HAP1、HIP1等适配子以及像Rab这样的分子开关如何协调这类持续的运输,使神经元能够快速且可靠地传递信号。
突变亨廷顿蛋白如何造成堵塞
在亨廷顿病中,亨廷顿蛋白上额外延长的一段谷氨酰胺序列会微妙改变其构象与结合偏好。该突变形式对某些伙伴结合得过紧,对另一些则结合不足。因此,线粒体发生断裂并滞留在细胞体而无法到达末梢,BDNF囊泡行进速度变慢且方向错误,囊泡无法得到适当填充、停靠或回收。关键的辅助蛋白可能被困在富含亨廷顿蛋白的聚集体中,而应负责清除受损成分的细胞自噬——一种专门的细胞自噬清理机制——其效率也降低。随着时间推移,皮质-纹状体突触的发送端会因能量、生长支持和新囊泡的短缺而被耗竭,导致信号减弱并最终断连。
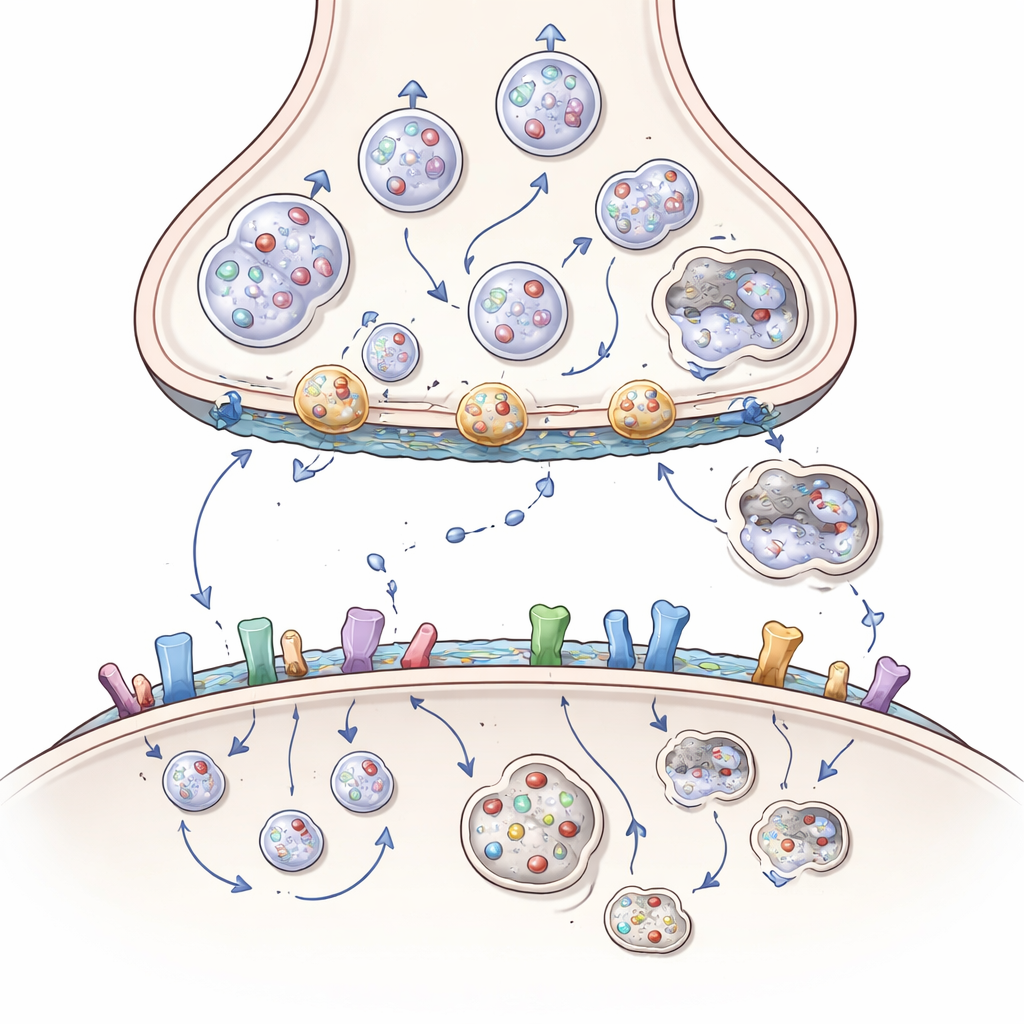
信号接收、黏着性与脂质的作用
损伤并不限于发送端。在接收端,亨廷顿蛋白帮助控制兴奋性和抑制性递质受体在细胞表面的数量、它们如何聚集以及回收速度。通过与支架蛋白及连接脂肪尾的酶合作,亨廷顿蛋白通常将某些谷氨酸受体维持在有保护性的突触位置,并抑制那些更具危害性的突触外受体。突变亨廷顿蛋白打破了这种平衡,使受体偏向有利于有毒钙内流和细胞死亡的位置与组合。它也干扰维持突触黏合的细胞黏附分子,以及塑造膜并支持信号传递的大脑脂质,如胆固醇和神经节苷脂。在亨廷顿病中这些脂质的流失进一步削弱了突触和生长因子信号。
治疗的新思路
综述总结认为,亨廷顿蛋白并非突变的被动受害者,而是突触的积极组织者,其伙伴关系在疾病中走向失衡。由于其许多关键盟友位于易受损的皮质神经元的突触前侧,针对这些伙伴——如运输适配子、生长因子载体、像ADAM10这样的关键酶或脂质通路——可能提供在不必完全清除亨廷顿蛋白的情况下保护皮质-纹状体突触的新途径。未来超分辨成像、“脑在芯片”模型以及对亨廷顿蛋白化学修饰的研究,可能揭示应在何处何时干预,从而带来保护大脑通讯线路并减缓亨廷顿病进展的希望。
引用: Zuccato, C., Scolz, A. & Iennaco, R. Huntingtin and its allies at the cortico-striatal synapse. Cell Death Dis 17, 412 (2026). https://doi.org/10.1038/s41419-026-08584-6
关键词: 亨廷顿病, 皮质-纹状体突触, 亨廷顿蛋白, 突触功能障碍, 轴突运输