Clear Sky Science · tr
Kortiko-striyatal sinaptikte huntingtin ve müttefikleri
Bu beyin proteini neden önemli
Huntington hastalığı tik benzeri ani hareketler ve hafıza sorunlarıyla tanınır, ancak özünde nöronlar arasındaki iletişimin bozulması hastalığın temelidir. Bu makale, tek bir protein olan huntingtinin ve sinapslardaki birçok “müttefikinin” beyin devrelerinin işlemesine nasıl yardımcı olduğunu—ve bu proteindeki değişikliklerin özellikle düşünce ile hareketi bağlayan önemli bir güzergâhta bu devreleri nasıl rayından çıkarabildiğini—inceliyor. Bu gizli bağlantıları anlamak, hastalığı yavaşlatma veya önleme için yeni fikirler sunuyor.
Düşünce ve hareket için beynin trafik merkezi
Yazarlar iki beyin bölgesi arasındaki bağlantıya odaklanıyor: düşünme işlevlerini üstlenen dış katman (korteks) ile eylem ve alışkanlıkları kontrollemeye yardımcı olan derin bir yapı (striatum). Korteksteki nöronlar uzun lifler göndererek striatuma ulaşır ve burada binlerce küçük temas noktası yani sinaps oluşturur. Bu kortiko-striyatal sinapslar, birçok beyin hücresi ölmeden çok önce Huntington hastalığında bozulan ilk yapılardan biridir. Beyin görüntülemeleri ve hayvan çalışmaları, bu yol zayıfladığında semptomların kötüleştiğini gösteriyor. Derleme, sorunların yalnızca alıcı striyatal hücrelerde değil—eski düşüncelerin aksine—gönderici kortikal tarafta da ortaya çıktığını ve büyük kısmı hasarın sürükleyicisi olabileceğini savunuyor.
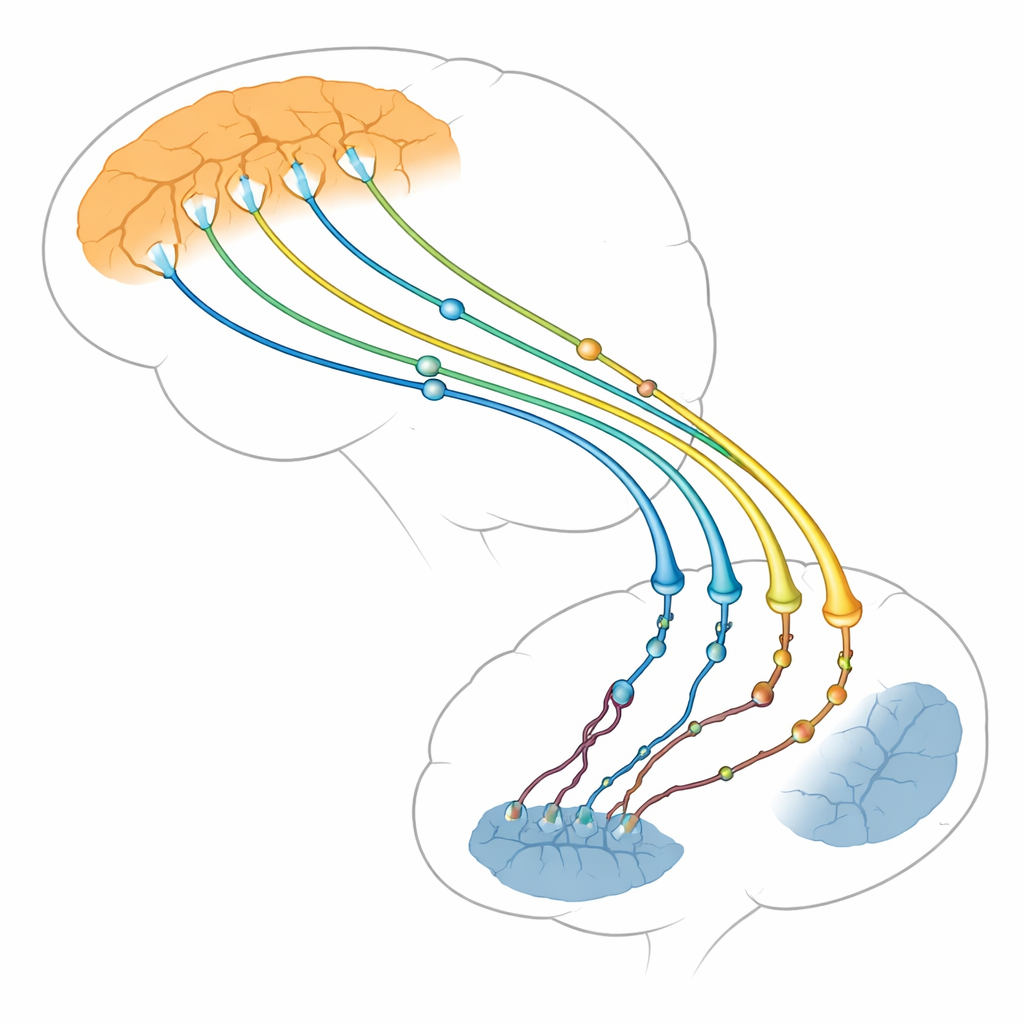
Nöron uçlarını organize eden ustabaşı olarak huntingtin
Huntingtin, nöronların tamamında bulunan büyük bir protein olup özellikle sinapslarda yoğunlaşır; burada iskele veya demirleme noktası gibi davranarak 3.000’den fazla partner proteini bir arada tutar. Sinapsın gönderici tarafında, enerji üreten mitokondriler, kimyasal dolu veziküller ve BDNF adı verilen büyüme faktörü paketleri gibi yükleri iç yollar boyunca sinir ucuna taşınmasına yardımcı olur. Ayrıca vezikülleri salıverme konumuna yerleştirmeye, içeriği boşaltmak için zarla kaynaştırmaya ve yeni veziküller oluşturmak üzere zarı geri çekmeye aracılık eder. Makale, HAP1 ve HIP1 gibi adaptörler ile Rab proteinleri gibi küçük anahtarlar aracılığıyla huntingtinin bu sürekli trafiği nasıl koordine ettiğini gösteriyor, böylece nöronlar hızlı ve güvenilir şekilde sinyal gönderebiliyor.
Mutant huntingtin işleyişi tıkadığında
Huntington hastalığında huntingtinde ekstra uzun bir glutamin dizisi onun şekil ve bağlanma tercihlerini ince bir şekilde değiştirir. Bu mutant form bazı partnerlere çok sıkı, bazılarına ise çok zayıf tutunur. Sonuç olarak mitokondriler parçalanır ve sinir uçlarına ulaşmak yerine hücre gövdesinde takılıp kalır, BDNF paketleri daha yavaş ve yanlış yönde hareket eder ve veziküller düzgün şekilde stoklanmaz, demetlenmez veya geri dönüştürülmez. Temel yardımcı proteinler huntingtin açısından zengin yumaklarda hapsedilebilir ve hasarlı bileşenleri uzaklaştırması gereken hücresel temizleme sistemi—otofaji olarak adlandırılan özel bir kendini yiyme mekanizması—daha az verimli çalışır. Zamanla kortiko-striyatal sinapsın gönderici tarafı enerji, büyüme desteği ve taze veziküllerden yoksun kalır; bu da sinyallerin zayıflamasına ve sonunda bağlantının kopmasına yol açar.
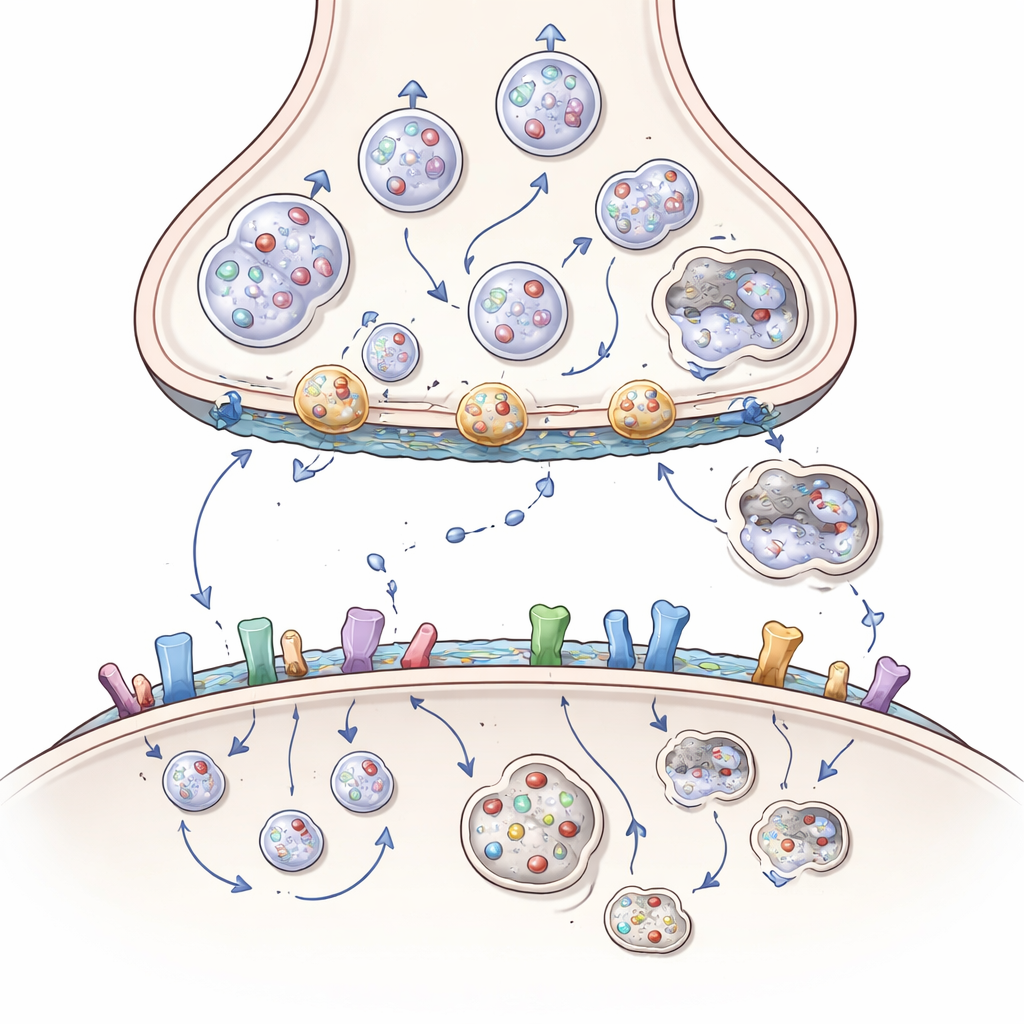
Sinyal alımı, yapışkanlık ve yağların rolü
Hasar yalnızca gönderici tarafla sınırlı değildir. Alıcı tarafta huntingtin, uyarıcı ve inhibitör haberci reseptörlerinin yüzeyde ne kadar bulunduğunu, nerede kümelendiklerini ve ne kadar hızlı geri dönüştürüldüklerini kontrol etmeye yardımcı olur. İskelet proteinleri ve yağlı kuyruk ekleyen enzimlerle iş birliği yaparak huntingtin normalde belirli glutamat reseptörlerini koruyucu sinaptik pozisyonlarda tutar ve daha zararlı, ekstrasinaptik olanları sınırlar. Mutant huntingtin bu dengeyi bozar ve reseptörleri toksik kalsiyum girişini ve hücre ölümünü kolaylaştıran konumlara ve kombinasyonlara iter. Ayrıca sinapsları bir arada tutan hücre-adezyon (yapışma) moleküllerini ve zarları şekillendirip sinyali destekleyen kolesterol ve gangliozidler gibi beyin lipidlerini etkiler. Huntington hastalığındaki bu lipid kaybı sinapsları ve büyüme faktörü sinyallemesini daha da zayıflatır.
Tedavi için yeni açı açıklaları
Derleme, huntingtinin yalnızca mutasyonun pasif bir kurbanı olmadığını, aynı zamanda hastalıkta ortaklıklarının bozulduğu aktif bir sinaps düzenleyicisi olduğunu sonuçlandırıyor. En kritik müttefiklerinin çoğu savunmasız kortikal nöronların presinaptik tarafında yer aldığından, taşıma adaptörleri, büyüme faktörü taşıyıcıları, ADAM10 gibi kilit enzimler veya lipid yolları gibi bu partnerleri hedeflemek, huntingtini tamamen ortadan kaldırmaya gerek kalmadan kortiko-striyatal sinapsları korumaya yönelik yeni yollar sunabilir. Süper çözünürlüklü görüntüleme, "beyin-çipte" modeller ve huntingtinin kimyasal değişikliklerinin incelenmesindeki ilerlemeler, müdahalenin tam olarak nerede ve ne zaman yapılacağını gösterebilir; bu da beynin iletişim hatlarını koruyan ve Huntington ilerleyişini yavaşlatan tedavilere dair umut veriyor.
Atıf: Zuccato, C., Scolz, A. & Iennaco, R. Huntingtin and its allies at the cortico-striatal synapse. Cell Death Dis 17, 412 (2026). https://doi.org/10.1038/s41419-026-08584-6
Anahtar kelimeler: Huntington hastalığı, kortiko-striyatal sinaps, huntingtin proteini, sinaptik disfonksiyon, aksonal taşınma