Clear Sky Science · ar
البروتين هنتنغتين وحلفاؤه عند المشبك القشري-المخطط
لماذا يهم هذا البروتين الدماغي
يشتهر مرض هنتنغتون بالتسبب في حركات متقطعة ومشكلات في الذاكرة، لكن جوهره مرض ناتج عن انهيار التواصل بين خلايا الدماغ. تستعرض هذه المقالة كيف يساعد بروتين واحد، الهنتنغتين، والعديد من «حلفائه» عند نقاط الاتصال بين الخلايا العصبية في الحفاظ على عمل الدوائر الدماغية — وكيف تؤدي تغيّرات في هذا البروتين إلى تعطيل تلك الدوائر، لا سيما على طول طريق رئيسي يربط التفكير بالحركة. يمكن أن يوفر فهم هذا السلك الخفي أفكارًا جديدة لكيفية إبطاء المرض أو الوقاية منه.
محور حركة الدماغ للتفكير والحركة
يركز المؤلفون على الاتصال بين منطقتين في الدماغ: الطبقة الخارجية المسؤولة عن التفكير (القشرة) وبنية عميقة تساعد في التحكم في الأفعال والعادات (المخطط). ترسل الخلايا العصبية في القشرة أليافًا طويلة إلى المخطط، حيث تُشكل آلاف النقاط الصغيرة للاتصال، أو المشابك. تُعد هذه المشابك القشرية-المخططية من بين أوائل التركيبات التي تتدهور في مرض هنتنغتون، قبل وقت طويل من موت كثير من الخلايا الدماغية. تُظهر صور الدماغ ودراسات الحيوانات أنه عندما تضعف هذه المسلكية تتفاقم الأعراض. وتؤكد المراجعة أن المشكلات لا تنشأ في خلايا المخطط المستقبلة فقط كما كان يُعتقد سابقًا، بل أيضًا في الجانب القشري المرسل، الذي قد يكون الدافع الأكبر للضرر.
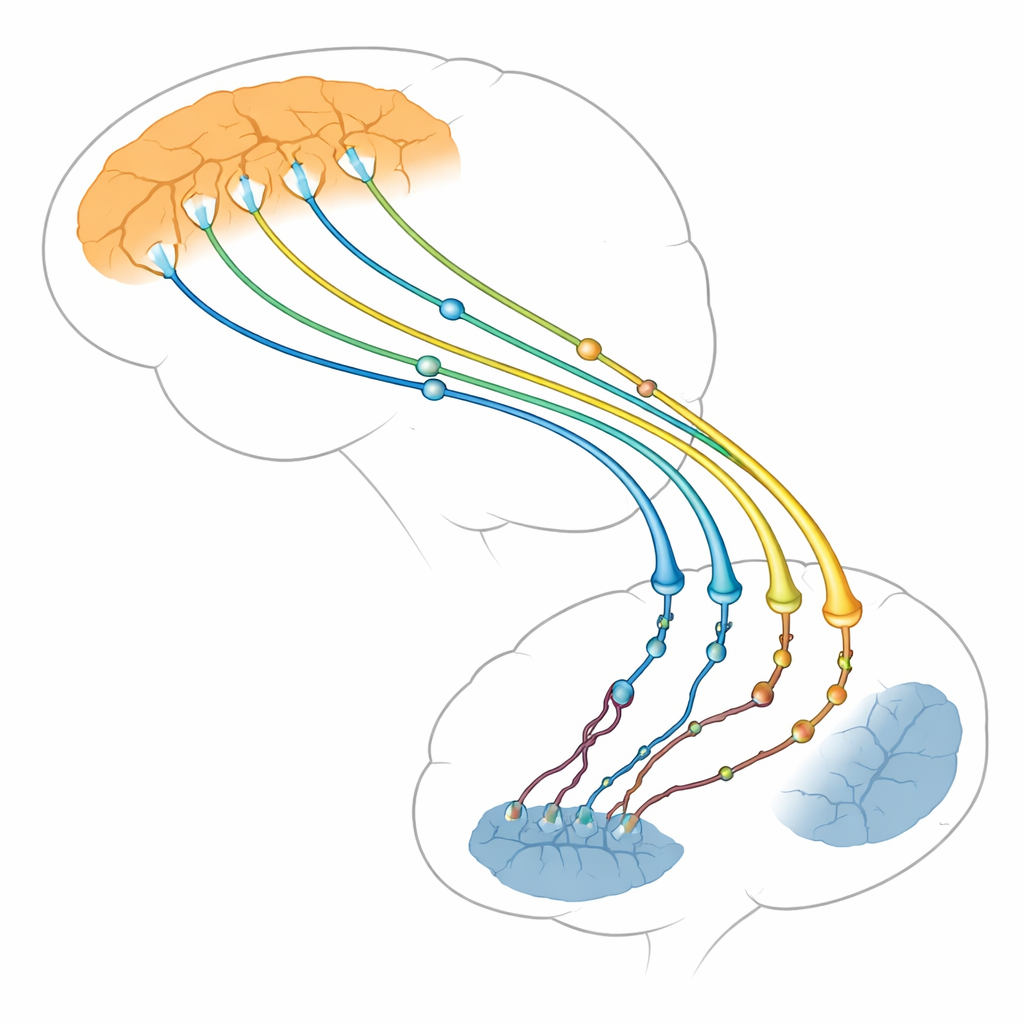
الهنتنغتين كمنظّم رئيسي لنهايات الأعصاب
الهنتنغتين بروتين كبير موجود في أنحاء الخلايا العصبية، لكنه يتركز بشكل خاص عند المشابك، حيث يعمل كهيكل داعم أو محطة ربط لأكثر من 3000 بروتين شريك. في جانب الإرسال من المشبك، يساعد على نقل الحمولة — مثل الميتوكوندريا المنتجة للطاقة، والحويصلات المحملة بالمواد الكيميائية، وحزم عوامل النمو مثل BDNF — على طول المسارات الداخلية إلى نهاية العصب. كما يساعد في وضع الحويصلات للإفراز، ودمجها مع الغشاء لإطلاق محتوياتها، وسحب الغشاء للخلف لإعادة تدوير حويصلات جديدة. توضح المقالة كيف ينسق الهنتنغتين، عبر محولات مثل HAP1 وHIP1 ومفاتيح صغيرة تسمى بروتينات Rab، هذه الحركة المستمرة حتى تستمر الخلايا العصبية في الإرسال بسرعة وموثوقية.
عندما يعرقل الهنتنغتين المتحوّر العمل
في مرض هنتنغتون، يغيّر امتداد طويل إضافي من وحدات الغلوتامين شكل الهنتنغتين وتفضيلات ارتباطه بشكل طفيف. هذا الشكل المتحوّر يلتصق بشدة ببعض الشركاء وبضعف مع آخرين. ونتيجة لذلك، تتفتت الميتوكوندريا وتتوقف في جسم الخلية بدلاً من الوصول إلى النهايات العصبية، وتسير حزم BDNF ببطء وبالاتجاه الخاطئ، ولا تُزوَّد الحويصلات أو تُثبّت أو تُعاد تدويرها بشكل صحيح. يمكن أن تصير البروتينات المساعدة الرئيسية محاصرة في تجمعات غنية بالهنتنغتين، ويعمل نظام التنظيف الذي يزيل المكونات التالفة — وهو شكل متخصّص من الهضم الذاتي الخلوي يسمى التحلل الذاتي (autophagy) — بكفاءة أقل. بمرور الوقت، يصبح جانب الإرسال في المشبك القشري-المخططي محرومًا من الطاقة والدعم النمائي والحويصلات الجديدة، مما يؤدي إلى تلاشي الإشارات وفصلها في نهاية المطاف.
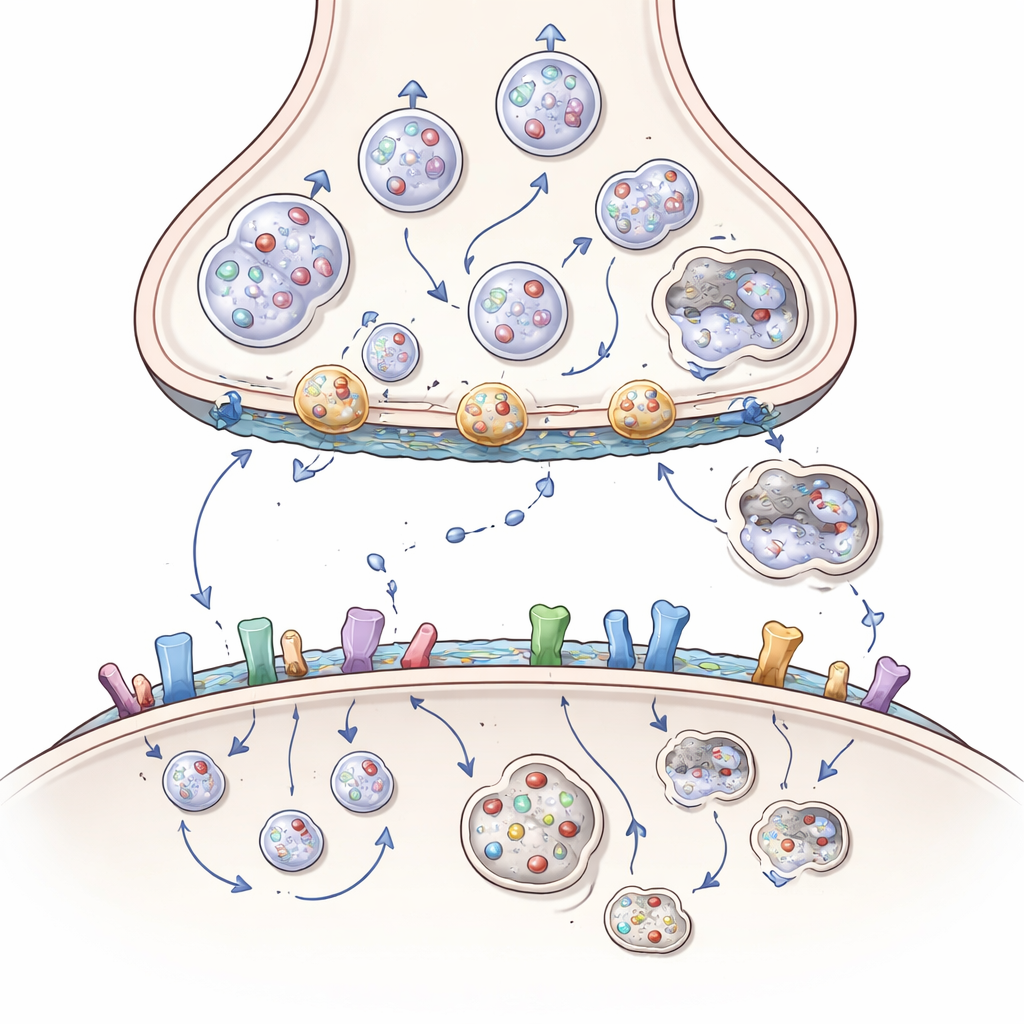
استقبال الإشارات والالتصاق ودور الدهون
لا يقتصر الضرر على جانب الإرسال. في الجانب المستقبل، يساعد الهنتنغتين على التحكم في عدد المستقبلات للناقلات المنبهة والمثبطة على السطح، وكيف تتجمع وأسرعية إعادة تدويرها. من خلال الشراكة مع بروتينات هيكلية وإنزيمات تذيّل الذنبيات الدهنية، يبقي الهنتنغتين عادةً مستقبلات معينة للغلوتامات في مواقع مشبكية حمائية ويقيد المستقبلات الأكثر ضررًا خارج المشبك. يخل الهنتنغتين المتحوّر بهذا التوازن، دافعًا المستقبلات إلى مواقع وتركيبات تُفضّل دخولًا سامًا للكالسيوم وموت الخلايا. كما يتداخل مع جزيئات التصاق الخلايا التي تُمسك المشابك معًا ومع دهون الدماغ مثل الكوليسترول والغانغليوسيدات التي تشكّل الأغشية وتدعم الإرسال. يؤدي فقدان هذه الدهون في مرض هنتنغتون إلى إضعاف المشابك وإشارة عوامل النمو أكثر.
زوايا جديدة للعلاج
تخلص المراجعة إلى أن الهنتنغتين ليس مجرد ضحية سلبية للطفرات بل منظّم نشط للمشابك تتعطل شراكاته في المرض. وبما أن كثيرًا من حلفائه الأكثر أهمية يجلسون على الجانب قبل المشبكي للخلايا القشرية الحساسة، فقد يوفر استهداف هؤلاء الشركاء — مثل محولات النقل، وحاملات عوامل النمو، والإنزيمات الرئيسية مثل ADAM10، أو مسارات الدهون — طرقًا جديدة لحماية المشابك القشرية-المخططية دون الحاجة إلى إزالة الهنتنغتين تمامًا. قد تكشف التقدّمات المستقبلية في التصوير فائق الدقة، ونماذج «الدماغ على رقاقة»، ودراسة التعديلات الكيميائية على الهنتنغتين المكان والوقت الأمثلين للتدخل، مما يثير الأمل في علاجات تحافظ على خطوط تواصل الدماغ وتبطئ تقدم هنتنغتون.
الاستشهاد: Zuccato, C., Scolz, A. & Iennaco, R. Huntingtin and its allies at the cortico-striatal synapse. Cell Death Dis 17, 412 (2026). https://doi.org/10.1038/s41419-026-08584-6
الكلمات المفتاحية: مرض هنتنغتون, المشبك القشري-المخطط, بروتين هنتنغتين, خلل في المشبكات, نقل محوري