Clear Sky Science · zh
SSTNIV,一种靶向syndecan-1的肽嵌合体,逆转免疫抑制并抑制多发性骨髓瘤进展
这项研究对患者为何重要
多发性骨髓瘤是一种骨髓细胞的癌症,常在治疗后复发,使患者的治疗选择越来越少。本研究提出了一种新型实验室设计的肽,称为SSTNIV,它从两个方面同时攻击癌症:直接损伤骨髓瘤细胞,并松解保护肿瘤的不良免疫环境。该研究在高级小鼠模型和人类样本中完成,提示通过同时靶向肿瘤及其保护性微环境,可以为耐药疾病提供一种不同的治疗途径。
帮助骨髓瘤生存的一种粘性分子
骨髓瘤细胞位于骨髓中,被支持细胞和免疫细胞环绕,共同形成一个有利于肿瘤的生态位。表面分子syndecan-1在骨髓瘤细胞上表达极高,并且也会以可溶形式被剪切释放到周围空间。这两种形式像脚手架一样将生长受体和细胞表面的黏附蛋白聚集在一起,帮助癌细胞存活、扩散并躲避免疫攻击。患者血液中高水平的可溶syndecan-1与更差的预后相关,使其成为一个有吸引力的治疗靶点。
构建一种更聪明的肽类药物
研究人员此前曾设计出两种小肽,分别阻断由syndecan-1驱动的不同通路:一种恢复骨髓瘤细胞内的死亡信号,另一种干扰癌细胞迁移并释放免疫细胞的活动。在这项工作中,他们将每个肽缩短到最短的活性核心并将二者融合成一个名为SSTNIV的单一嵌合体,在血液中具有较长的半衰期。在细胞培养试验中,SSTNIV在骨髓瘤细胞和肿瘤相关巨噬细胞中强烈诱导凋亡,而对有益的T细胞影响较小。同时,它减缓了骨髓瘤细胞、抑制性巨噬细胞和调节性T细胞的迁移,但增强了杀伤性T细胞的移动能力。
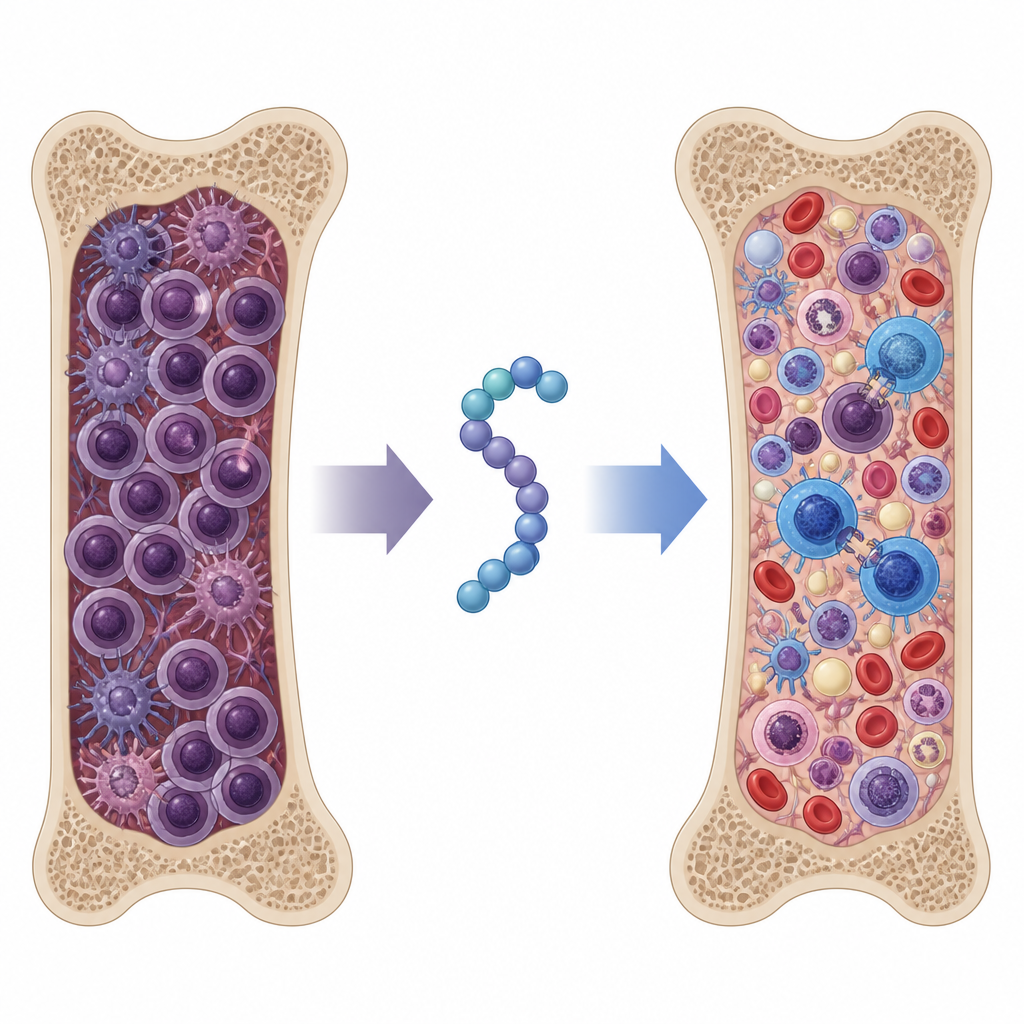
在侵袭性骨髓瘤模型中测试该肽
为评估这些效应在整体生物体中的意义,研究团队使用了一个高度模拟人类晚期耐药骨髓瘤的小鼠模型。小鼠分别接受了标准的硼替佐米化疗、原先的单功能肽之一、新的SSTNIV肽,或肽与硼替佐米的组合。血液蛋白检测和骨髓分析显示,单用SSTNIV在降低肿瘤负荷方面与旧肽加化疗的最佳组合同样有效。将硼替佐米加入SSTNIV治疗后,骨髓中可检测到的骨髓瘤细胞几乎降至正常水平,并大幅限制了对脾脏和肝脏等器官的转移。接受SSTNIV处理的小鼠存活时间更长,骨髓结构和血象得到更好保留,提示正常造血正在恢复。
唤醒免疫反应
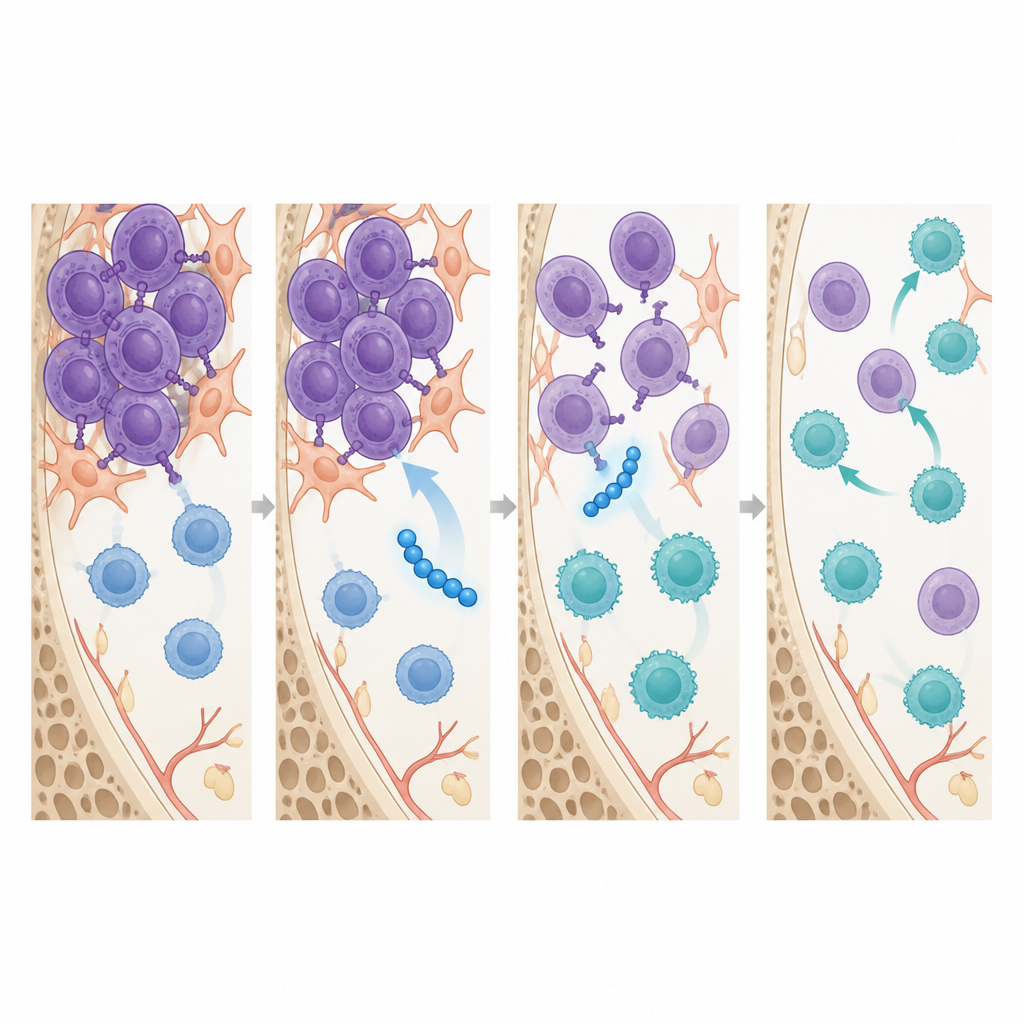
除了缩小肿瘤,SSTNIV还重塑了骨髓内的免疫格局。在治疗后一周内、在肿瘤体积出现大幅变化之前,接受SSTNIV的小鼠骨髓中细胞毒性CD8 T细胞数量增加,而通常抑制免疫攻击并帮助肿瘤耐药的两类细胞——调节性T细胞和肿瘤相关巨噬细胞——显著减少。成像研究显示,SSTNIV物理上破坏了骨髓瘤细胞上由syndecan-1组装的受体簇,重新激活了一种触发细胞死亡的应激感应器,并关闭了驱动细胞迁移的信号。在人类骨髓瘤样本中也检测到了类似的基于syndecan-1的受体复合体,但在健康供者中未见,支持这些通路是疾病特异性靶点的想法。
这对未来骨髓瘤治疗可能意味着什么
对普通读者而言,结论是这项研究探索了一种新型精准肽药,它同时攻击骨髓瘤细胞及其保护性的免疫“茧”。在晚期小鼠模型中,SSTNIV减少了骨髓中的癌细胞、限制了向其他器官的扩散、恢复了更健康的造血,并将免疫细胞转向更具攻击性的状态,尤其是在与现有化疗联合时。尽管这些发现仍处于临床前阶段,但它们表明基于SSTNIV建模的药物有朝一日可能帮助治疗对现有疗法失去反应的患者,通过破坏癌细胞依赖的关键支持系统来发挥作用。
引用: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
关键词: 多发性骨髓瘤, syndecan-1, 肿瘤微环境, 肽治疗, 免疫细胞