Clear Sky Science · ru
SSTNIV, химерный пептид, нацеленный на синдромекан‑1, восстанавливает иммунную активность и тормозит прогрессирование миеломы
Почему это исследование важно для пациентов
Множественная миелома — это рак клеток костного мозга, который часто рецидивирует после лечения, оставляя пациентам все меньше вариантов. В этом исследовании представлен новый лабораторно разработанный пептид SSTNIV, который действует против опухоли по двум направлениям одновременно: он непосредственно повреждает клетки миеломы и ослабляет влияние нездоровой иммунной среды, защищающей опухоль. Работа, выполненная на продвинутых мышиных моделях и образцах от людей, предлагает иной подход к лечению лекарственно‑устойчивой болезни, направленный как на опухоль, так и на ее защитное окружение.
Липкий молекула, которая помогает миеломе выживать
Клетки миеломы обитают в костном мозге, окруженные поддерживающими и иммунными клетками, формирующими благоприятную для опухоли нишу. Поверхностная молекула, называемая синдромекан‑1, обнаруживается на очень высоком уровне на клетках миеломы и также отщепляется в окружающее пространство. Обе формы действуют как каркас, объединяя рецепторы роста и белки сцепления на поверхностях клеток, что помогает раковым клеткам выживать, распространяться и уклоняться от иммунной атаки. Высокие уровни отщепленного синдромекан‑1 в крови пациентов связаны с худшим прогнозом, что делает эту молекулу привлекательной мишенью для терапии.
Создание более умного пептидного лекарства
Ранее исследователи создали два небольших пептида, каждый из которых блокировал один из путей, управляемых синдромекан‑1: один восстанавливал сигналы апоптоза в клетках миеломы, другой мешал движению раковых клеток и одновременно освобождал иммунные клетки для перемещения. В этой работе они сократили каждый пептид до его минимального активного ядра и слили их в единый химерный пептид SSTNIV с длительным временем циркуляции в крови. В культурах клеток SSTNIV вызывал выраженный апоптоз клеток миеломы и ассоциированных с опухолью макрофагов, при этом в основном не затрагивал полезные T‑клетки. Одновременно он замедлял миграцию клеток миеломы, иммунодепрессивных макрофагов и регуляторных T‑клеток, но усиливал подвижность цитотоксичных T‑лимфоцитов.
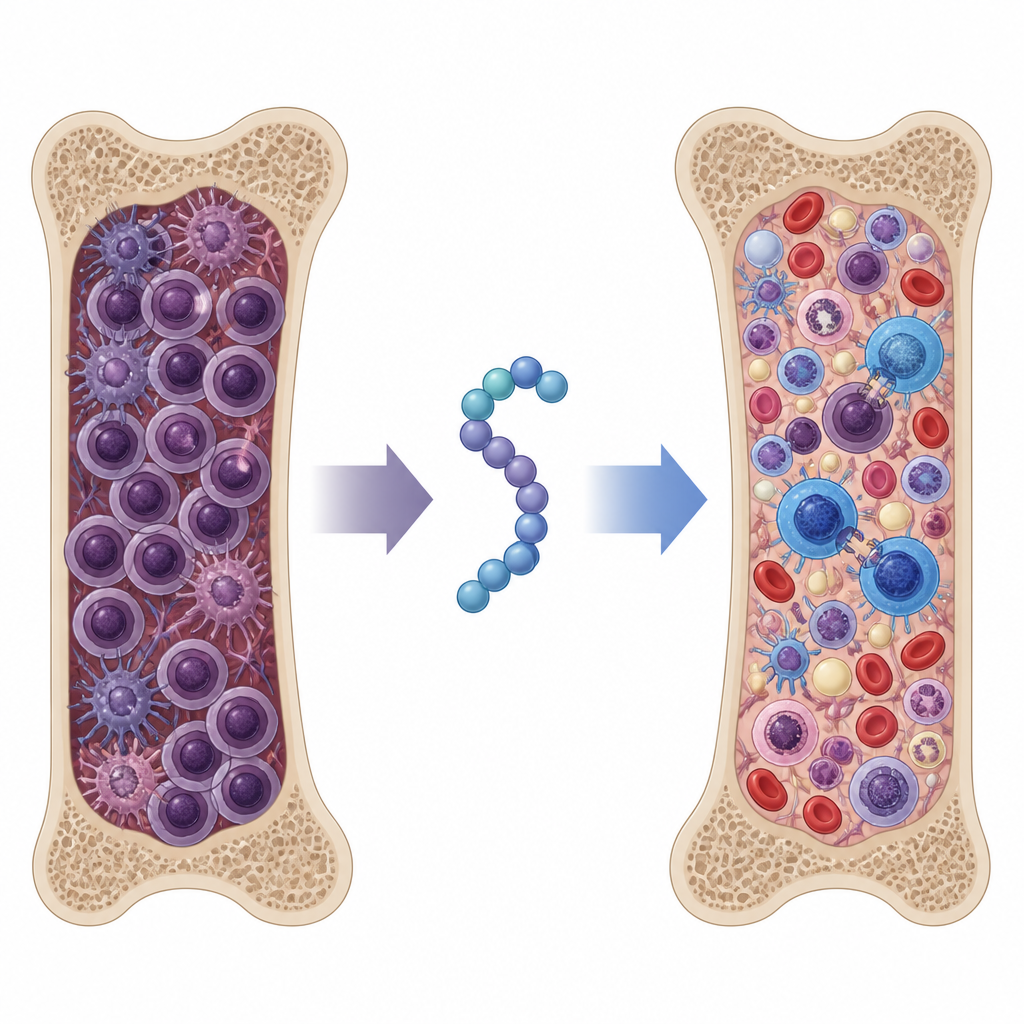
Испытание пептида в агрессивной модели миеломы
Чтобы понять, имеют ли эти эффекты значение в целом организме, команда использовала мышиную модель, хорошо имитирующую позднюю, резистентную к лечению миелому у людей. Мышам вводили либо стандартную химиотерапию бортезомибом, либо один из исходных однофункциональных пептидов, либо новый пептид SSTNIV, либо комбинации пептида с бортезомибом. Анализы белков крови и исследование костного мозга показали, что SSTNIV сам по себе сокращал опухолевую нагрузку так же эффективно, как лучшая комбинация старого пептида с химиотерапией. Добавление бортезомиба к SSTNIV снизило количество обнаруживаемых клеток миеломы в костном мозге почти до нормального уровня и существенно ограничило распространение в такие органы, как селезенка и печень. Мыши, получавшие SSTNIV, жили дольше и демонстрировали лучше сохраненную структуру костного мозга и показатели крови, что указывает на восстановление нормального кроветворения.
Пробуждение иммунного ответа
Помимо уменьшения опухоли, SSTNIV перестраивал иммунный ландшафт в костном мозге. Уже в течение недели лечения, до появления крупных изменений в размере опухоли, у мышей, получавших SSTNIV, в костном мозге увеличивалось число цитотоксичных CD8 T‑клеток и значительно сокращалось количество регуляторных T‑клеток и опухолеассоциированных макрофагов — двух типов клеток, которые обычно подавляют иммунную атаку и помогают опухолям сопротивляться лекарствам. Визуализационные исследования показали, что SSTNIV физически разрушает скопления рецепторов, собранных синдромекан‑1 на клетках миеломы, повторно активируя сенсор стресса, запускающий гибель клетки, и угнетая сигналы, ответственные за движение клеток. Похожие комплексы рецепторов, основанные на синдромекан‑1, были обнаружены в образцах костного мозга пациентов с миеломой, но не у здоровых доноров, что подтверждает идею о том, что эти пути являются специфичными мишенями при заболевании.
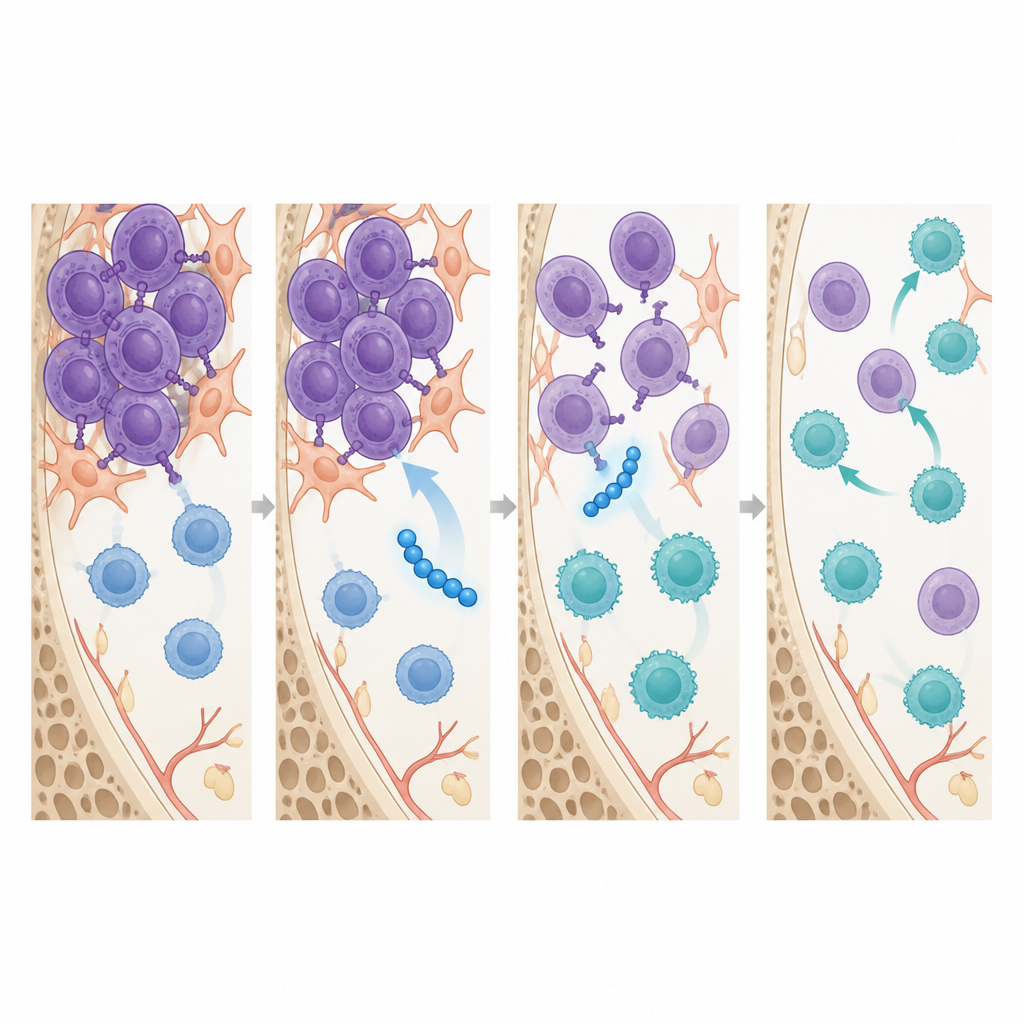
Что это может значить для будущего лечения миеломы
Для неспециалиста вывод таков: это исследование изучает новый класс точечных пептидов, которые одновременно атакуют клетки миеломы и их защитную иммунную «капсулу». В моделях продвинутой мышиной болезни SSTNIV снижал число раковых клеток в костном мозге, ограничивал метастазирование в другие органы, восстанавливал более здоровое кроветворение и сдвигал иммунный профиль в сторону готовности к атаке, особенно в сочетании с существующей химиотерапией. Хотя эти данные пока доклинические, они позволяют предположить, что препараты, смоделированные по образцу SSTNIV, в будущем могут помочь пациентам, чья миелома перестала отвечать на имеющиеся терапии, отключая ключевую систему поддержки, на которую опирается опухоль.
Цитирование: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
Ключевые слова: множественная миелома, синдромекан‑1, опухолевая микросреда, пептидная терапия, иммунные клетки