Clear Sky Science · es
SSTNIV, una quimera peptídica dirigida a la sindecán-1, revierte la supresión inmune e inhibe la progresión del mieloma
Por qué esta investigación importa a los pacientes
El mieloma múltiple es un cáncer de las células de la médula ósea que con frecuencia reaparece tras el tratamiento, dejando a los pacientes con cada vez menos opciones. Este estudio presenta un nuevo péptido diseñado en laboratorio, llamado SSTNIV, que ataca el cáncer en dos frentes a la vez: daña directamente las células de mieloma y además afloja el control de un entorno inmune disfuncional que protege al tumor. El trabajo, realizado en modelos avanzados de ratón y en muestras humanas, sugiere una vía distinta para tratar la enfermedad resistente a fármacos al dirigirse tanto al tumor como a su vecindario protector.
Una molécula adhesiva que ayuda al mieloma a prosperar
Las células de mieloma se asientan en la médula ósea rodeadas por células de soporte y células inmunes que, en conjunto, forman un nicho favorable al tumor. Una molécula de superficie llamada sindecán-1 se encuentra en niveles muy altos en las células de mieloma y también se desprende al espacio circundante. Ambas formas actúan como un andamiaje que reúne receptores de crecimiento y proteínas de anclaje en las superficies celulares, ayudando a las células cancerosas a sobrevivir, diseminarse y eludir el ataque inmune. Niveles elevados de sindecán-1 desprendido en la sangre de pacientes se asocian con peores resultados, lo que la convierte en un objetivo atractivo para la terapia.
Construyendo un fármaco peptídico más inteligente
Los investigadores habían creado previamente dos péptidos pequeños que bloqueaban por separado una vía impulsada por la sindecán-1: uno restauraba las señales de muerte celular dentro de las células de mieloma, y el otro interfería con el movimiento de las células cancerosas mientras liberaba a las células inmunes para que se desplazaran. En este trabajo recortaron cada péptido hasta su núcleo activo más corto y los fusionaron en una sola quimera llamada SSTNIV con una larga vida en el torrente sanguíneo. En pruebas en cultivo celular, SSTNIV provocó una apoptosis potente en las células de mieloma y en macrófagos asociados al tumor, mientras dejaba en su mayoría indemnes a las células T beneficiosas. Al mismo tiempo, ralentizó la migración de células de mieloma, macrófagos supresores y células T reguladoras, pero aumentó el movimiento de las células T citotóxicas que matan el cáncer.
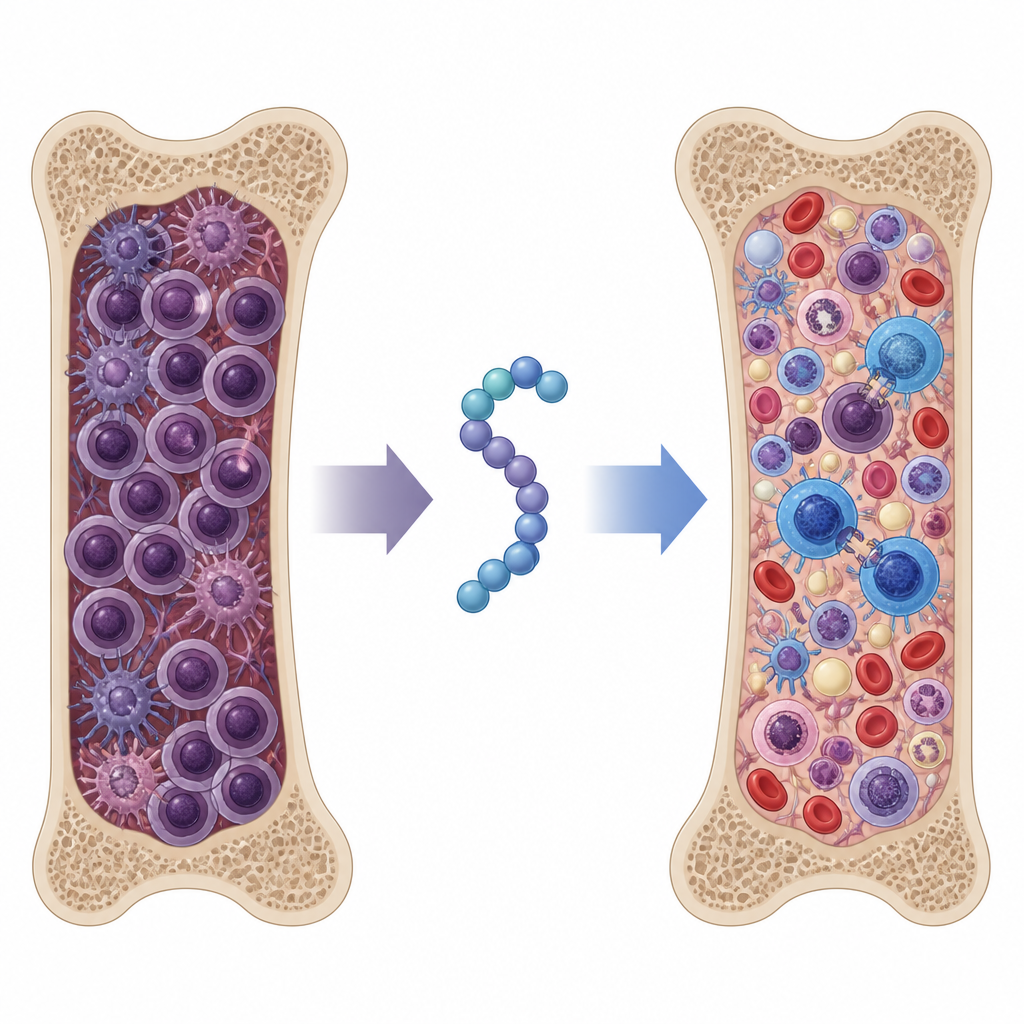
Probando el péptido en un modelo agresivo de mieloma
Para ver si estos efectos podían tener relevancia en un organismo completo, el equipo utilizó un modelo de ratón que imita de cerca el mieloma avanzado y resistente al tratamiento en humanos. Los ratones recibieron ya fuera la quimioterapia estándar bortezomib, uno de los péptidos originales de función única, el nuevo péptido SSTNIV, o combinaciones de péptido más bortezomib. Los análisis de proteínas en sangre y de médula ósea mostraron que SSTNIV por sí solo redujo la carga tumoral tan eficazmente como la mejor combinación del péptido antiguo con quimioterapia. Añadir bortezomib a SSTNIV redujo las células de mieloma detectables en médula ósea a niveles casi normales y limitó en gran medida la diseminación a órganos como el bazo y el hígado. Los ratones tratados con SSTNIV vivieron más tiempo y mostraron una mejor preservación de la estructura de la médula ósea y de los recuentos sanguíneos, lo que sugiere que la formación de sangre normal se estaba recuperando.
Reavivar la respuesta inmune
Más allá de reducir los tumores, SSTNIV remodeló el paisaje inmune dentro de la médula ósea. En el plazo de una semana de tratamiento, antes de que aparecieran grandes cambios en el tamaño del tumor, los ratones tratados con SSTNIV tenían más células T CD8 citotóxicas en su médula y muchas menos células T reguladoras y macrófagos asociados al tumor, los dos tipos celulares que habitualmente atenúan el ataque inmune y ayudan a los tumores a resistir fármacos. Estudios de imagen mostraron que SSTNIV disrumpió físicamente los cúmulos de receptores ensamblados por la sindecán-1 en las células de mieloma, reactivando un sensor de estrés que desencadena la muerte celular y apagando señales que impulsan el movimiento celular. Complejos receptores basados en sindecán-1 similares se detectaron en muestras de médula ósea de pacientes con mieloma pero no en donantes sanos, lo que respalda la idea de que estas vías son objetivos específicos de la enfermedad.
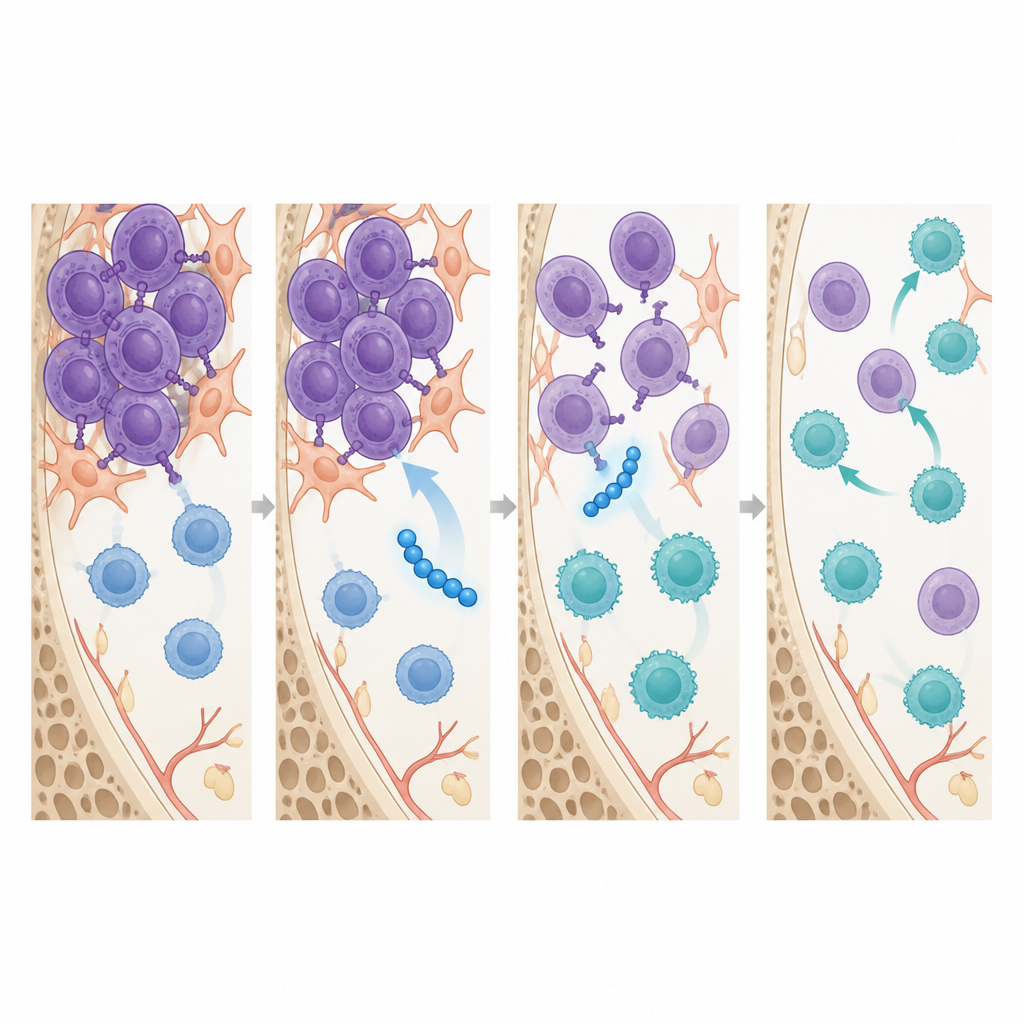
Qué podría significar esto para el tratamiento futuro del mieloma
Para un lector no especializado, la conclusión es que esta investigación explora un nuevo tipo de péptido de precisión que ataca las células de mieloma y su capullo protector inmune al mismo tiempo. En enfermedad avanzada en ratones, SSTNIV redujo las células cancerosas en médula ósea, limitó la diseminación a otros órganos, restauró una producción de sangre más saludable y orientó las células inmunes hacia un estado más proclive al ataque, especialmente cuando se combinó con la quimioterapia existente. Aunque estos hallazgos siguen siendo preclínicos, sugieren que fármacos modelados según SSTNIV podrían algún día ayudar a tratar a pacientes cuyo mieloma ha dejado de responder a las terapias actuales al desactivar un sistema de apoyo clave del que depende el cáncer.
Cita: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
Palabras clave: mieloma múltiple, sindecán-1, microambiente tumoral, terapia peptídica, células inmunes