Clear Sky Science · it
SSTNIV, un peptide chimerico che prende di mira sindecano-1, inverte la soppressione immunitaria e inibisce la progressione del mieloma
Perché questa ricerca è importante per i pazienti
Il mieloma multiplo è un tumore delle cellule del midollo osseo che spesso recidiva dopo il trattamento, lasciando ai pazienti opzioni sempre più limitate. Questo studio presenta un nuovo peptide progettato in laboratorio, chiamato SSTNIV, che agisce contro il cancro su due fronti: danneggia direttamente le cellule del mieloma e al tempo stesso allenta la presa di un ambiente immunitario alterato che protegge il tumore. Il lavoro, condotto in modelli murini avanzati e su campioni umani, suggerisce un modo differente di trattare le malattie resistenti ai farmaci mirando sia al tumore sia al suo quartiere protettivo.
Una molecola “appiccicosa” che aiuta il mieloma a prosperare
Le cellule del mieloma risiedono nel midollo osseo circondate da cellule di supporto e cellule immunitarie che insieme formano una nicchia favorevole al tumore. Una molecola di superficie chiamata sindecano-1 è presente a livelli molto alti sulle cellule del mieloma ed è anche rilasciata nello spazio circostante. Entrambe le forme agiscono come uno scheletro che mette in contatto recettori di crescita e proteine di ancoraggio sulla superficie cellulare, aiutando le cellule tumorali a sopravvivere, diffondersi ed eludere l’attacco immunitario. Livelli elevati di sindecano-1 rilasciato nel sangue dei pazienti sono associati a esiti peggiori, rendendolo un bersaglio terapeutico attraente.
Costruire un peptide terapeutico più intelligente
I ricercatori avevano in precedenza creato due piccoli peptidi che bloccavano ciascuno una via guidata da sindecano-1: uno ripristinava i segnali di morte cellulare all’interno delle cellule del mieloma, e l’altro interferiva con il movimento delle cellule tumorali liberando al contempo le cellule immunitarie per muoversi. In questo lavoro hanno ridotto ciascun peptide al nucleo attivo più breve e li hanno fusi in un unico chimera chiamata SSTNIV con una lunga emivita nel sangue. Nei test in coltura cellulare, SSTNIV ha indotto una forte apoptosi nelle cellule del mieloma e nei macrofagi associati al tumore, lasciando per lo più indenni le cellule T benefiche. Allo stesso tempo, ha rallentato la migrazione delle cellule del mieloma, dei macrofagi soppressivi e delle cellule T regolatorie, ma ha aumentato il movimento delle cellule T killer.
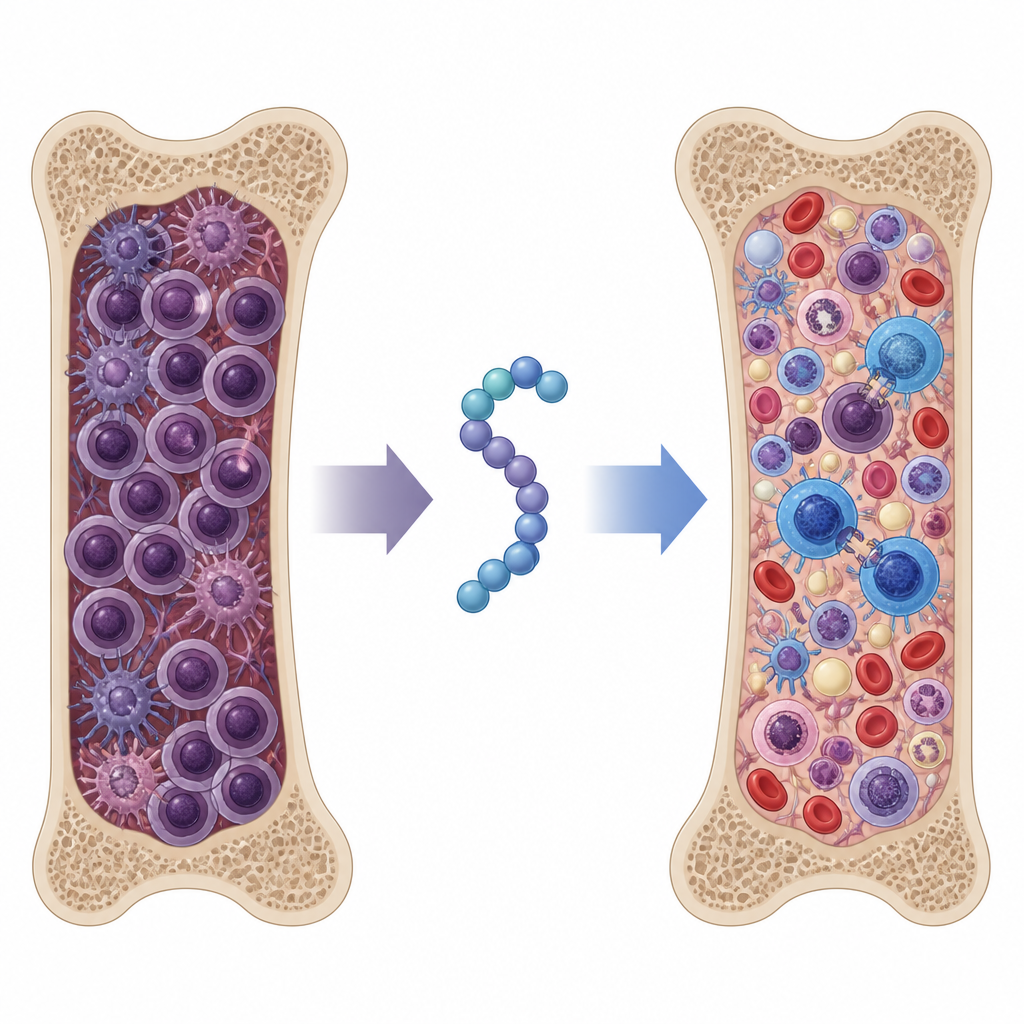
Testare il peptide in un modello aggressivo di mieloma
Per verificare se questi effetti potessero avere rilevanza in un organismo intero, il team ha utilizzato un modello murino che imita da vicino il mieloma avanzato e resistente ai trattamenti nell’uomo. I topi hanno ricevuto o la chemioterapia standard con bortezomib, uno dei peptidi originari a funzione singola, il nuovo peptide SSTNIV, o combinazioni di peptide più bortezomib. Gli esami proteici del sangue e l’analisi del midollo osseo hanno mostrato che SSTNIV da solo ha ridotto il carico tumorale efficacemente quanto la migliore combinazione del peptide più vecchio con la chemioterapia. L’aggiunta di bortezomib a SSTNIV ha ridotto le cellule di mieloma rilevabili nel midollo osseo a livelli quasi normali e ha limitato fortemente la diffusione a organi come milza e fegato. I topi trattati con SSTNIV hanno vissuto più a lungo e hanno mostrato una migliore preservazione della struttura del midollo osseo e dei parametri ematici, suggerendo un recupero della normale emopoiesi.
Riattivare la risposta immunitaria
Oltre a ridurre i tumori, SSTNIV ha rimodellato il panorama immunitario all’interno del midollo osseo. Entro una settimana dal trattamento, prima che si manifestassero grandi variazioni nelle dimensioni del tumore, i topi trattati con SSTNIV avevano più cellule T citotossiche CD8 nel midollo e molte meno cellule T regolatorie e macrofagi associati al tumore, i due tipi cellulari che normalmente attenuano l’attacco immunitario e aiutano i tumori a resistere ai farmaci. Studi di imaging hanno mostrato che SSTNIV ha fisicamente disturbato i cluster di recettori assemblati da sindecano-1 sulle cellule del mieloma, riattivando un sensore di stress che innesca la morte cellulare e spegnendo i segnali che guidano il movimento cellulare. Complessi recettoriali basati su sindecano-1 simili sono stati rilevati in campioni di midollo osseo di pazienti con mieloma ma non in donatori sani, sostenendo l’idea che queste vie siano bersagli specifici della malattia.
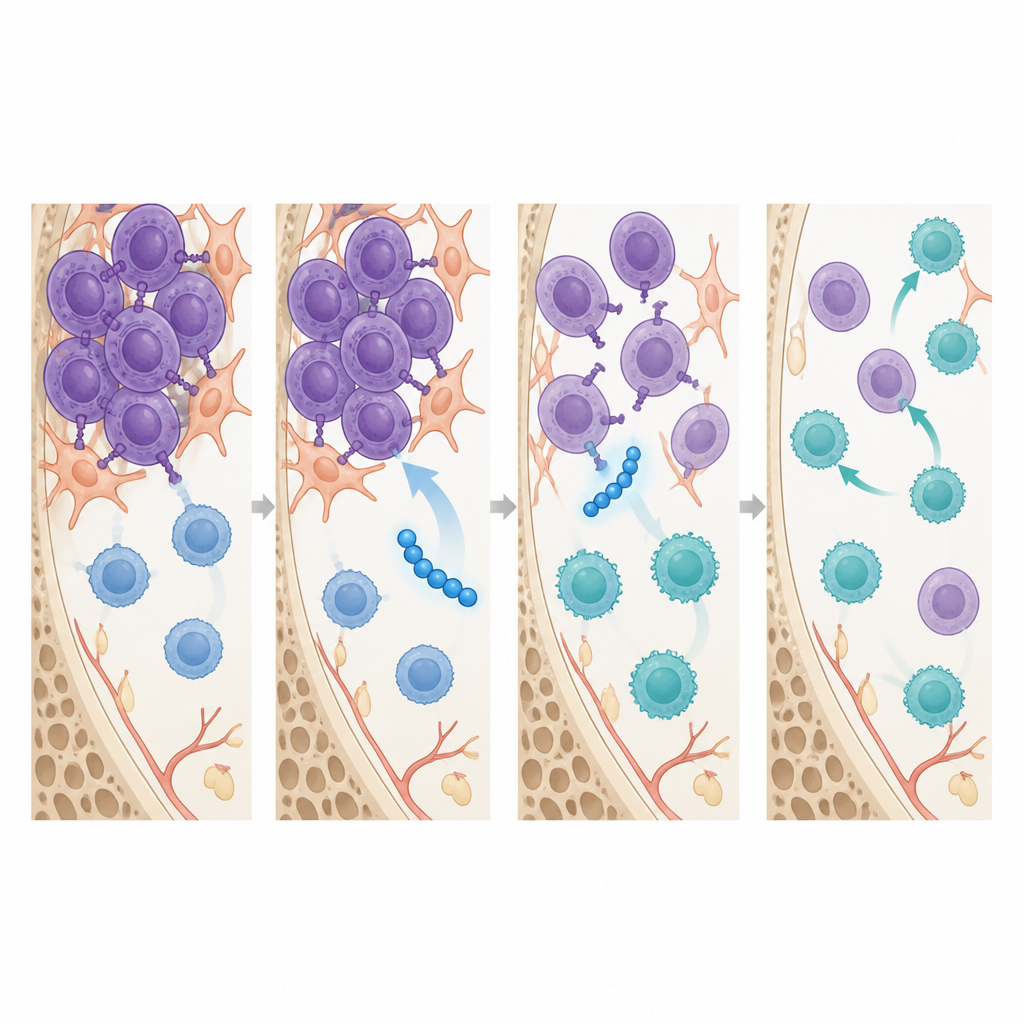
Cosa potrebbe significare per i futuri trattamenti del mieloma
Per il lettore non specialista, il messaggio è che questa ricerca esplora un nuovo tipo di peptide di precisione che attacca contemporaneamente le cellule del mieloma e il loro bozzolo immunitario protettivo. Nel modello murino di malattia avanzata, SSTNIV ha ridotto le cellule tumorali nel midollo osseo, limitato la diffusione ad altri organi, ripristinato una produzione ematica più sana e spostato le cellule immunitarie verso uno stato più pronto all’attacco, soprattutto se combinato con la chemioterapia esistente. Sebbene questi risultati siano ancora preclinici, suggeriscono che farmaci modellati su SSTNIV potrebbero un giorno aiutare i pazienti il cui mieloma ha cessato di rispondere alle terapie attuali disattivando un sistema di supporto chiave su cui il cancro fa affidamento.
Citazione: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
Parole chiave: mieloma multiplo, sindecano-1, microambiente tumorale, terapia peptidica, cellule immunitarie