Clear Sky Science · nl
SSTNIV, een peptidenchimera gericht op syndecan-1, keert immuunsuppressie om en remt progressie van myeloom
Waarom dit onderzoek belangrijk is voor patiënten
Multipel myeloom is een kanker van beenmergcellen die vaak terugkeert na behandeling, waardoor patiënten steeds minder behandelopties overhouden. Deze studie introduceert een nieuw in het laboratorium ontworpen peptide, SSTNIV, dat de kanker op twee fronten tegelijk aanvalt: het schaadt myeloomcellen direct en verzwakt tevens de greep van een ongezonde immuunomgeving die de tumor beschermt. Het werk, uitgevoerd in gevorderde muismodellen en met menselijke monsters, suggereert een andere manier om resistente ziekte te behandelen door zowel de tumor als de beschermende omgeving aan te pakken.
Een kleverig molecuul dat myeloom helpt gedijen
Myeloomcellen nestelen zich in het beenmerg omgeven door ondersteunende cellen en immuuncellen die samen een tumorvriendelijke niche vormen. Een oppervlaktemolecuul, syndecan-1, komt in zeer hoge niveaus voor op myeloomcellen en wordt ook in de omgeving afgescheiden. Beide vormen fungeren als een scaffold die groeireceptoren en hechtende eiwitten op celoppervlakken bij elkaar brengt, wat kankercellen helpt overleven, zich te verspreiden en aan immuunaanval te ontsnappen. Hoge niveaus van afgescheiden syndecan-1 in het bloed van patiënten zijn gekoppeld aan slechtere uitkomsten, wat het tot een aantrekkelijk doelwit voor therapie maakt.
Een slimmer peptidenmiddel ontwerpen
De onderzoekers hadden eerder twee kleine peptiden ontwikkeld die elk één door syndecan-1 gedreven pad blokkeerden: het ene herstelde signalen voor celdood binnen myeloomcellen, het andere verstoorde de beweging van kankercellen terwijl het immuuncellen vrijmaakte om te migreren. In dit werk verkortten ze elk peptide tot de kortste actieve kern en fuseerden die tot één chimera, SSTNIV, met een lange levensduur in de bloedbaan. In kweektests veroorzaakte SSTNIV sterke apoptose in myeloomcellen en in tumor-geassocieerde macrofagen, terwijl nuttige T-cellen grotendeels gespaard bleven. Tegelijkertijd remde het de migratie van myeloomcellen, suppressieve macrofagen en regulerende T-cellen, maar stimuleerde het de beweging van kanker-dodende T-cellen.
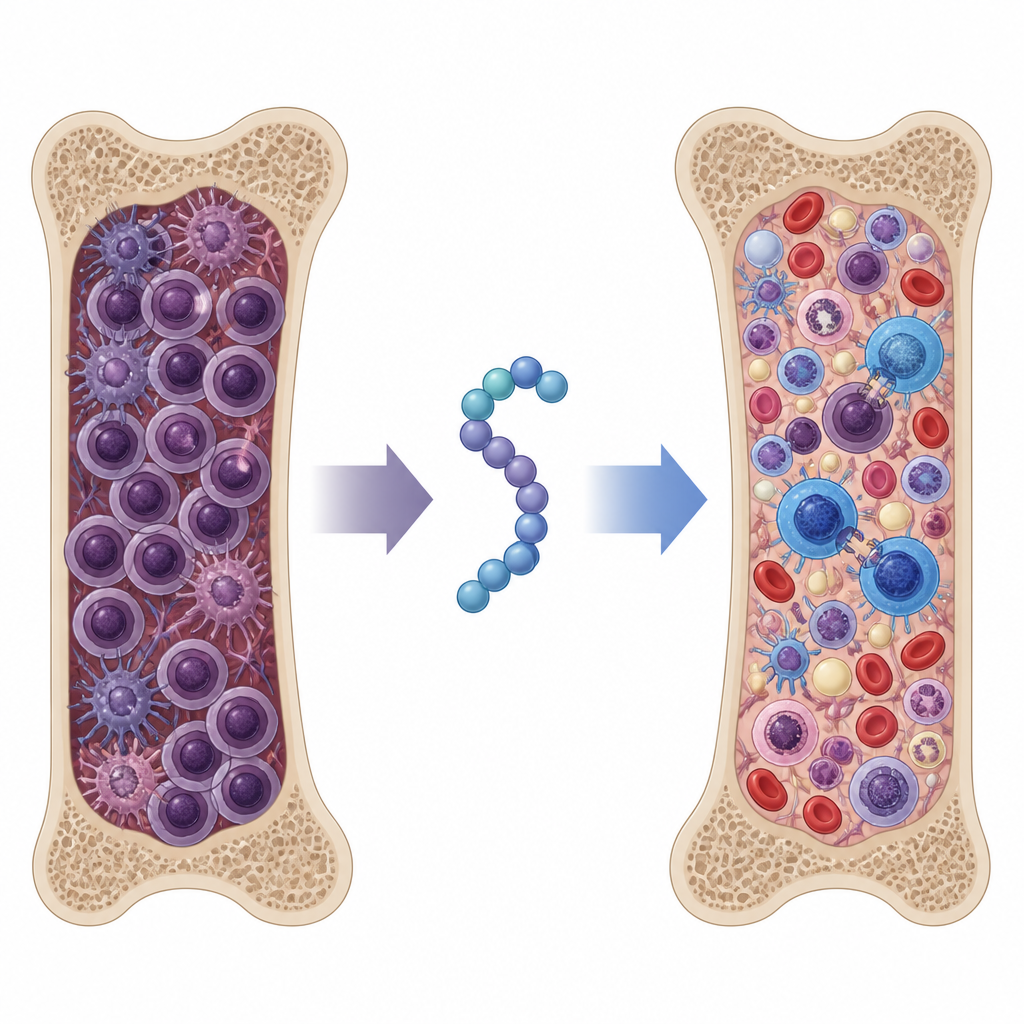
Het peptide testen in een agressief myeloommodel
Om te zien of deze effecten in een heel organisme van belang waren, gebruikte het team een muismodel dat sterk lijkt op gevorderd, therapieresistent myeloom bij mensen. Muizen kregen ofwel standaard chemotherapie met bortezomib, één van de oorspronkelijke enkelvoudige peptiden, het nieuwe SSTNIV-peptide, of combinaties van peptide plus bortezomib. Bloed-eiwitmetingen en beenmerganalyse toonden aan dat SSTNIV op zichzelf de tumorbelasting even effectief verminderde als de beste combinatie van het oudere peptide met chemotherapie. Het toevoegen van bortezomib aan SSTNIV verlaagde aantoonbare myeloomcellen in het beenmerg tot bijna normale niveaus en beperkte de verspreiding naar organen zoals milt en lever sterk. Muizen behandeld met SSTNIV leefden langer en toonden beter bewaarde beenmergstructuur en bloedwaarden, wat erop wijst dat normale bloedvorming herstelt.
Het immuunrespons heractiveren
Buiten het krimpen van tumoren, hervormde SSTNIV het immuurlandschap in het beenmerg. Binnen een week na behandeling, voordat grote veranderingen in tumorgrootte zichtbaar werden, hadden muizen die SSTNIV kregen meer cytotoxische CD8 T-cellen in hun mergholte en veel minder regulerende T-cellen en tumor-geassocieerde macrofagen, de twee celtypen die normaal gesproken de immuunaanval dempen en tumoren helpen resistent te worden tegen geneesmiddelen. Beeldvorming toonde dat SSTNIV fysieke receptorclusters die door syndecan-1 op myeloomcellen werden samengesteld, verstoorde, een stress-sensor heractiveerde die celdood triggert en signalen uitschakelde die migratie aansturen. Vergelijkbare syndecan-1-gebaseerde receptorcomplexen werden gedetecteerd in menselijke myeloom-beenmergmonsters maar niet bij gezonde donoren, wat het idee ondersteunt dat deze paden ziekte-specifieke doelen zijn.
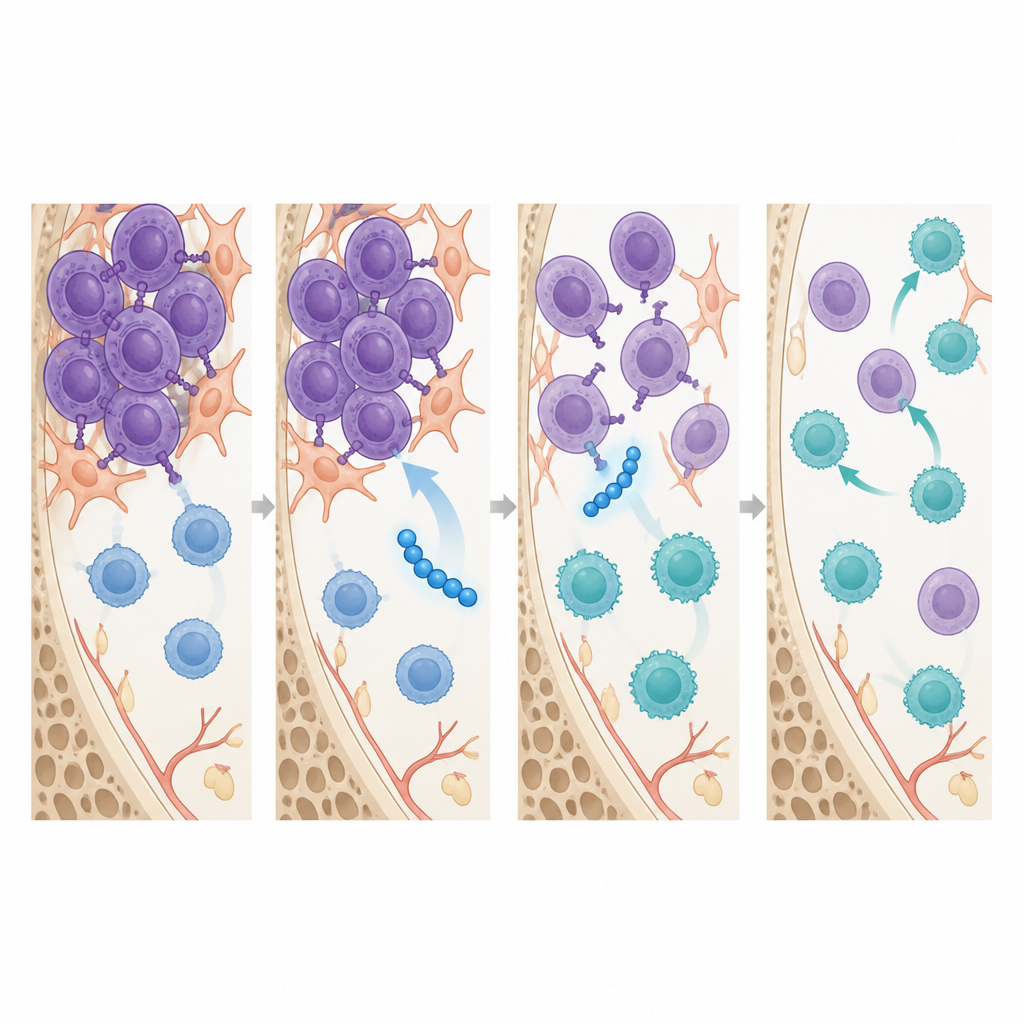
Wat dit kan betekenen voor toekomstige myeloombehandeling
Voor een algemeen publiek is de kernboodschap dat dit onderzoek een nieuw type precisiepeptide verkent dat myeloomcellen en hun beschermende immuunomhulsel tegelijk aanvalt. In gevorderde muismodellen verminderde SSTNIV het aantal kankercellen in het beenmerg, beperkte het de verspreiding naar andere organen, herstelde gezondere bloedproductie en verschuifde immuuncellen naar een meer aanvalsklare staat, vooral in combinatie met bestaande chemotherapie. Hoewel deze bevindingen nog preklinisch zijn, suggereren ze dat geneesmiddelen gemodelleerd naar SSTNIV op een dag patiënten zouden kunnen helpen van wie het myeloom niet meer reageert op huidige therapieën door een sleutelondersteuningssysteem van de kanker uit te schakelen.
Bronvermelding: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
Trefwoorden: multipel myeloom, syndecan-1, tumor-micro-omgeving, peptide-therapie, immuuncellen