Clear Sky Science · pl
SSTNIV, chimera peptydowa celująca w syndekan‑1, odwraca immunosupresję i hamuje postęp szpiczaka mnogiego
Dlaczego te badania mają znaczenie dla pacjentów
Szpiczak mnogi to nowotwór komórek szpiku kostnego, który często nawraca po leczeniu, pozostawiając pacjentom coraz mniej opcji terapeutycznych. W tym badaniu przedstawiono nowo zaprojektowany w laboratorium peptyd, nazwany SSTNIV, który atakuje chorobę na dwóch frontach: uszkadza komórki szpiczaka bezpośrednio oraz rozluźnia patogenne środowisko immunologiczne chroniące guz. Prace przeprowadzone w zaawansowanych modelach mysich i na próbkach ludzkich sugerują inną strategię leczenia chorób odpornych na leki poprzez jednoczesne celowanie w guz i jego ochronne otoczenie.
Lepląca cząsteczka, która sprzyja rozwojowi szpiczaka
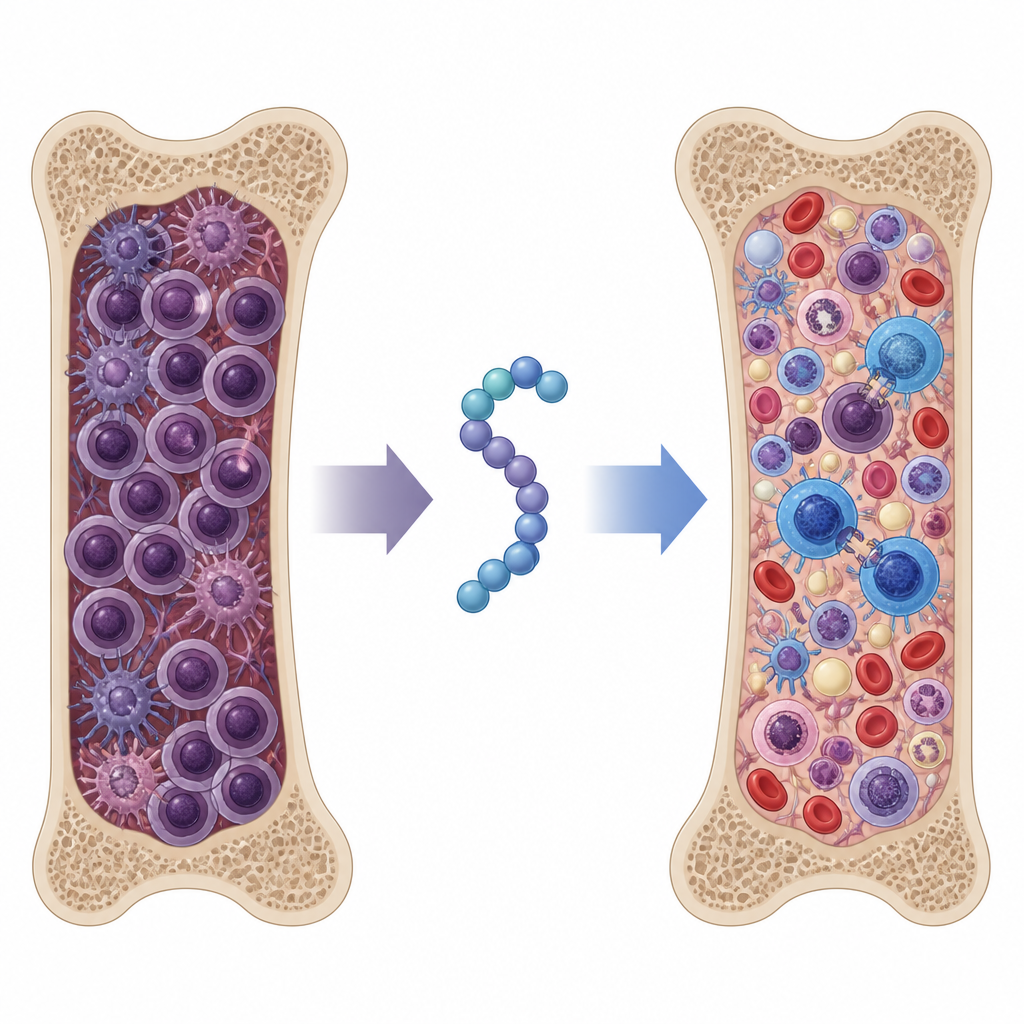
Komórki szpiczaka osadzają się w szpiku kostnym w otoczeniu komórek wspierających i komórek odpornościowych tworzących niszę sprzyjającą guzowi. Białko powierzchniowe zwane syndekan‑1 występuje w bardzo wysokim stężeniu na komórkach szpiczaka i jest także uwalniane do otaczającej przestrzeni. Obie formy działają jak rusztowanie, łącząc receptory wzrostu i białka adhezyjne na powierzchni komórek, co pomaga komórkom nowotworowym przetrwać, rozprzestrzeniać się i unikać ataku immunologicznego. Wysokie stężenia uwolnionego syndekan‑1 we krwi pacjentów wiążą się z gorszym rokowaniem, co czyni je atrakcyjnym celem terapeutycznym.
Projektowanie bardziej zaawansowanego leku peptydowego
Badacze wcześniej stworzyli dwa krótkie peptydy, z których każdy blokował jedną ze ścieżek zależnych od syndekan‑1: jeden przywracał sygnały prowadzące do śmierci komórkowej w komórkach szpiczaka, a drugi zaburzał ruchliwość komórek nowotworowych, uwalniając jednocześnie komórki odpornościowe do migracji. W niniejszej pracy każdy peptyd skrócili do najkrótszego aktywnego rdzenia i połączyli w pojedynczą chimeryczną cząsteczkę o nazwie SSTNIV, cechującą się wydłużonym czasem półtrwania we krwi. W testach in vitro SSTNIV silnie indukował apoptozę w komórkach szpiczaka i w makrofagach związanych z guzem, przy niemal minimalnym wpływie na korzystne limfocyty T. Równocześnie spowalniał migrację komórek szpiczaka, supresyjnych makrofagów i limfocytów T regulatorowych, przyspieszając ruchliwość komórek T zdolnych do niszczenia nowotworu.
Testy peptydu w agresywnym modelu szpiczaka
Aby sprawdzić, czy te efekty mają znaczenie w całym organizmie, zespół użył modelu mysiego, który wiernie naśladuje zaawansowanego, opornego na leczenie szpiczaka u ludzi. Myszy otrzymywały albo standardową chemioterapię bortezomibem, jeden z pierwotnych peptydów o pojedynczej funkcji, nowy peptyd SSTNIV, albo kombinacje peptydu z bortezomibem. Badania białek we krwi i analizy szpiku wykazały, że SSTNIV sam w sobie zmniejszał obciążenie guzem równie skutecznie jak najlepsza kombinacja starszego peptydu z chemioterapią. Dodanie bortezomibu do SSTNIV obniżało wykrywalne komórki szpiczaka w szpiku do niemal normalnych poziomów i znacząco ograniczało przerzuty do narządów takich jak śledziona i wątroba. Myszy leczone SSTNIV żyły dłużej i miały lepiej zachowaną strukturę szpiku oraz liczby krwinek, co sugeruje przywracanie prawidłowego procesu tworzenia krwi.
Przywrócenie odpowiedzi immunologicznej
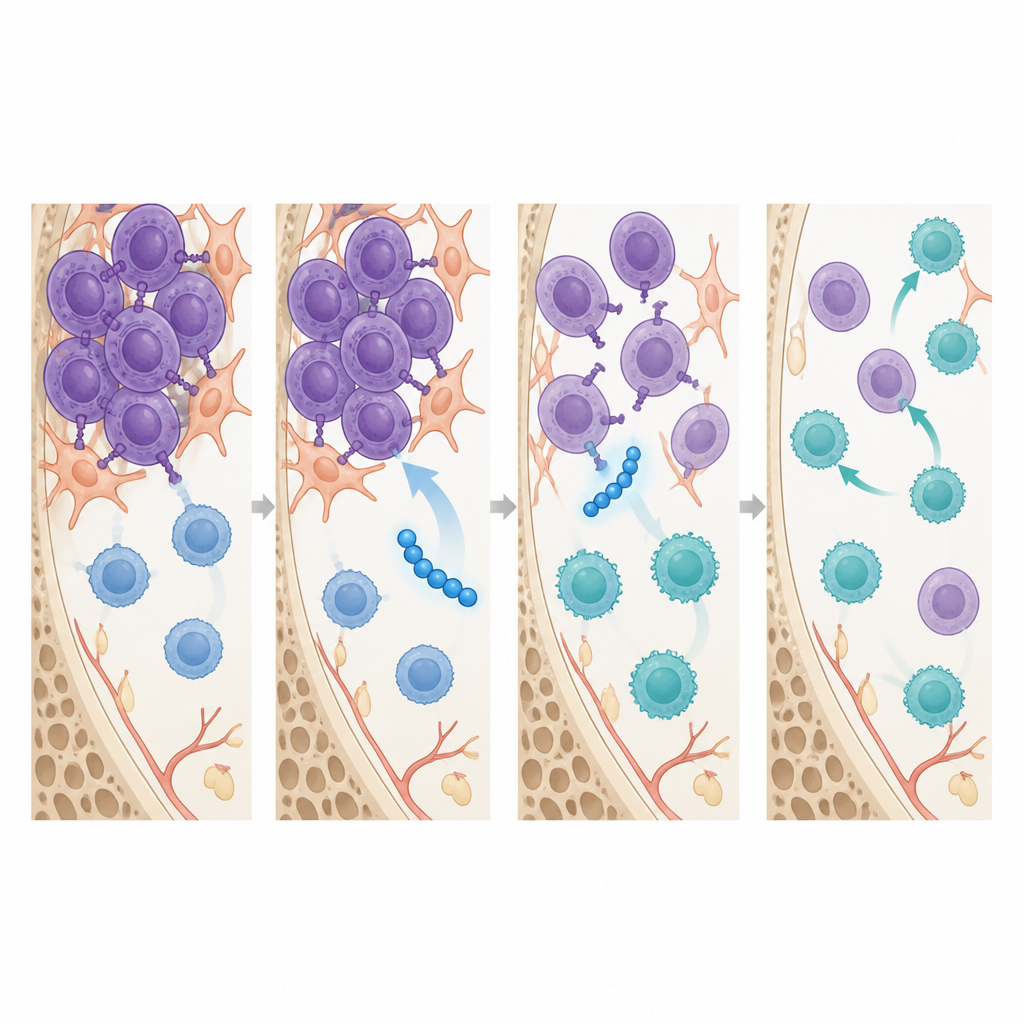
Poza zmniejszaniem guzów, SSTNIV przekształcał krajobraz immunologiczny w szpiku kostnym. W ciągu tygodnia od rozpoczęcia terapii, jeszcze przed wystąpieniem dużych zmian w wielkości guza, myszy leczone SSTNIV miały więcej cytotoksycznych limfocytów CD8 w szpiku i znacznie mniej limfocytów T regulatorowych oraz makrofagów związanych z guzem — dwóch typów komórek, które zazwyczaj tłumią odpowiedź immunologiczną i pomagają guzom w oporności na leki. Badania obrazowe wykazały, że SSTNIV fizycznie rozpraszał skupiska receptorów organizowane przez syndekan‑1 na komórkach szpiczaka, reaktywując czujnik stresu, który uruchamia śmierć komórkową, oraz hamując sygnały kierujące migracją komórek. Podobne kompleksy receptorowe zależne od syndekan‑1 wykryto w próbkach szpiku ludzkiego od chorych na szpiczaka, ale nie u zdrowych dawców, co potwierdza, że te szlaki stanowią specyficzne dla choroby cele.
Co to może oznaczać dla przyszłego leczenia szpiczaka
Dla czytelnika niebędącego specjalistą kluczowe jest to, że badania eksplorują nowy typ precyzyjnego peptydu, który jednocześnie atakuje komórki szpiczaka i ich ochronną immunologiczną otoczkę. W zaawansowanym modelu mysim SSTNIV zmniejszał liczbę komórek nowotworowych w szpiku, ograniczał przerzuty do innych narządów, przywracał zdrowsze tworzenie krwi i przesuwał skład komórek odpornościowych w kierunku stanu gotowości do ataku, zwłaszcza w połączeniu z istniejącą chemioterapią. Chociaż wyniki są wciąż przedkliniczne, sugerują, że leki wzorowane na SSTNIV mogłyby w przyszłości pomóc pacjentom, których szpiczak przestał reagować na dostępne terapie, przez unieruchomienie kluczowego mechanizmu wsparcia, od którego zależy nowotwór.
Cytowanie: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
Słowa kluczowe: szpiczak mnogi, syndekan‑1, mikrośrodowisko guza, terapia peptydowa, komórki odpornościowe