Clear Sky Science · sv
SSTNIV, en peptidchimär som riktar sig mot syndecan-1, vänder immunsuppression och hämmar myelomets progression
Varför denna forskning betyder något för patienter
Multipelt myelom är en cancer i benmärgens celler som ofta återkommer efter behandling, vilket lämnar patienter med allt färre behandlingsalternativ. Denna studie presenterar ett nytt laboratoriedesignat peptid, kallat SSTNIV, som angriper cancern på två fronter samtidigt: det skadar myelomceller direkt och luckrar också upp ett ohälsosamt immungsmiljö som skyddar tumören. Arbetet, utfört i avancerade musemodeller och mänskliga prover, antyder ett annat sätt att behandla läkemedelsresistent sjukdom genom att rikta in sig både på tumören och dess skyddande omgivning.
En klibbig molekyl som hjälper myelom att frodas
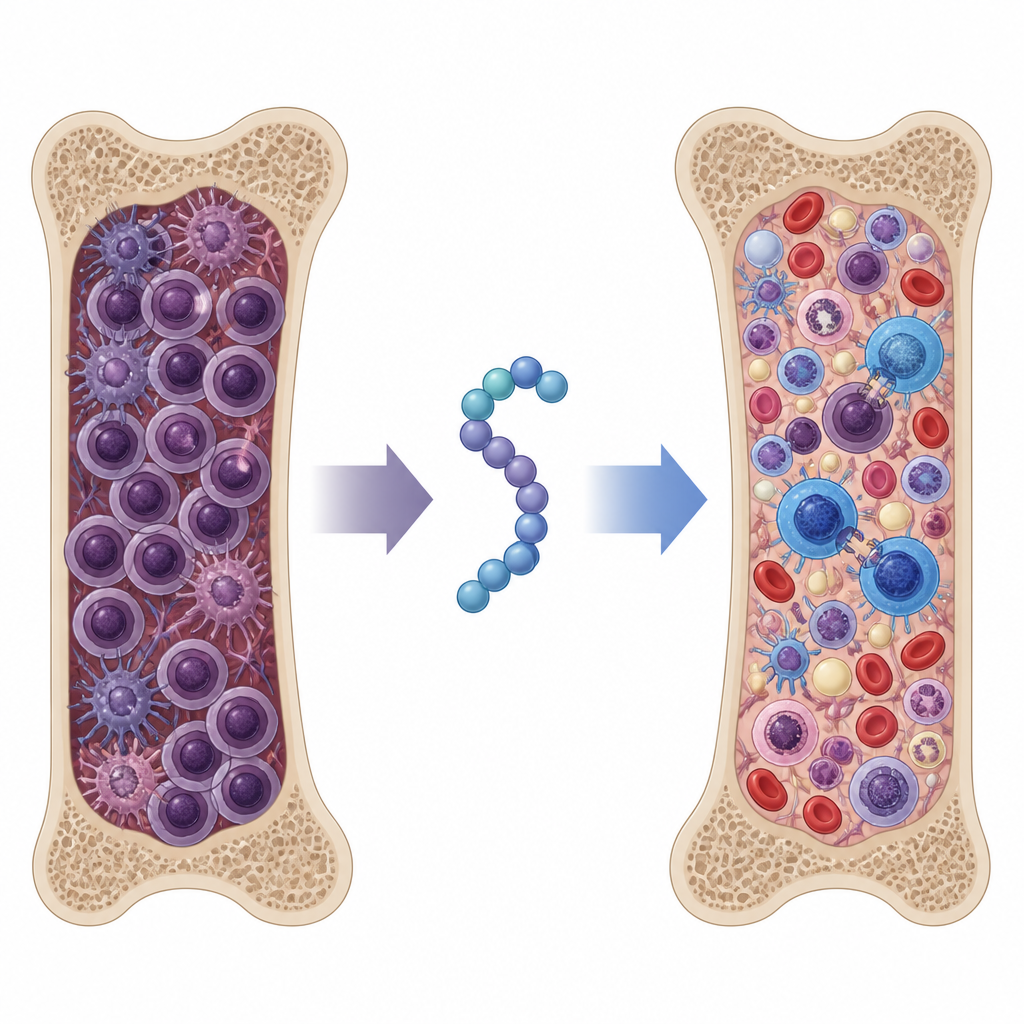
Myelomceller sitter i benmärgen omgivna av stödjeceller och immunceller som tillsammans bildar en tumörvänlig nisch. En ytmolekyl kallad syndecan-1 finns i mycket höga nivåer på myelomceller och släpps även löst ut i omgivningen. Båda formerna fungerar som ett ställverk som för samman tillväxtreceptorer och fästproteiner på cellytor, vilket hjälper cancercellerna att överleva, sprida sig och undkomma immunsystemets angrepp. Höga nivåer av utsläppt syndecan-1 i patienters blod är kopplade till sämre prognos, vilket gör det till ett attraktivt mål för terapi.
Att bygga ett smartare peptidläkemedel
Forskarna hade tidigare skapat två små peptider som vardera blockerade en syndecan-1‑driven väg: den ena återställde signalsystem för celldöd inne i myelomcellerna, och den andra störde cancercellers rörelse samtidigt som den frigjorde immunceller att röra sig. I detta arbete beskärde de varje peptid till dess kortaste aktiva kärna och förenade dem till en enda chimär kallad SSTNIV med lång halveringstid i blodomloppet. I cellodlingstester utlöste SSTNIV stark apoptos i myelomceller och i tumörassocierade makrofager, samtidigt som gynnsamma T‑celler i huvudsak lämnades intakta. Samtidigt hämnade den migrationen av myelomceller, suppressiva makrofager och regulatoriska T‑celler, men ökade rörligheten hos cancer‑dödande T‑celler.
Test av peptiden i en aggressiv myelommodell
För att se om dessa effekter kunde få betydelse i en hel organism använde teamet en musemodell som nära efterliknar avancerat, behandlingsresistent myelom hos människor. Mössen fick antingen standardkemoterapin bortezomib, en av de ursprungliga enkelriktade peptiderna, den nya SSTNIV‑peptiden, eller kombinationer av peptid plus bortezomib. Blodproteinprov och analyser av benmärg visade att SSTNIV på egen hand minskade tumörbördan lika effektivt som den bästa kombinationen av den äldre peptiden med kemoterapi. Att lägga till bortezomib till SSTNIV reducerade detekterbara myelomceller i benmärgen till nästan normala nivåer och begränsade i hög grad spridning till organ som mjälte och lever. Möss behandlade med SSTNIV levde längre och uppvisade bättre bevarad benmärgsstruktur och blodvärden, vilket tyder på att normal blodbildning återhämtade sig.
Att återväcka immunsvaret
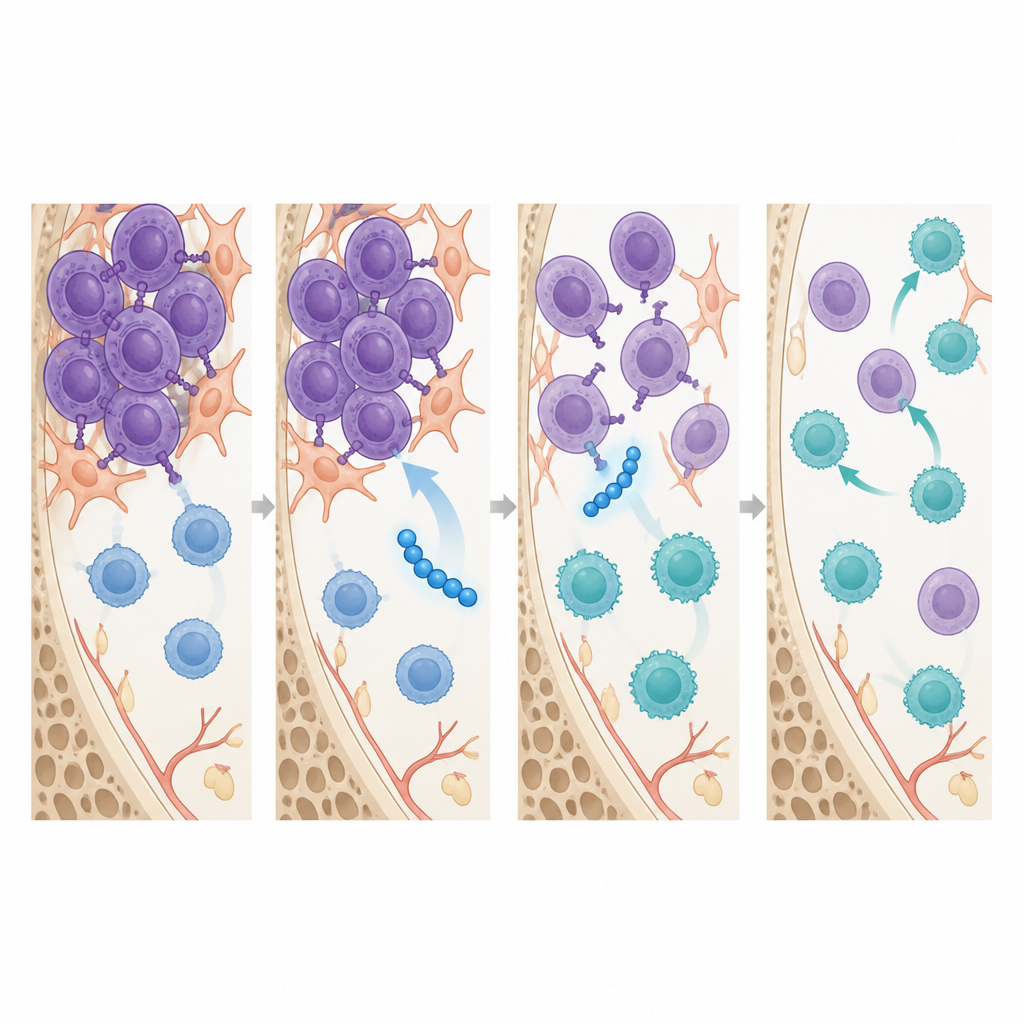
Utöver att krympa tumörer omformade SSTNIV immunlandskapet inne i benmärgen. Inom en vecka efter behandling, innan stora förändringar i tumörstorlek uppträdde, hade möss som fått SSTNIV fler cytotoxiska CD8 T‑celler i sin märg och betydligt färre regulatoriska T‑celler och tumörassocierade makrofager, de två celltyper som vanligtvis dämpar immunsvar och hjälper tumörer att motstå läkemedel. Avbildningsstudier visade att SSTNIV fysiskt störde de receptorkluster som byggs upp av syndecan‑1 på myelomceller, återaktiverade en stressensor som utlöser celldöd och stängde av signaler som driver cellrörelse. Liknande syndecan‑1‑baserade receptorcomplex kunde upptäckas i mänskliga myelombenmärgsexemplar men inte hos friska donatorer, vilket stöder idén att dessa vägar är sjukdomsspecifika mål.
Vad detta kan betyda för framtida myelombehandling
För en lekmannaläsare är slutsatsen att denna forskning utforskar en ny typ av precisionspeptid som angriper myelomceller och deras skyddande immunkapsel samtidigt. I avancerad musmodell minskade SSTNIV cancerceller i benmärgen, begränsade spridning till andra organ, återställde friskare blodbildning och försköt immunceller mot ett mer attackberedskap tillstånd, särskilt i kombination med befintlig kemoterapi. Även om dessa fynd fortfarande är prekliniska, antyder de att läkemedel modellerade på SSTNIV en dag skulle kunna hjälpa patienter vars myelom slutat svara på dagens behandlingar genom att inaktivera ett centralt stödsystem som cancern är beroende av.
Citering: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
Nyckelord: multipelt myelom, syndecan-1, tumörmikromiljö, peptidterapi, immunceller