Clear Sky Science · fr
SSTNIV, une chimère peptidique ciblant la syndécane‑1, renverse l’immunosuppression et inhibe la progression du myélome
Pourquoi cette recherche importe pour les patients
Le myélome multiple est un cancer des cellules de la moelle osseuse qui récidive souvent après traitement, laissant les patients avec des options thérapeutiques de plus en plus limitées. Cette étude présente un nouveau peptide conçu en laboratoire, nommé SSTNIV, qui attaque la maladie sur deux fronts : il nuit directement aux cellules myélomateuses et relâche en même temps l’étau d’un microenvironnement immunitaire délétère qui protège la tumeur. Les travaux, réalisés sur des modèles murins avancés et sur des échantillons humains, suggèrent une approche alternative pour traiter les maladies résistantes aux médicaments en ciblant à la fois la tumeur et son environnement protecteur.
Une molécule collante qui aide le myélome à prospérer
Les cellules myélomateuses résident dans la moelle osseuse entourées de cellules de soutien et de cellules immunitaires qui forment ensemble une niche favorable à la tumeur. Une molécule de surface appelée syndécane‑1 est présente à des niveaux très élevés sur les cellules myélomateuses et est également libérée dans le milieu environnant. Les deux formes agissent comme un échafaudage rassemblant récepteurs de croissance et protéines d’adhésion à la surface cellulaire, aidant les cellules cancéreuses à survivre, à se diffuser et à échapper à l’attaque immunitaire. Des niveaux élevés de syndécane‑1 circulante chez les patients sont associés à de moins bons pronostics, ce qui en fait une cible thérapeutique attrayante.
Concevoir un médicament peptidique plus intelligent
Les chercheurs avaient précédemment mis au point deux petits peptides qui bloquaient chacun une voie activée par la syndécane‑1 : l’un rétablissait les signaux d’apoptose à l’intérieur des cellules myélomateuses, l’autre perturbait la migration des cellules cancéreuses tout en libérant les cellules immunitaires pour qu’elles puissent se déplacer. Dans ce travail, ils ont réduit chaque peptide à son noyau actif le plus court et les ont fusionnés en une seule chimère, SSTNIV, dotée d’une longue demi‑vie dans le sang. En culture cellulaire, SSTNIV a déclenché une apoptose marquée des cellules myélomateuses et des macrophages associés aux tumeurs, tout en épargnant pour la plupart les lymphocytes T bénéfiques. Parallèlement, il a ralenti la migration des cellules myélomateuses, des macrophages suppressifs et des lymphocytes T régulateurs, tout en favorisant le déplacement des cellules T tueuses du cancer.
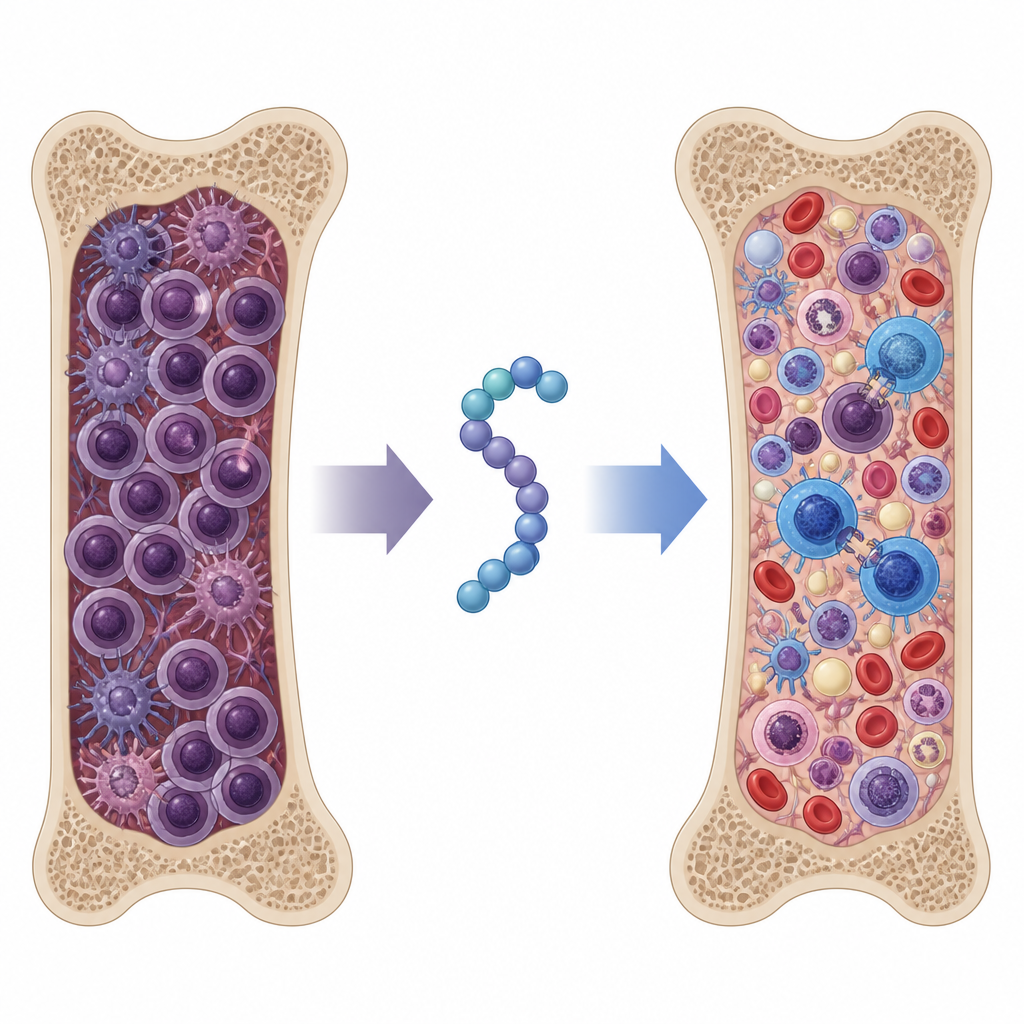
Tester le peptide dans un modèle agressif de myélome
Pour savoir si ces effets avaient un impact dans un organisme entier, l’équipe a utilisé un modèle murin reproduisant fidèlement un myélome avancé et résistant chez l’homme. Les souris ont reçu soit la chimiothérapie standard au bortézomib, soit l’un des peptides originaux monofonctionnels, soit le nouveau peptide SSTNIV, ou des combinaisons peptide plus bortézomib. Les dosages protéiques sanguins et l’analyse de la moelle osseuse ont montré que SSTNIV seul réduisait la charge tumorale aussi efficacement que la meilleure combinaison de l’ancien peptide avec la chimiothérapie. L’ajout de bortézomib à SSTNIV a abaissé le nombre de cellules myélomateuses détectables dans la moelle osseuse à des niveaux quasi normaux et a fortement limité la dissémination vers des organes comme la rate et le foie. Les souris traitées par SSTNIV ont vécu plus longtemps et présentaient une structure de la moelle osseuse et des chiffres sanguins mieux préservés, suggérant une reprise de la formation normale du sang.
Réanimer la réponse immunitaire
Au‑delà de la réduction tumorale, SSTNIV a remodelé le paysage immunitaire au sein de la moelle osseuse. En une semaine de traitement, avant l’apparition de changements importants de taille tumorale, les souris ayant reçu SSTNIV présentaient plus de lymphocytes CD8 cytotoxiques dans leur moelle et bien moins de lymphocytes T régulateurs et de macrophages associés aux tumeurs, deux populations qui atténuent normalement l’attaque immune et aident les tumeurs à résister aux traitements. Des études d’imagerie ont montré que SSTNIV perturbait physiquement les amas de récepteurs formés par la syndécane‑1 sur les cellules myélomateuses, réactivant un senseur de stress qui déclenche la mort cellulaire et coupant les signaux qui pilotent la migration cellulaire. Des complexes récepteurs basés sur la syndécane‑1 similaires ont été détectés dans des échantillons de moelle osseuse de patients myélomateux mais pas chez des donneurs sains, soutenant l’idée que ces voies sont des cibles spécifiques de la maladie.
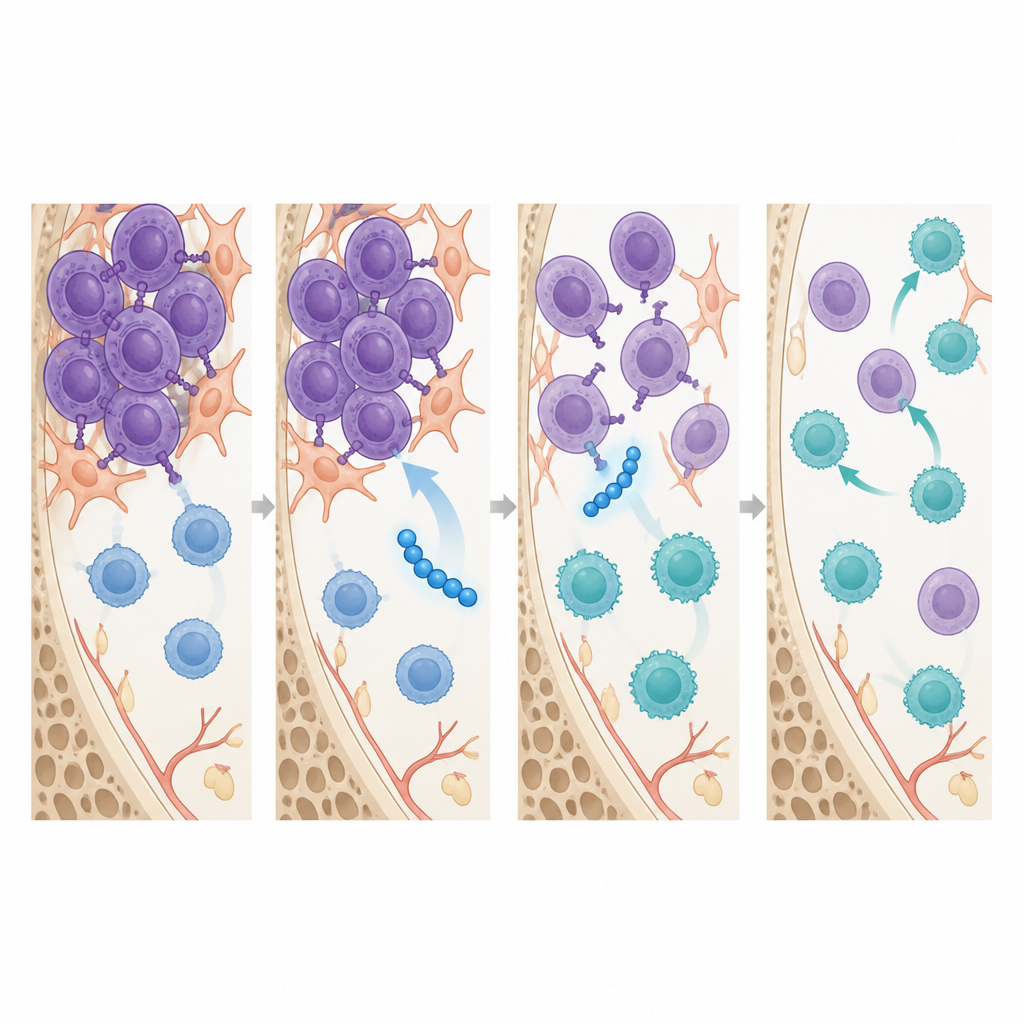
Ce que cela pourrait signifier pour le traitement futur du myélome
Pour le lecteur non spécialiste, l’essentiel est que cette recherche explore un nouveau type de peptide de précision qui attaque simultanément les cellules myélomateuses et leur cocon immunitaire protecteur. Dans un modèle murin de maladie avancée, SSTNIV a réduit les cellules cancéreuses dans la moelle osseuse, limité la dissémination vers d’autres organes, restauré une production sanguine plus saine et orienté les cellules immunitaires vers un état plus prêt à attaquer, en particulier en association avec la chimiothérapie existante. Bien que ces résultats restent précliniques, ils suggèrent que des médicaments modélisés sur SSTNIV pourraient un jour aider les patients dont le myélome ne répond plus aux thérapies actuelles en neutralisant un système de soutien clé sur lequel la tumeur dépend.
Citation: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
Mots-clés: myélome multiple, syndécane‑1, microenvironnement tumoral, thérapie peptidique, cellules immunitaires