Clear Sky Science · de
SSTNIV, ein auf Syndecan-1 zielender Peptidchimär, hebt Immunsuppression auf und hemmt das Fortschreiten des Myeloms
Warum diese Forschung für Patientinnen und Patienten wichtig ist
Multiples Myelom ist ein Krebs der Knochenmarkszellen, der oft nach einer Behandlung wiederkehrt und den Betroffenen zunehmend weniger Optionen lässt. Diese Studie stellt ein neu entwickeltes Peptid namens SSTNIV vor, das den Tumor auf zwei Arten zugleich angreift: Es schädigt Myelomzellen direkt und lockert gleichzeitig das ungünstige Immunumfeld, das den Tumor schützt. Die Arbeiten an fortgeschrittenen Mausmodellen und an menschlichen Proben deuten auf einen neuen Behandlungsansatz für medikamentenresistente Erkrankungen hin, bei dem sowohl der Tumor als auch seine schützende Nachbarschaft angegriffen werden.
Ein klebriges Molekül, das dem Myelom hilft zu gedeihen
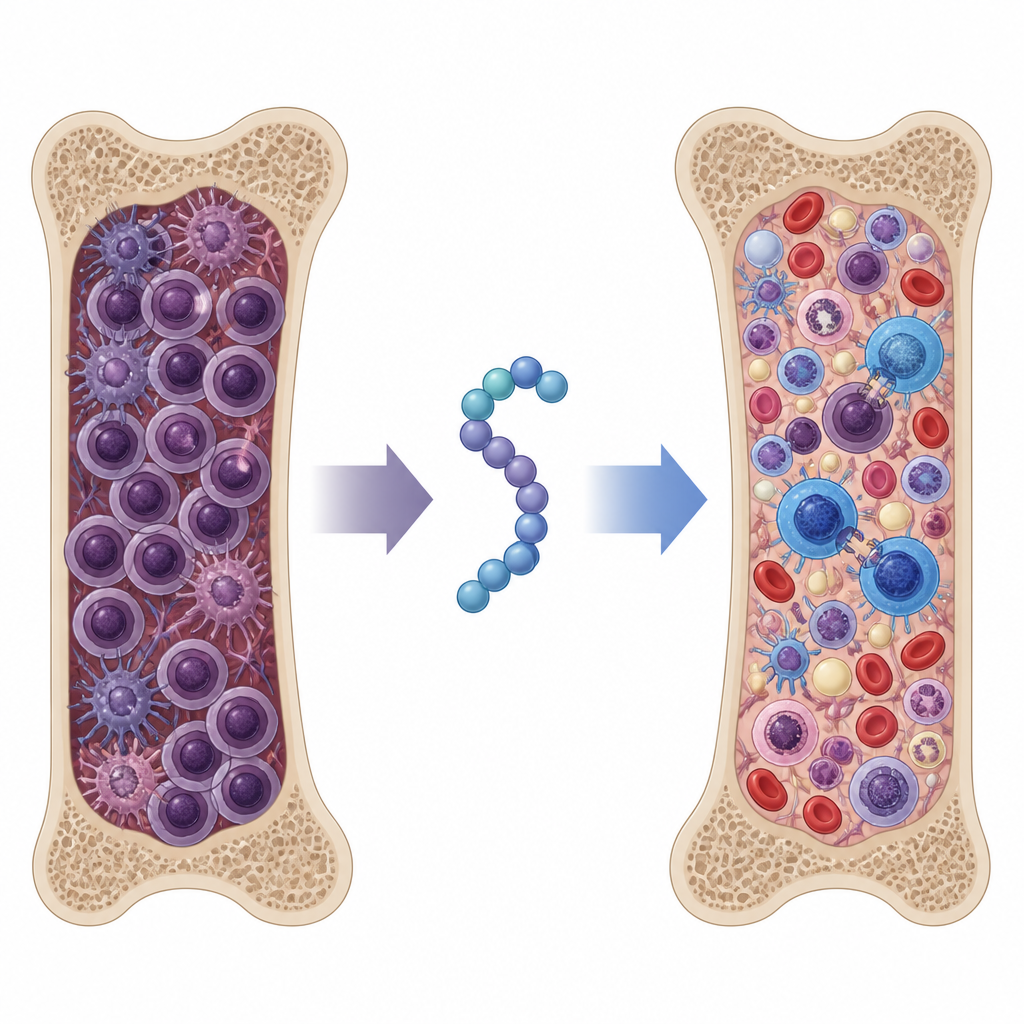
Myelomzellen sitzen im Knochenmark umgeben von Stützzellen und Immunzellen, die zusammen eine tumorfördernde Nische bilden. Ein Oberflächenmolekül namens Syndecan-1 kommt auf Myelomzellen in sehr hohen Mengen vor und wird außerdem in die Umgebung abgeschieden. Beide Formen wirken wie ein Gerüst, das Wachstumsrezeptoren und Haftproteine an Zelloberflächen zusammenbringt, wodurch Krebszellen beim Überleben, beim Ausbreiten und beim Umgehen der Immunabwehr unterstützt werden. Hohe Werte von ausgeschiedenem Syndecan-1 im Blut von Patienten korrelieren mit schlechterer Prognose, was es zu einem attraktiven Therapieansatz macht.
Entwicklung eines intelligenteren Peptidwirkstoffs
Die Forschenden hatten zuvor zwei kleine Peptide entwickelt, die jeweils einen von Syndecan-1 gesteuerten Signalweg blockierten: Eines stellte die Todes-Signale innerhalb der Myelomzellen wieder her, das andere störte die Beweglichkeit der Krebszellen und befreite gleichzeitig Immunzellen, damit sie sich bewegen konnten. In dieser Arbeit kürzten sie jedes Peptid auf seinen kürzesten aktiven Kern und verbanden die beiden zu einer einzigen Chimäre namens SSTNIV mit langer Verweildauer im Blutkreislauf. In Zellkulturtests löste SSTNIV starke Apoptose in Myelomzellen und in tumornahen Makrophagen aus, während nützliche T‑Zellen weitgehend verschont blieben. Gleichzeitig verlangsamte es die Migration von Myelomzellen, suppressiven Makrophagen und regulatorischen T‑Zellen, erhöhte aber die Beweglichkeit von krebsabtötenden T‑Zellen.
Test des Peptids in einem aggressiven Myelommodell
Um zu prüfen, ob diese Effekte in einem ganzen Organismus relevant sind, nutzte das Team ein Mausmodell, das fortgeschrittenes, therapieresistentes Myelom beim Menschen gut nachbildet. Die Mäuse erhielten entweder die Standardchemotherapie Bortezomib, eines der ursprünglichen einzelfunktionalen Peptide, das neue Peptid SSTNIV oder Kombinationen aus Peptid und Bortezomib. Blutprotein-Tests und Knochenmarkanalysen zeigten, dass SSTNIV allein die Tumorlast ebenso wirksam verringerte wie die beste Kombination des älteren Peptids mit Chemotherapie. Die Zugabe von Bortezomib zu SSTNIV reduzierte nachweisbare Myelomzellen im Knochenmark auf nahezu normale Werte und begrenzte die Ausbreitung auf Organe wie Milz und Leber deutlich. Mit SSTNIV behandelte Mäuse lebten länger und zeigten besser erhaltene Knochenmarkstruktur und Blutwerte, was darauf hindeutet, dass die normale Blutbildung sich erholte.
Wiedererweckung der Immunantwort
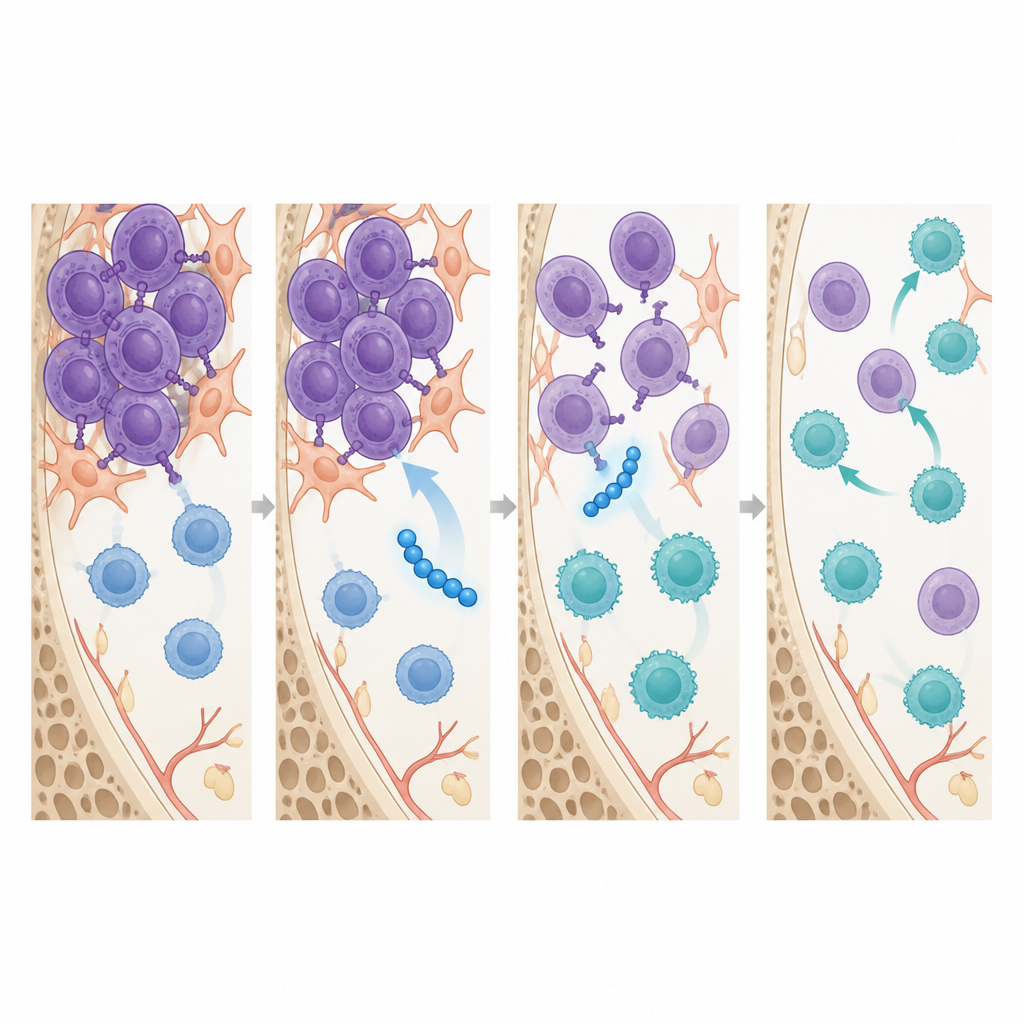
Über die Tumorverkleinerung hinaus formte SSTNIV die Immunlandschaft im Knochenmark um. Innerhalb einer Woche nach Behandlung, also bevor große Veränderungen der Tumorgröße sichtbar wurden, hatten Mäuse, die SSTNIV erhielten, mehr zytotoxische CD8‑T‑Zellen in ihrem Mark und deutlich weniger regulatorische T‑Zellen sowie tumornahe Makrophagen – die beiden Zelltypen, die normalerweise Immunangriffe dämpfen und Tumoren helfen, Medikamenten zu widerstehen. Bildgebende Studien zeigten, dass SSTNIV die von Syndecan-1 gebildeten Rezeptorkluster auf Myelomzellen physisch störte, einen Stresssensor reaktivierte, der zum Zelltod führt, und Signale ausschaltete, die die Zellbewegung antreiben. Ähnliche syndecan-1-basierte Rezeptorkomplexe wurden in Knochenmarkproben von Myelompatienten, jedoch nicht in Proben gesunder Spender nachgewiesen, was die Idee stützt, dass diese Wege krankheitsspezifische Ziele sind.
Was das für die zukünftige Myelombehandlung bedeuten könnte
Für Laien lässt sich festhalten, dass diese Forschung einen neuen Typ Präzisionspeptids untersucht, der Myelomzellen und ihre schützende Immunhülle zugleich angreift. In einem fortgeschrittenen Mausmodell reduzierte SSTNIV die Krebszellzahl im Knochenmark, begrenzte die Ausbreitung in andere Organe, stellte eine gesündere Blutbildung wieder her und verschob die Immunzellen hin zu einem angreifbereiteren Zustand, besonders in Kombination mit vorhandener Chemotherapie. Zwar sind diese Befunde noch präklinisch, doch sie legen nahe, dass auf SSTNIV modellierte Wirkstoffe eines Tages Patienten helfen könnten, deren Myelom nicht mehr auf aktuelle Therapien anspricht, indem sie ein zentrales Unterstützungssystem des Tumors außer Kraft setzen.
Zitation: Jung, O., Beauvais, D.M., Ibaan, G.L. et al. SSTNIV, a syndecan-1-targeting peptide chimera, reverses immune suppression and inhibits myeloma progression. Sig Transduct Target Ther 11, 175 (2026). https://doi.org/10.1038/s41392-026-02709-1
Schlüsselwörter: multiples Myelom, syndecan-1, Tumormikroumgebung, Peptidtherapie, Immunzellen