Clear Sky Science · zh
通过ERK1/2–Cyclin D1/CDK4/6轴稳定E2F1,抑制BMX克服小细胞肺癌化疗耐药性
这对肺癌患者的重要性
小细胞肺癌是肺癌中致死率最高的类型之一。它在接受化疗后常常初期缩小,但随后以一种不再对治疗敏感的形式强势复发。本研究揭示了肿瘤细胞用来逃避化疗的关键分子“逃生通路”,并提出了一种旨在阻断该通路的新药候选物。通过展示如何重新使顽固肿瘤对标准药物恢复敏感,这项工作为患者带来了更持久治疗选择的希望。
失控的小细胞肺癌的挑战
小细胞肺癌约占肺癌病例的15%,但由于其生长和转移速度快,致死数占比却很高。几十年来,主要治疗仍是铂类化疗联合依托泊苷。许多患者最初反应良好,但大多数肿瘤很快以更难治疗的形式复发,五年生存率仍低于10%。包括免疫疗法在内的新方法仅在晚期患者中带来有限的生存延长。因此,弄清这些肿瘤如何产生化疗耐药性,是该领域最紧迫的问题之一。
肿瘤细胞内的生存开关
研究者将注意力集中在两种在癌细胞内起信号调控作用的蛋白上。一种叫BMX,是一种激酶——通过磷酸化开启或关闭其他蛋白的酶;另一种E2F1,是一种转录因子,控制细胞分裂、DNA修复以及细胞迁移和侵袭的基因。在来自100名患者的样本及多种小细胞肺癌细胞系中,研究团队发现活性BMX与高水平E2F1几乎总是共存,尤其是在已对化疗失去反应的肿瘤中。当细胞暴露于顺铂或依托泊苷等常用药物时,BMX活性和E2F1水平同步上升,而耐药细胞系这两种蛋白的水平显著高于敏感系。
肿瘤内部线路如何保护它免受药物攻击
深入研究表明,BMX如何帮助E2F1保持活性。BMX并不直接与E2F1结合,而是激活一条中继通路——ERK1/2及Cyclin D1/CDK4/6复合体——这些因子在特定位点化学修饰E2F1。这些修饰像保护盔甲,使E2F1更稳定并在细胞核中富集,从而启动促进快速生长、高效DNA修复和细胞迁移的基因。通常,E2F1会被细胞的蛋白回收机制标记并降解。然而在化疗耐药细胞中,BMX信号屏蔽了这种处置系统,使E2F1持续存在,帮助肿瘤细胞在化疗诱导的损伤中存活下来。
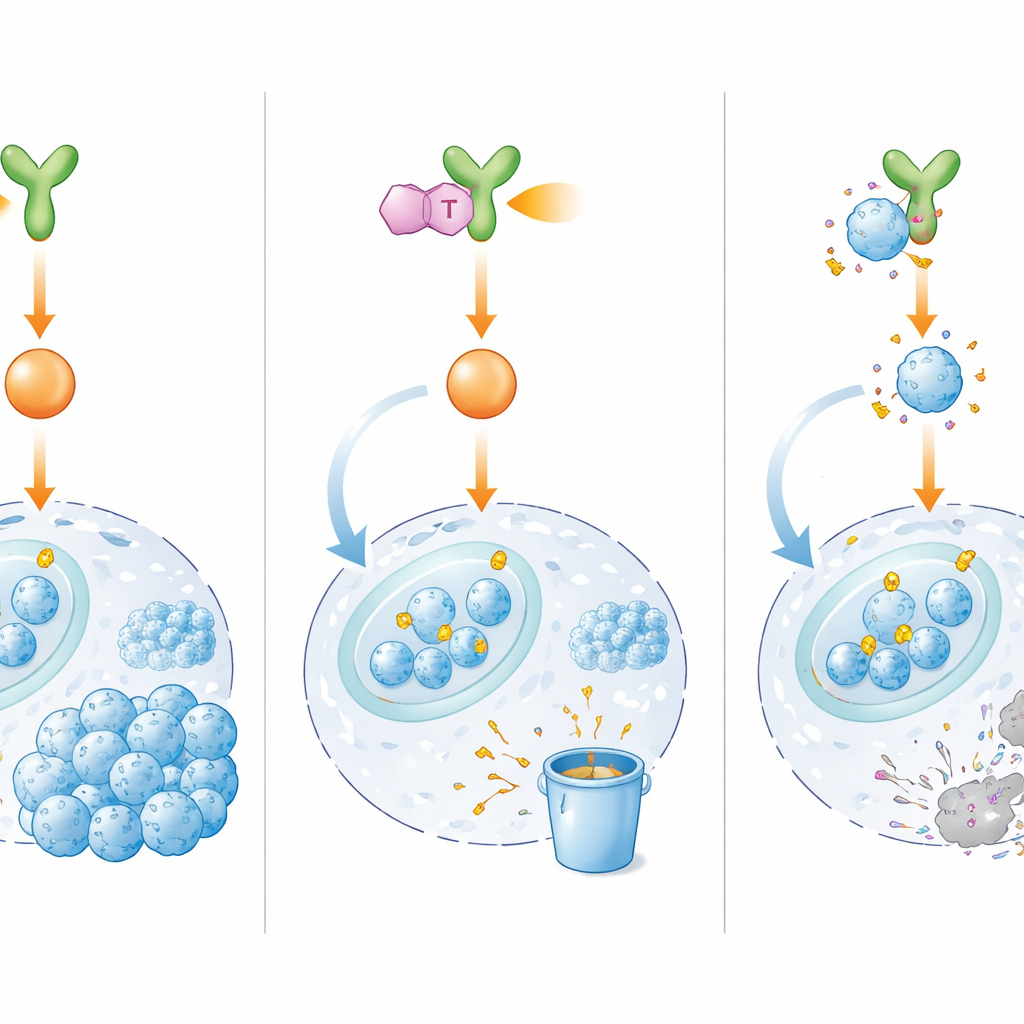
切断开关电源的新药
由于直接靶向E2F1一直很困难,研究者转而阻断其上游控制者BMX。他们从数千种候选分子中筛选出IHMT‑15137,这是一种能强烈且选择性结合BMX并似乎与其不可逆结合的小分子。在实验室测试中,IHMT‑15137抑制了BMX活性并削弱了其下游信号,包括ERK1/2和Cyclin D1/CDK4/6。结果,E2F1失去保护性化学修饰,更多地被标记为待降解并迅速分解。在多种耐药细胞系、患者来源的细胞以及三维小型肿瘤模型中,IHMT‑15137与顺铂联用较单独化疗导致更强的细胞周期阻滞、更严重的DNA损伤、更高的细胞死亡率,以及显著降低的生长、迁移和侵袭能力。
在动物和类患者模型中的获益证据
研究团队随后在携带人源小细胞肺癌移植瘤的小鼠中测试了该联用策略,包含来自化疗复发患者直接取材的肿瘤。在若干独立模型中,将IHMT‑15137加入标准的顺铂‑依托泊苷治疗显著减缓了肿瘤生长,且动物未见明显体重下降或明确的器官损伤。来自治疗组小鼠的肿瘤显示BMX及其信号伙伴活性下降、E2F1水平降低,并伴随更多DNA损伤和凋亡标志。安全性研究表明,IHMT‑15137比早期那些非选择性地也作用于BMX的药物,出血和离靶效应更少,支持其作为化疗的更耐受性搭档的潜力。
这对未来治疗的意义
对非专业读者而言,关键信息是:研究者追踪到小细胞肺癌中的一条重要耐药通路并展示了如何将其关闭。肿瘤细胞通过BMX稳定E2F1这一主要生长调节因子,帮助它们修复化疗造成的损伤并继续分裂。新型抑制剂IHMT‑15137切断了这一路径,使E2F1失稳,从而让长期耐药的肿瘤再次对现有药物变得敏感。尽管该化合物仍需进一步优化并进入人体试验,这项研究为延长和深化对这种侵袭性癌症的化疗反应提供了明确的治疗蓝图。
引用: Wu, T., Qi, S., Shi, C. et al. BMX inhibition overcomes small cell lung cancer chemoresistance by stabilizing E2F1 via ERK1/2-Cyclin D1/CDK4/6 axis. Sig Transduct Target Ther 11, 125 (2026). https://doi.org/10.1038/s41392-026-02644-1
关键词: 小细胞肺癌, 化疗耐药, BMX激酶, E2F1信号通路, 靶向治疗