Clear Sky Science · nl
BMX-remming overwint chemoresistentie bij kleincellige longkanker door E2F1 te stabiliseren via de ERK1/2‑Cyclin D1/CDK4/6‑as
Waarom dit belangrijk is voor mensen met longkanker
Kleincellige longkanker is een van de dodelijkste vormen van longkanker. Vaak krimpt de tumor aanvankelijk na chemotherapie, om vervolgens terug te komen in een vorm die niet meer op de behandeling reageert. Deze studie onthult een belangrijk moleculair "ontsnappingspad" dat tumorcellen gebruiken om chemotherapie te overleven en introduceert een nieuw kandidaat‑geneesmiddel dat dat pad blokkeert. Door te laten zien hoe hardnekkige tumoren opnieuw gevoelig gemaakt kunnen worden voor standaardmedicijnen, wijst het werk op meer duurzame behandelopties voor patiënten.
De uitdaging van razendsnelle kleincellige longkanker
Kleincellige longkanker is verantwoordelijk voor ongeveer 15% van de gevallen van longkanker, maar veroorzaakt een onevenredig groot aantal sterfgevallen omdat de ziekte snel groeit en uitzaait. Decennialang bestond de standaardbehandeling uit een combinatie van platinumhoudende chemotherapie en het middel etoposide. Veel patiënten reageren aanvankelijk goed, maar de meeste tumoren keren snel terug in een moeilijker behandelbare vorm, en de vijfjaarsoverleving blijft onder de 10%. Nieuwere benaderingen, waaronder immunotherapie, hebben het leven van mensen met gevorderde ziekte slechts beperkt verlengd. Begrijpen hoe deze tumoren precies resistent worden tegen chemotherapie is daarom een van de meest urgente vragen in dit vakgebied.
Een overlevingsschakel binnen tumorcellen
De onderzoekers concentreerden zich op twee eiwitten die fungeren als een signaal‑schakelbord binnen kankercellen. Eén, genaamd BMX, is een kinase — een enzym dat andere eiwitten aan‑ of uitzet. De ander, E2F1, is een transcriptiefactor die genen activeert die celdeling, DNA‑herstel en het vermogen van cellen om te migreren en te infiltreren regelen. In monsters van 100 patiënten en in meerdere kleincellige longkanker‑cellijnen vonden de onderzoekers dat actieve BMX en hoge E2F1‑niveaus vrijwel altijd samen voorkwamen, vooral in tumoren die gestopt waren met reageren op chemotherapie. Wanneer cellen werden blootgesteld aan gangbare middelen zoals cisplatine of etoposide, stegen zowel BMX‑activiteit als E2F1‑niveaus synchroon, en chemoresistente cellijnen vertoonden veel hogere concentraties van beide eiwitten dan hun chemogevoelige tegenhangers.
Hoe de interne bedrading van de tumor hem tegen medicijnen beschermt
Dieper gravend onthulden de onderzoekers hoe BMX helpt E2F1 actief te houden. In plaats van direct aan E2F1 te binden, schakelt BMX een relais van andere eiwitten in — ERK1/2 en het Cyclin D1/CDK4/6‑complex — die E2F1 chemisch modificeren op specifieke plaatsen. Deze modificaties werken als beschermende pantserplaten: ze maken E2F1 stabieler en helpen het zich op te hopen in de celkern, waar het genen kan inschakelen voor snelle groei, efficiënt DNA‑herstel en celmigratie. Normaal kan E2F1 worden gemarkeerd voor afbraak door het eiwitafval‑machinerie van de cel. In chemoresistente cellen beschermt BMX‑signalering E2F1 echter tegen dat afbraaksysteem, waardoor het eiwit blijft bestaan en tumorcellen helpt schade door chemotherapie te overleven.
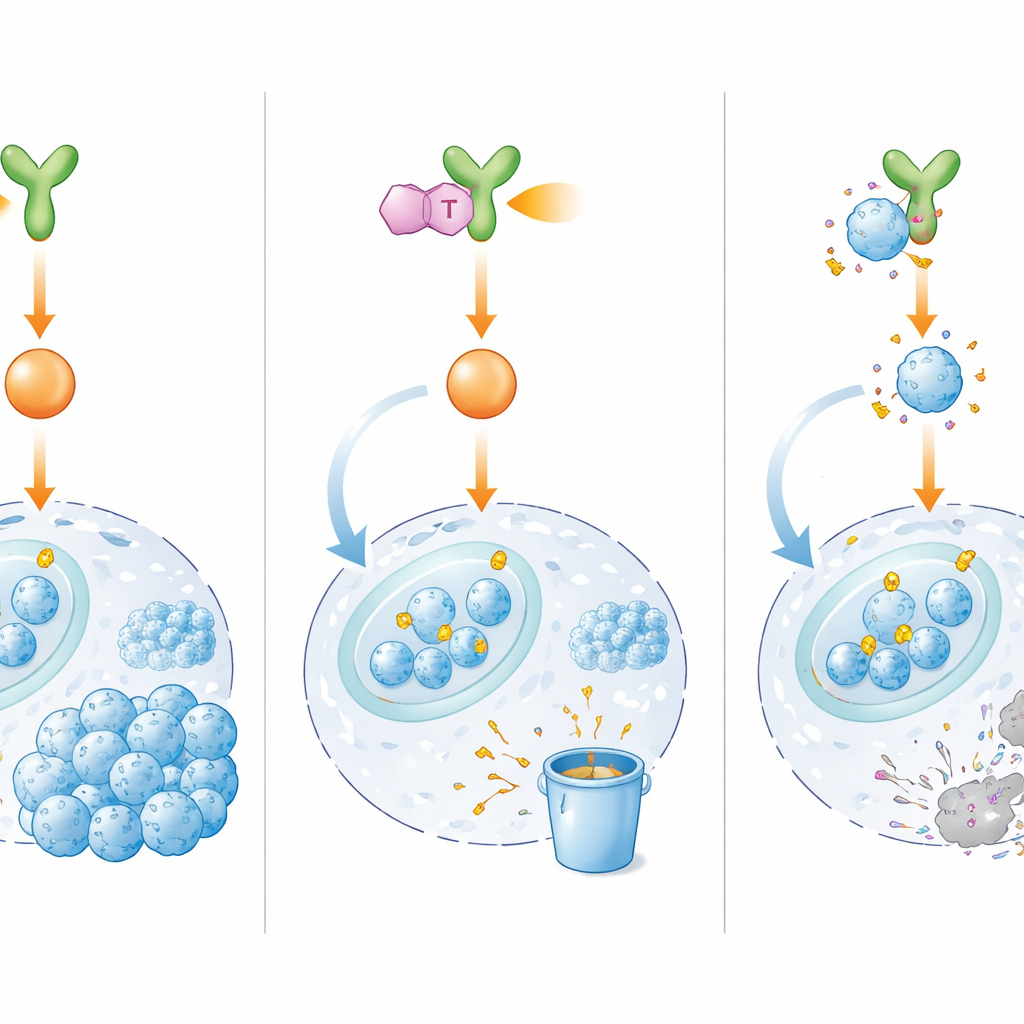
Een nieuw geneesmiddel dat de stroom naar de schakelaar afsluit
Aangezien direct richten op E2F1 moeilijk blijkt, besloten de onderzoekers zijn upstream‑regelaar BMX te blokkeren. Uit duizenden kandidaat‑moleculen identificeerden ze IHMT‑15137, een klein gekoppeld molecuul dat sterk en selectief aan BMX bindt en naar lijkt onomkeerbaar vast te houden. In laboratoriumtesten schakelde IHMT‑15137 BMX‑activiteit uit en dempte het de downstream‑signalen, waaronder ERK1/2 en Cyclin D1/CDK4/6. Daardoor verloor E2F1 zijn beschermende chemische merken, werd het sterker gemarkeerd voor afbraak en snel afgebroken. In meerdere chemoresistente cellijnen, evenals in patiëntafgeleide cellen en driedimensionale mini‑tumoren, leidde de combinatie van IHMT‑15137 met cisplatine tot sterkere celdelingsarrestatie, meer DNA‑schade, hogere sterftecijfers en sterk verminderde groei, migratie en invasie vergeleken met alleen chemotherapie.
Bewijs van voordeel in dier‑ en patiëntachtige modellen
Vervolgens testte het team de combinatie in muizen met humane kleincellige longkanker‑xenografts, inclusief tumoren rechtstreeks afkomstig van patiënten wiens ziekte was teruggekeerd na chemotherapie. In verschillende onafhankelijke modellen vertraagde de toevoeging van IHMT‑15137 aan de standaard cisplatine–etoposide‑therapie de tumorgroei significant zonder substantiële gewichtsverlies of duidelijke orgaanschade bij de dieren. Tumoren van behandelde muizen toonden verminderde activatie van BMX en zijn signaalpartners, lagere E2F1‑niveaus en meer merkers van DNA‑schade en apoptose. Veiligheidsstudies suggereerden dat IHMT‑15137 minder bloedings‑ en off‑target‑effecten heeft dan oudere, minder selectieve middelen die ook BMX remmen, wat zijn potentieel ondersteunt als een beter verdragen partner voor chemotherapie.
Wat dit betekent voor toekomstige behandeling
Voor niet‑specialisten is de kernboodschap dat de onderzoekers een belangrijk resistentiepad in kleincellige longkanker in kaart hebben gebracht en laten zien hoe dat afgesloten kan worden. Tumorcellen gebruiken BMX om E2F1, een meesterregulator van celgroei, te stabiliseren, waardoor ze schade door chemotherapie kunnen herstellen en blijven delen. De nieuwe remmer IHMT‑15137 knipt de stroom naar dit pad door, destabiliseert E2F1 en maakt lang‑resistente tumoren weer kwetsbaar voor bestaande geneesmiddelen. Hoewel deze verbinding verdere optimalisatie en humane proeven nodig heeft, biedt de studie een duidelijk draaiboek voor therapieën die chemotherapie‑responsen bij patiënten met deze agressieve kanker kunnen verlengen en verdiepen.
Bronvermelding: Wu, T., Qi, S., Shi, C. et al. BMX inhibition overcomes small cell lung cancer chemoresistance by stabilizing E2F1 via ERK1/2-Cyclin D1/CDK4/6 axis. Sig Transduct Target Ther 11, 125 (2026). https://doi.org/10.1038/s41392-026-02644-1
Trefwoorden: kleincellige longkanker, chemoresistentie, BMX‑kinase, E2F1‑signalering, gerichte therapie