Clear Sky Science · ar
مثبط BMX يتغلب على مقاومة العلاج الكيميائي في سرطان الرئة صغير الخلايا من خلال استقرار E2F1 عبر محور ERK1/2‑سايكلين D1/CDK4/6
لماذا هذا مهم للأشخاص المصابين بسرطان الرئة
يُعد سرطان الرئة صغير الخلايا أحد أكثر أنواع سرطان الرئة فتكاً. غالباً ما يتقلص في البداية بعد العلاج الكيميائي، ثم يعود بقوة بشكل لم يعد يستجيب للعلاج. تكشف هذه الدراسة عن «طريق هروب» جزيئي رئيسي تستخدمه الخلايا الورمية للبقاء على قيد الحياة بعد العلاج الكيميائي وتقدم مرشح دوائي جديد مصممًا لحظر هذا الطريق. من خلال إظهار كيفية إعادة حساسية الأورام العنيدة للأدوية القياسية، يشير العمل إلى إمكانيات لعلاجات أكثر دوامًا للمرضى.
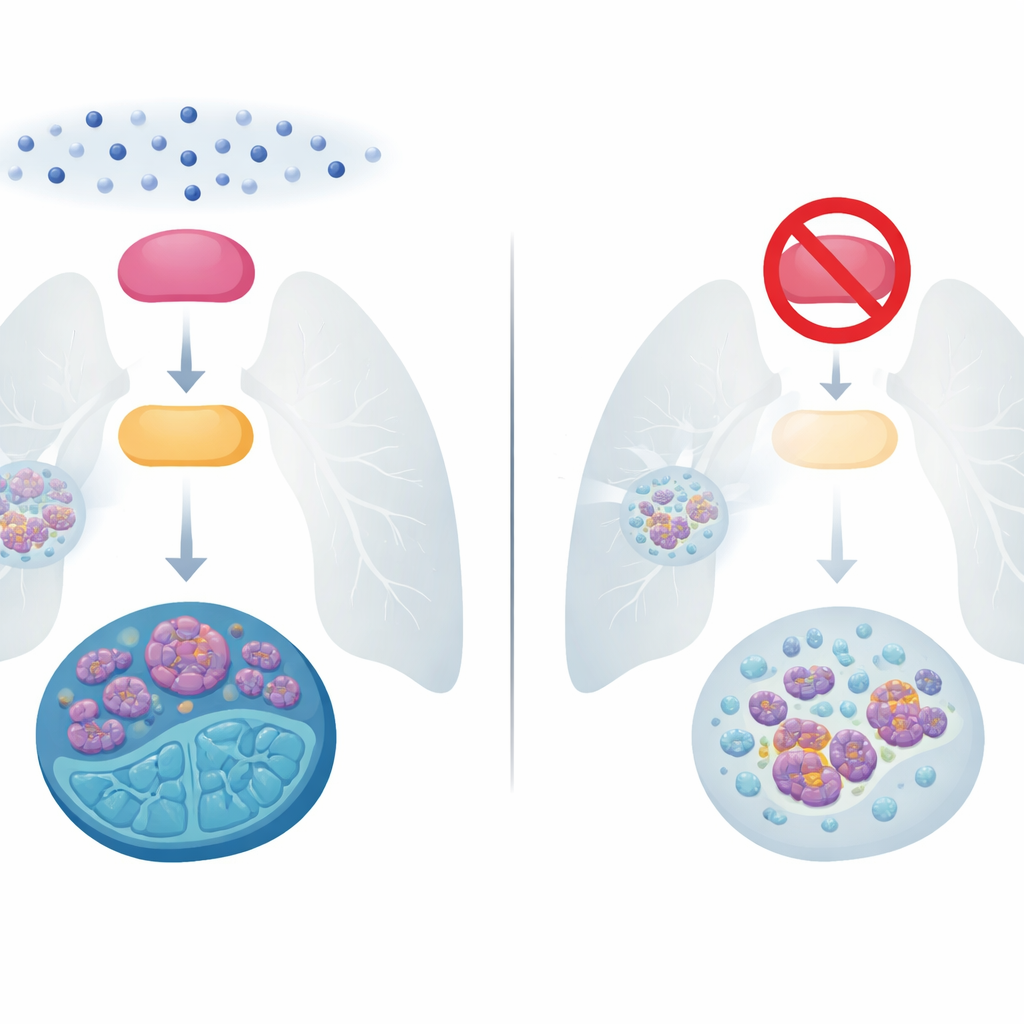
تحدي سرطان الرئة صغير الخلايا المتسارع
يشكل سرطان الرئة صغير الخلايا نحو 15% من حالات سرطان الرئة لكنه يتسبب في نسبة كبيرة من الوفيات لأنه ينمو وينتشر بسرعة. لعقود، كان العلاج الرئيسي هو مزيج من العلاج الكيميائي القائم على البلاتين ودواء الإيتوبوسايد. يستجيب العديد من المرضى في البداية بشكل جيد، لكن معظم الأورام تعود بسرعة بصيغة أصعب علاجًا، ولا تزال نسبة البقاء لخمس سنوات تقل عن 10%. الأساليب الأحدث، بما في ذلك العلاج المناعي، وسعت الحياة بشكل طفيف فقط للمرضى ذوي المرض المتقدم. لذلك، فإن فهم الكيفية التي تصبح بها هذه الأورام مقاومة للعلاج الكيميائي يعد أحد الأسئلة الأكثر إلحاحًا في هذا المجال.
مفتاح بقاء داخل خلايا الورم
ركز الباحثون على بروتينين يعملان بمثابة لوحة تبديل إشارية داخل الخلايا السرطانية. أحدهما، المسمى BMX، هو كيناز — نوع من الإنزيمات الذي يشغّل أو يوقف بروتينات أخرى. والآخر، E2F1، هو عامل نسخ يُشغِّل جينات تتحكم في انقسام الخلايا وإصلاح الحمض النووي وقدرة الخلايا على الحركة والغزو. في عينات من 100 مريض وفي عدة خطوط خلوية لسرطان الرئة صغير الخلايا، وجد الفريق أن نشاط BMX وارتفاع مستويات E2F1 غالبًا ما يسيران معًا، خصوصًا في الأورام التي توقفت عن الاستجابة للعلاج الكيميائي. عندما تعرضت الخلايا لأدوية شائعة مثل السيستبلاتين أو الإيتوبوسايد، ارتفع نشاط BMX ومستويات E2F1 معًا، وأظهرت خطوط الخلايا المقاومة للأدوية مستويات أعلى بكثير من كلا البروتينين مقارنة بنظيراتها الحساسة للأدوية.
كيف تحمي الدوائر الداخلية للورم الخلايا من الأدوية
من خلال تعمق أكبر، كشف الفريق كيف يساعد BMX في إبقاء E2F1 نشطًا. بدلاً من الارتباط المباشر بـ E2F1، يقوم BMX بتشغيل سلسلة من البروتينات الوسيطة — ERK1/2 ومجمع سايكلين D1/CDK4/6 — التي تعدل كيميائيًا E2F1 في مواقع محددة. تعمل هذه التعديلات كدرع واقٍ، فتجعل E2F1 أكثر استقرارًا وتساعده على التراكم في نواة الخلية حيث يمكنه تشغيل جينات للنمو السريع وإصلاح الحمض النووي والهجرة الخلوية. عادةً يمكن وسم E2F1 للهدم بواسطة آليات إعادة تدوير البروتين في الخلية. في الخلايا المقاومة للعقاقير، مع ذلك، تعمل إشارة BMX على حماية E2F1 من هذا النظام، فيستمر وجود البروتين ويساعد خلايا الورم على النجاة من أضرار العلاج الكيميائي.
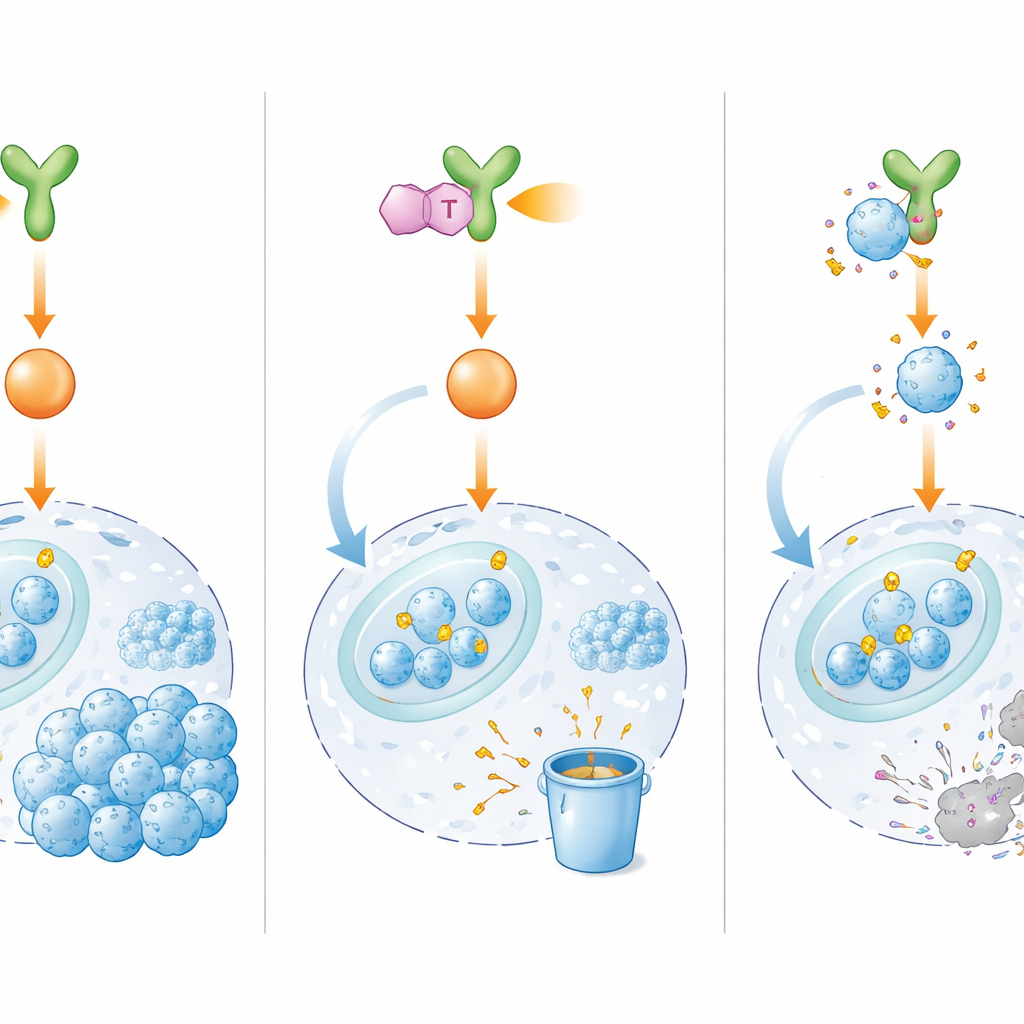
دواء جديد يقطع الطاقة عن لوحة المفاتيح
نظرًا لأن استهداف E2F1 مباشرة ثبت أنه أمر صعب، سعى الباحثون إلى حجب المتحكم الأعلى به، BMX. من بين آلاف الجزيئات المرشحة، حددوا IHMT‑15137، مركبًا صغيرًا يرتبط بقوة وانتقائية بـ BMX ويبدو أنه يتصل به بشكل لا رجعة فيه. في الاختبارات المخبرية، أوقف IHMT‑15137 نشاط BMX وأضعف إشاراته اللاحقة، بما في ذلك ERK1/2 ومجمع سايكلين D1/CDK4/6. نتيجة لذلك، فقد E2F1 علامات الحماية الكيميائية، وزاد وسمه للهدم، وتعرض لتفكك سريع. في عدة خطوط خلوية مقاومة للأدوية، وكذلك في خلايا مشتقة من مرضى وفي أورام مصغرة ثلاثية الأبعاد، أدى الجمع بين IHMT‑15137 والسيستبلاتين إلى توقف أقوى لدورة الخلية، ومزيد من أضرار الحمض النووي، ومعدلات أعلى من موت الخلايا، وانخفاض حاد في النمو والهجرة والغزو مقارنة بالعلاج الكيميائي وحده.
دليل على الفائدة في نماذج حيوانية وشبيهة بالبشر
اختبر الفريق بعد ذلك التركيبة في فئران تحمل زراعات لأورام بشرية من سرطان الرئة صغير الخلايا، بما في ذلك أورام مشتقة مباشرة من مرضى تكرر لديهم المرض بعد العلاج الكيميائي. في عدة نماذج مستقلة، أدى إضافة IHMT‑15137 إلى العلاج القياسي بالسيستبلاتين–الإيتوبوسايد إلى إبطاء نمو الورم بشكل كبير دون التسبب في فقدان وزن كبير أو تلف واضح للأعضاء في الحيوانات. أظهرت الأورام من الفئران المعالجة انخفاضًا في تنشيط BMX وشركائه الإشاريين، وانخفاض مستويات E2F1، وزيادة مؤشرات تلف الحمض النووي والاستماتة. أشارت دراسات السلامة إلى أن IHMT‑15137 له آثار نزف وآثار جانبية خارج الهدف أقل من الأدوية الأقدم الأقل انتقائية التي تستهدف BMX أيضًا، مما يدعم احتمالية كونه شريكًا أكثر تحملاً للعلاج الكيميائي.
ماذا يعني هذا للعلاج المستقبلي
بالنسبة لغير المتخصص، الرسالة الأساسية هي أن الباحثين تتبعوا مسار مقاومة رئيسي في سرطان الرئة صغير الخلايا وأظهروا كيفية إغلاقه. تستخدم خلايا الورم BMX لاستقرار E2F1، وهو منظم نمو رئيسي، مما يساعدها على إصلاح الضرر الناجم عن العلاج الكيميائي ومواصلة الانقسام. يقطع المثبط الجديد IHMT‑15137 الطاقة عن هذا المسار، فيزعزع استقرار E2F1 ويجعل الأورام المقاومة منذ زمن طويل عرضة مرة أخرى للأدوية الحالية. على الرغم من أن هذا المركب سيحتاج إلى تحسينات إضافية وتجارب على البشر، فإن الدراسة تقدم مخططًا واضحًا لعلاجات يمكن أن تطيل وتعمق استجابات العلاج الكيميائي للمرضى المصابين بهذا السرطان العدواني.
الاستشهاد: Wu, T., Qi, S., Shi, C. et al. BMX inhibition overcomes small cell lung cancer chemoresistance by stabilizing E2F1 via ERK1/2-Cyclin D1/CDK4/6 axis. Sig Transduct Target Ther 11, 125 (2026). https://doi.org/10.1038/s41392-026-02644-1
الكلمات المفتاحية: سرطان الرئة صغير الخلايا, مقاومة العلاج الكيميائي, كيناز BMX, إشارة E2F1, علاج موجه