Clear Sky Science · de
BMX‑Hemmung überwindet Chemoresistenz beim kleinzelligen Lungenkrebs, indem E2F1 über die ERK1/2-Cyclin D1/CDK4/6-Achse stabilisiert wird
Warum das für Menschen mit Lungenkrebs wichtig ist
Kleinzelliger Lungenkrebs gehört zu den tödlichsten Formen von Lungenkrebs. Er spricht oft zunächst auf Chemotherapie an, kehrt dann jedoch in einer Form zurück, die nicht mehr auf die Behandlung reagiert. Diese Studie deckt eine zentrale molekulare „Fluchtroute“ auf, die Tumorzellen nutzen, um Chemotherapie zu überleben, und stellt einen neuen Wirkstoffkandidaten vor, der diese Route blockieren soll. Indem gezeigt wird, wie widerstandsfähige Tumoren wieder empfindlich für Standardmedikamente gemacht werden können, weist die Arbeit auf potenziell dauerhaftere Behandlungsoptionen für Patientinnen und Patienten hin.
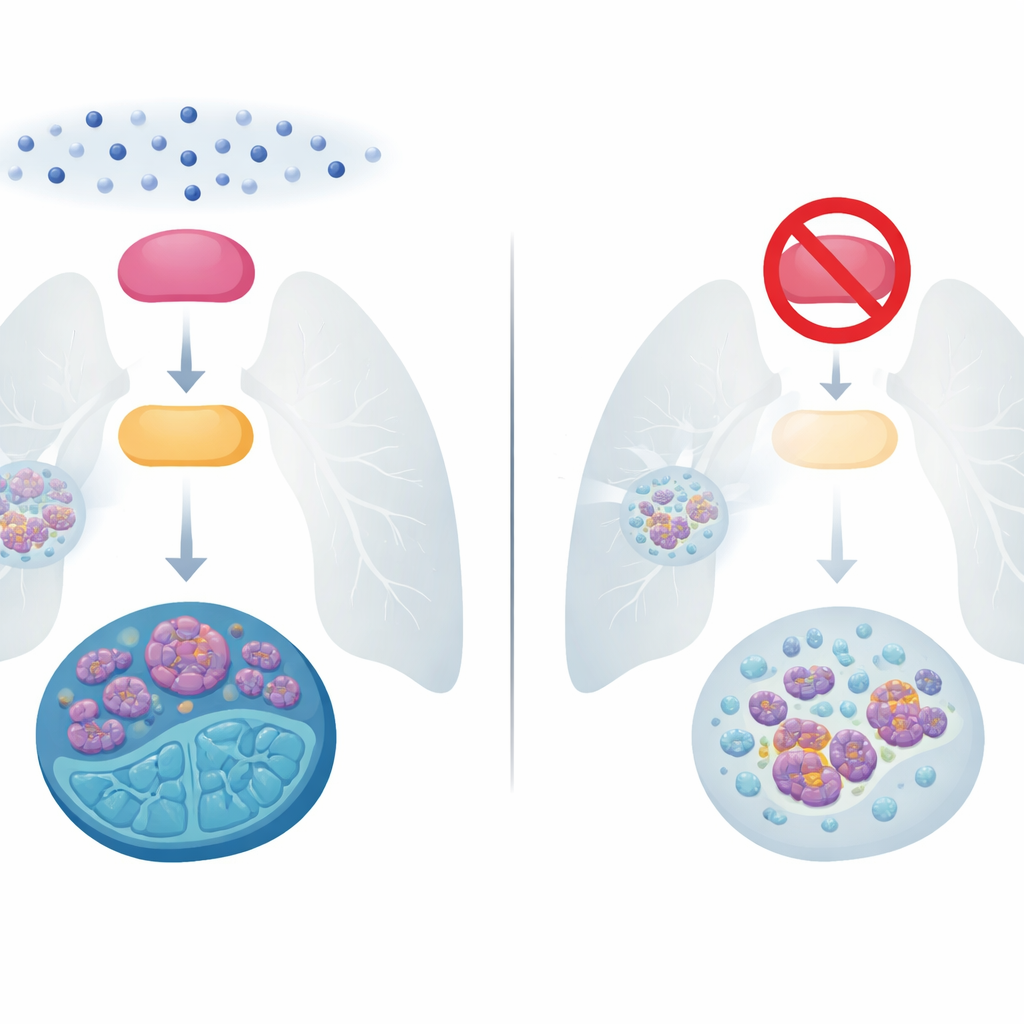
Die Herausforderung des unkontrollierten kleinzelligen Lungenkrebses
Kleinzelliger Lungenkrebs macht etwa 15 % aller Lungenkrebsfälle aus, verursacht aber einen unverhältnismäßig großen Anteil der Todesfälle, weil er schnell wächst und streut. Jahrzehntelang bestand die Standardtherapie aus einer Kombination aus platinhaltiger Chemotherapie und dem Wirkstoff Etoposid. Viele Patientinnen und Patienten sprechen zunächst gut an, doch die meisten Tumoren kehren bald in einer schwerer zu behandelnden Form zurück, und die Fünfjahresüberlebensrate liegt weiterhin unter 10 %. Neuere Ansätze, darunter Immuntherapien, haben das Leben bei fortgeschrittener Erkrankung nur moderat verlängert. Deshalb zählt das Verständnis, wie diese Tumoren Chemotherapie‑Resistenz entwickeln, zu den dringendsten Fragen in diesem Bereich.
Ein Überlebensschalter im Inneren der Tumorzellen
Die Forschenden konzentrierten sich auf zwei Proteine, die innerhalb der Krebszellen wie eine Schaltzentrale wirken. Das eine, BMX, ist eine Kinase – ein Enzym, das andere Proteine an- oder ausschaltet. Das andere, E2F1, ist ein Transkriptionsfaktor, der Gene aktiviert, die Zellteilung, DNA‑Reparatur sowie Bewegungs‑ und Invasionsfähigkeit steuern. In Proben von 100 Patientinnen und Patienten und in mehreren kleinzelligen Lungenkrebszelllinien fanden die Forschenden, dass aktive BMX‑Signale und hohe E2F1‑Spiegel fast immer zusammen auftraten, besonders in Tumoren, die nicht mehr auf Chemotherapie reagierten. Bei Exposition gegenüber gängigen Medikamenten wie Cisplatin oder Etoposid stiegen BMX‑Aktivität und E2F1‑Level synchron an, und chemoresistente Zelllinien zeigten deutlich höhere Mengen beider Proteine als ihre medikamentenempfindlichen Gegenstücke.
Wie die innere Verkabelung des Tumors ihn vor Medikamenten schützt
Bei tieferer Untersuchung enthüllte das Team, wie BMX E2F1 aktiv hält. BMX bindet nicht direkt an E2F1, sondern schaltet eine Kaskade anderer Proteine ein – ERK1/2 und den Cyclin D1/CDK4/6‑Komplex –, die E2F1 an spezifischen Stellen chemisch modifizieren. Diese Modifikationen wirken wie eine schützende Rüstung, machen E2F1 stabiler und begünstigen seine Anreicherung im Zellkern, wo es Gene für schnelles Wachstum, effiziente DNA‑Reparatur und Zellmigration aktivieren kann. Normalerweise kann E2F1 zur Zerstörung durch das zelluläre Proteinfaltungs‑ und Recycling‑System markiert werden. In chemoresistenten Zellen jedoch schützt das BMX‑Signal E2F1 vor diesem Abbausystem, sodass das Protein persistent bleibt und den Tumorzellen hilft, Schäden durch Chemotherapie zu überleben.
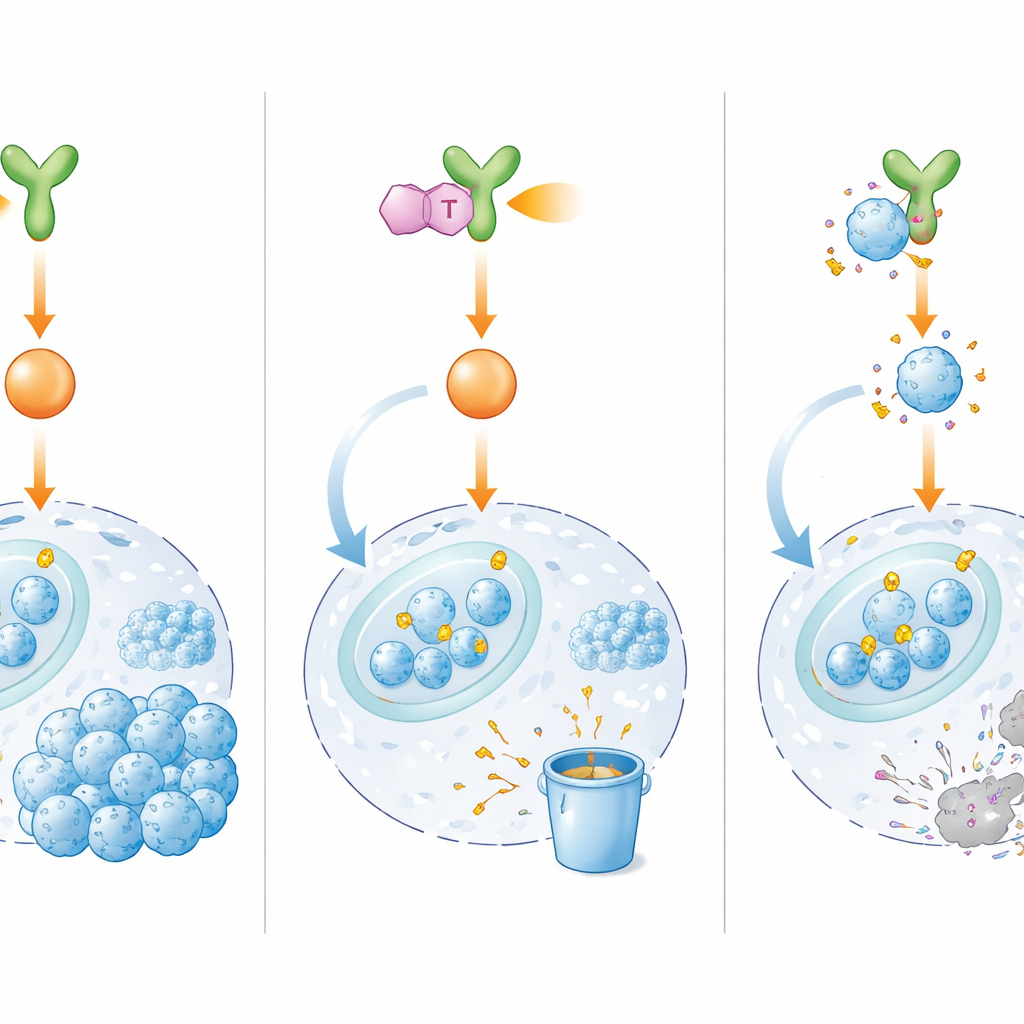
Ein neues Medikament, das den Schalter abschaltet
Da eine direkte Ansteuerung von E2F1 schwierig ist, suchten die Forschenden danach, seinen upstream‑Kontrolleur BMX zu blockieren. Aus tausenden Kandidaten identifizierten sie IHMT‑15137, eine kleine Verbindung, die stark und selektiv an BMX bindet und offenbar irreversibel an dieses anknüpft. In Labortests schaltete IHMT‑15137 die BMX‑Aktivität aus und dämpfte seine downstream‑Signale, darunter ERK1/2 und Cyclin D1/CDK4/6. Infolgedessen verlor E2F1 seine schützenden chemischen Markierungen, wurde verstärkt für den Abbau markiert und rasch abgebaut. In mehreren medikamentenresistenten Zelllinien sowie in patientenabgeleiteten Zellen und dreidimensionalen Mini‑Tumoren führte die Kombination von IHMT‑15137 mit Cisplatin zu stärkerer Zellzyklusarretierung, mehr DNA‑Schäden, höheren Sterberaten und deutlich reduzierter Proliferation, Migration und Invasion im Vergleich zur Chemotherapie allein.
Nutzennachweis in Tier‑ und patientenähnlichen Modellen
Das Team testete die Kombination anschließend an Mäusen mit humanen kleinzelligen Lungenkrebs‑Grafts, einschließlich Tumoren, die direkt von Patientinnen und Patienten stammten, deren Erkrankung nach Chemotherapie rezidiviert war. In mehreren unabhängigen Modellen verlangsamte die Zugabe von IHMT‑15137 zur Standardtherapie aus Cisplatin und Etoposid das Tumorwachstum signifikant, ohne dass die Tiere deutlich an Gewicht verloren oder offensichtliche Organschäden zeigten. Tumoren aus behandelten Mäusen zeigten reduzierte Aktivierung von BMX und seinen Signalpartnern, niedrigere E2F1‑Spiegel sowie mehr Marker für DNA‑Schäden und Apoptose. Sicherheitsstudien deuteten darauf hin, dass IHMT‑15137 weniger Blutungs‑ und Off‑Target‑Effekte verursacht als ältere, weniger selektive Wirkstoffe, die ebenfalls BMX treffen, was seine Eignung als besser verträglicher Partner für Chemotherapie stützt.
Was das für die zukünftige Behandlung bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft, dass die Forschenden einen wichtigen Resistenzweg beim kleinzelligen Lungenkrebs nachverfolgt und gezeigt haben, wie er ausgeschaltet werden kann. Tumorzellen nutzen BMX, um E2F1 zu stabilisieren – einen zentralen Wachstumskontrolleur – und unterstützen damit die Reparatur durch Chemotherapie verursachter Schäden und das weitere Teilen. Der neue Inhibitor IHMT‑15137 kappt die Energiezufuhr zu diesem Weg, destabilisiert E2F1 und macht seit langem resistente Tumoren wieder anfällig für bestehende Medikamente. Zwar muss diese Verbindung noch optimiert und in klinischen Studien am Menschen geprüft werden, doch die Studie liefert eine klare Blaupause für Therapien, die Chemotherapieantworten bei Patientinnen und Patienten mit diesem aggressiven Krebs verlängern und vertiefen könnten.
Zitation: Wu, T., Qi, S., Shi, C. et al. BMX inhibition overcomes small cell lung cancer chemoresistance by stabilizing E2F1 via ERK1/2-Cyclin D1/CDK4/6 axis. Sig Transduct Target Ther 11, 125 (2026). https://doi.org/10.1038/s41392-026-02644-1
Schlüsselwörter: kleinzelliger Lungenkrebs, Chemoresistenz, BMX‑Kinasen, E2F1‑Signalweg, zielgerichtete Therapie