Clear Sky Science · tr
BMX inhibisyonu, ERK1/2‑Siklin D1/CDK4/6 ekseni yoluyla E2F1’i stabilize ederek küçük hücreli akciğer kanserinde kemorezistansı yener
Akciğer kanseri olan kişiler için bunun önemi
Küçük hücreli akciğer kanseri, akciğer kanserlerinin en ölümcül türlerinden biridir. Çoğu kez kemoterapiye ilk başta küçülerek yanıt verir, ancak daha sonra tedaviye yanıt vermeyen bir biçimde şiddetlenerek geri döner. Bu çalışma, tümör hücrelerinin kemoterapiden kaçmak için kullandığı temel moleküler “kaçış yolunu” ortaya çıkarıyor ve bu yolu bloke etmeye yönelik yeni bir ilaç adayını tanıtıyor. İnatçı tümörleri standart ilaçlara yeniden duyarlı hale getirmenin yollarını göstererek, hastalar için daha kalıcı tedavi seçeneklerine işaret ediyor.
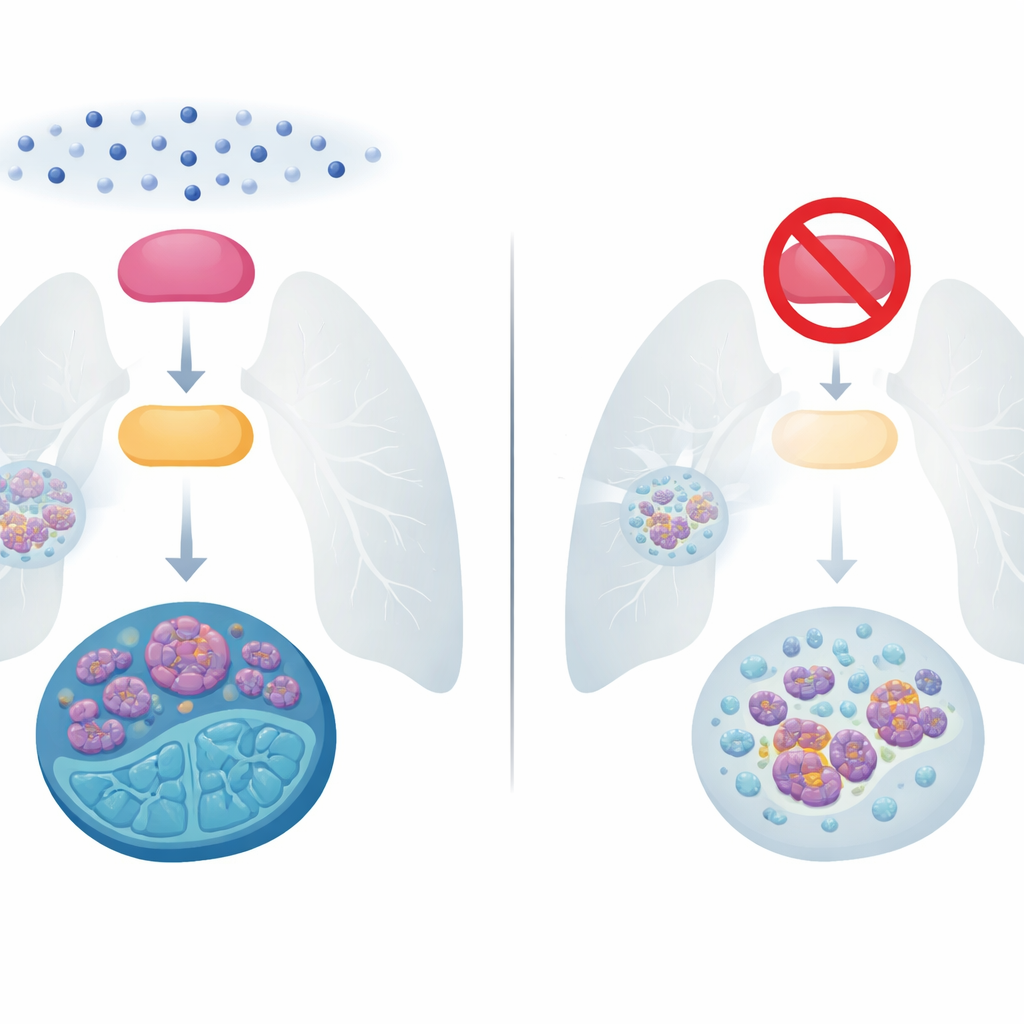
Kontrolden çıkan küçük hücreli akciğer kanserinin zorluğu
Küçük hücreli akciğer kanseri, akciğer kanseri vakalarının yaklaşık %15’ini oluşturur ancak hızla büyüyüp yayıldığı için orantısız bir ölüm oranına yol açar. On yıllardır ana tedavi, platin içeren kemoterapi ile etoposid kombinasyonudur. Birçok hasta başlangıçta iyi yanıt verir, ancak çoğu tümör kısa sürede daha zor tedavi edilen bir biçimde geri döner ve beş yıllık sağkalım oranı hâlâ %10’un altındadır. İmmünoterapi gibi daha yeni yaklaşımlar, ileri evre hastalarda yaşam süresini yalnızca sınırlı ölçüde uzatmıştır. Bu nedenle bu tümörlerin kemoterapiye nasıl direnç kazandığını tam olarak anlamak alandaki en acil sorulardan biridir.
Tümör hücreleri içinde bir hayatta kalma anahtarı
Araştırmacılar, kanser hücreleri içinde bir sinyal anahtar tahtası gibi işleyen iki proteine odaklandı. Bunlardan biri BMX adındaki bir kinaz—diğer proteinleri açıp kapatan bir enzim türü. Diğeri E2F1 ise hücre bölünmesini, DNA onarımını ve hücre göçü ile istila yeteneğini kontrol eden genleri etkinleştiren bir transkripsiyon faktörüdür. 100 hastadan alınan örneklerde ve birçok küçük hücreli akciğer kanseri hücre hattında ekip, aktif BMX ile yüksek E2F1 düzeylerinin neredeyse her zaman birlikte olduğunu, özellikle de kemoterapiye yanıt vermeyi bırakan tümörlerde bu ilişkinin güçlü olduğunu buldu. Hücreler sisplatin veya etoposid gibi yaygın ilaçlara maruz kaldığında hem BMX aktivitesi hem de E2F1 düzeyleri birlikte yükseldi ve ilaç‑dirençli hücre hatları, ilaç‑duyarlı muadillerine göre her iki proteinin de çok daha yüksek seviyelerini gösterdi.
Tümörün iç devreleri ilaca karşı nasıl koruma sağlar
Daha derine inince ekip, BMX’in E2F1’in aktif kalmasına nasıl yardımcı olduğunu açığa çıkardı. BMX doğrudan E2F1’e bağlanmak yerine, E2F1’i belirli pozisyonlarda kimyasal olarak değiştiren başka proteinlerin—ERK1/2 ve Siklin D1/CDK4/6 kompleksinin—bir rölesini etkinleştiriyor. Bu değişiklikler koruyucu bir zırh gibi davranarak E2F1’i daha stabil kılıyor ve hücre çekirdeğinde birikmesine yardımcı oluyor; burada hızlı büyüme, etkili DNA onarımı ve hücre göçü için genleri açabiliyor. Normalde E2F1, hücrenin protein geri dönüşüm mekanizması tarafından yıkım için işaretlenebilir. Ancak kemorezistan hücrelerde BMX sinyalleşmesi E2F1’i bu tasfiye sisteminden koruyor, böylece protein kalıcı hale geliyor ve tümör hücrelerinin kemoterapinin yol açtığı hasardan kurtulmasına yardımcı oluyor.
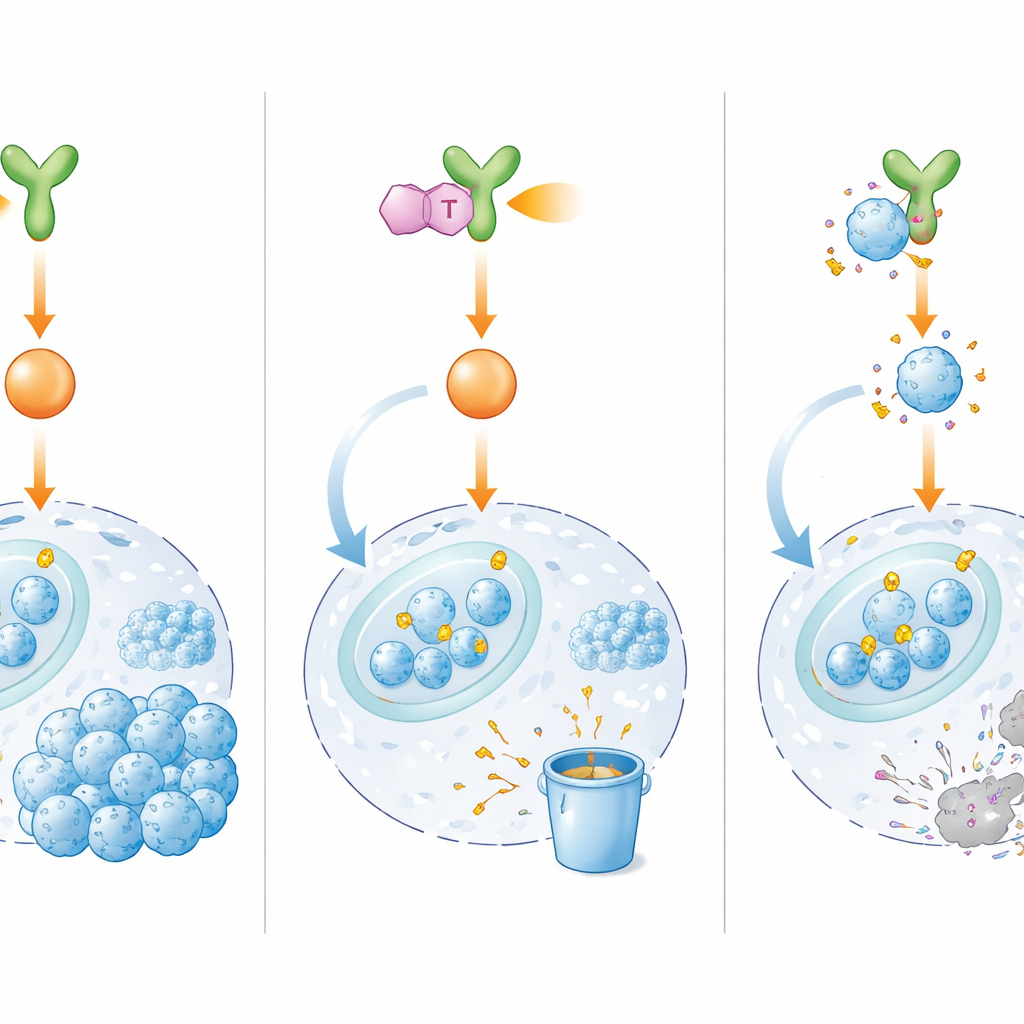
Anahtarı kesen yeni bir ilaç
E2F1’i doğrudan hedeflemenin zor olduğu düşünüldüğü için araştırmacılar onun yukarı akış kontrolörü BMX’i bloke etmeye karar verdi. Binlerce aday molekül arasından BMX’e güçlü ve seçici şekilde bağlanan ve görünüşe göre geri döndürülemez biçimde tutunan IHMT‑15137 adlı küçük bir bileşen belirlendi. Laboratuvar testlerinde IHMT‑15137 BMX aktivitesini kapattı ve ERK1/2 ile Siklin D1/CDK4/6 dahil olmak üzere aşağı akış sinyallerini zayıflattı. Sonuç olarak E2F1 koruyucu kimyasal işaretlerini kaybetti, yıkım için daha fazla işaretlendi ve hızla parçalandı. Çoklu ilaç‑dirençli hücre hatlarında, hasta kökenli hücrelerde ve üç boyutlu mini‑tümör modellerinde IHMT‑15137 ile cisplatin kombinasyonu, tek başına kemoterapiye kıyasla daha güçlü hücre döngüsü durması, daha fazla DNA hasarı, daha yüksek hücre ölümü oranları ve hızla azalan büyüme, göç ve invazyon sağladı.
Hayvan ve hasta‑benzeri modellerde fayda kanıtı
Ekip daha sonra kombinasyonu, hastalığı kemoterapi sonrası nüks etmiş hastalardan elde edilen tümörler de dahil olmak üzere insan küçük hücreli akciğer kanseri greftleri taşıyan farelerde test etti. Birkaç bağımsız modelde, IHMT‑15137’in standart sisplatin–etoposid tedavisine eklenmesi tümör büyümesini anlamlı şekilde yavaşlattı; hayvanlarda belirgin kilo kaybı veya açık organ hasarı oluşturmadı. Tedavi edilen farelerin tümörlerinde BMX ve sinyal ortaklarının aktivasyonunun azaldığı, E2F1 düzeylerinin düşürüldüğü ve daha fazla DNA hasarı ile apoptosis belirteçlerinin arttığı görüldü. Güvenlik çalışmaları, IHMT‑15137’in BMX’i hedefleyen daha eski, daha az seçici ilaçlara kıyasla daha az kanama ve hedef dışı etkiye sahip olabileceğini göstererek kemoterapi için daha tolere edilebilir bir eş aday olma potansiyelini destekledi.
Gelecekteki tedavi için ne anlama geliyor
Bir uzman olmayan için ana mesaj, araştırmacıların küçük hücreli akciğer kanserinde büyük bir direnç yolunu izledikleri ve bunu nasıl kapatacaklarını gösterdikleridir. Tümör hücreleri, E2F1’i stabilize etmek için BMX’i kullanıyor; bu ana büyüme düzenleyicisi, hücrelerin kemoterapinin yol açtığı hasarı onarmasına ve bölünmeye devam etmesine yardımcı oluyor. Yeni inhibitör IHMT‑15137 bu yolun gücünü kesiyor, E2F1’i destabilize ediyor ve uzun süredir dirençli kalan tümörleri mevcut ilaçlara karşı yeniden hassas hale getiriyor. Bu bileşik daha fazla optimizasyon ve insan deneyleri gerektirecek olsa da çalışma, bu agresif kanserle mücadelede kemoterapi yanıtlarını uzatıp derinleştirebilecek tedaviler için açık bir yol haritası sunuyor.
Atıf: Wu, T., Qi, S., Shi, C. et al. BMX inhibition overcomes small cell lung cancer chemoresistance by stabilizing E2F1 via ERK1/2-Cyclin D1/CDK4/6 axis. Sig Transduct Target Ther 11, 125 (2026). https://doi.org/10.1038/s41392-026-02644-1
Anahtar kelimeler: küçük hücreli akciğer kanseri, kemorezistans, BMX kinazı, E2F1 sinyalleşmesi, hedefe yönelik tedavi