Clear Sky Science · pl
Hamowanie BMX przezwycięża odporność drobnokomórkowego raka płuca na chemioterapię przez stabilizację E2F1 via osi ERK1/2-Cyklina D1/CDK4/6
Dlaczego to ma znaczenie dla osób z rakiem płuca
Drobnokomórkowy rak płuca jest jedną z najbardziej śmiertelnych postaci raka płuca. Często początkowo ustępuje po zastosowaniu chemioterapii, by następnie powrócić w formie, która już nie reaguje na leczenie. Badanie to odkrywa kluczową molekularną „drogę ucieczki”, której komórki nowotworowe używają, by przetrwać chemioterapię, i wprowadza nowy kandydat na lek zaprojektowany, by zablokować tę drogę. Pokazując, jak ponownie uczulić oporne guzy na standardowe leki, praca ta wskazuje kierunek do trwalszych opcji leczenia dla pacjentów.
Problem wymykającego się spod kontroli drobnokomórkowego raka płuca
Drobnokomórkowy rak płuca stanowi około 15% przypadków raka płuca, ale odpowiada za nieproporcjonalnie dużo zgonów, ponieważ rośnie i daje przerzuty bardzo szybko. Przez dziesięciolecia podstawowym leczeniem była kombinacja chemioterapii opartej na platynie i etopozydu. Wielu pacjentów początkowo dobrze reaguje, ale większość guzów wkrótce nawraca w formie trudniejszej do leczenia, a pięcioletnie przeżycie nadal wynosi poniżej 10%. Nowsze podejścia, w tym immunoterapia, tylko nieznacznie wydłużyły życie osób z zaawansowaną chorobą. Zrozumienie, w jaki sposób te guzy stają się odporne na chemioterapię, jest więc jednym z najpilniejszych pytań w tej dziedzinie.
Włącznik przeżycia wewnątrz komórek nowotworowych
Naukowcy skupili się na dwóch białkach, które działają jak wewnętrzny panel sygnalizacyjny w komórkach nowotworowych. Jedno, o nazwie BMX, jest kinazą — rodzajem enzymu, który włącza lub wyłącza inne białka. Drugie, E2F1, to czynnik transkrypcyjny, który włącza geny kontrolujące podział komórek, naprawę DNA oraz zdolność komórek do przemieszczania się i inwazji. W próbkach od 100 pacjentów oraz w wielu liniach komórkowych drobnokomórkowego raka płuca zespół stwierdził, że aktywny BMX i wysokie poziomy E2F1 niemal zawsze występowały razem, zwłaszcza w guzach, które przestały reagować na chemioterapię. Po ekspozycji komórek na powszechnie stosowane leki, takie jak cisplatyna czy etopozyd, aktywność BMX i poziomy E2F1 rosły równolegle, a linie komórek odpornych na leki wykazywały znacznie wyższe poziomy obu białek niż ich wrażliwe odpowiedniki.
Jak wewnętrzne okablowanie guza chroni go przed lekami
Zanurzając się głębiej, zespół wyjaśnił, jak BMX pomaga utrzymać aktywność E2F1. Zamiast wiązać się bezpośrednio z E2F1, BMX uruchamia przekaźnik innych białek — ERK1/2 oraz kompleks Cyklina D1/CDK4/6 — które chemicznie modyfikują E2F1 w określonych miejscach. Te modyfikacje działają jak pancerz ochronny, czyniąc E2F1 bardziej stabilnym i pomagając mu gromadzić się w jądrze komórkowym, gdzie może włączać geny odpowiadające za szybki wzrost, efektywną naprawę DNA i migrację komórek. Normalnie E2F1 może być oznaczany do zniszczenia przez komórkowe mechanizmy recyklingu białek. W komórkach opornych na chemioterapię sygnalizacja BMX chroni jednak E2F1 przed tym systemem utylizacji, więc białko utrzymuje się i pomaga komórkom nowotworowym przetrwać uszkodzenia wywołane chemioterapią.
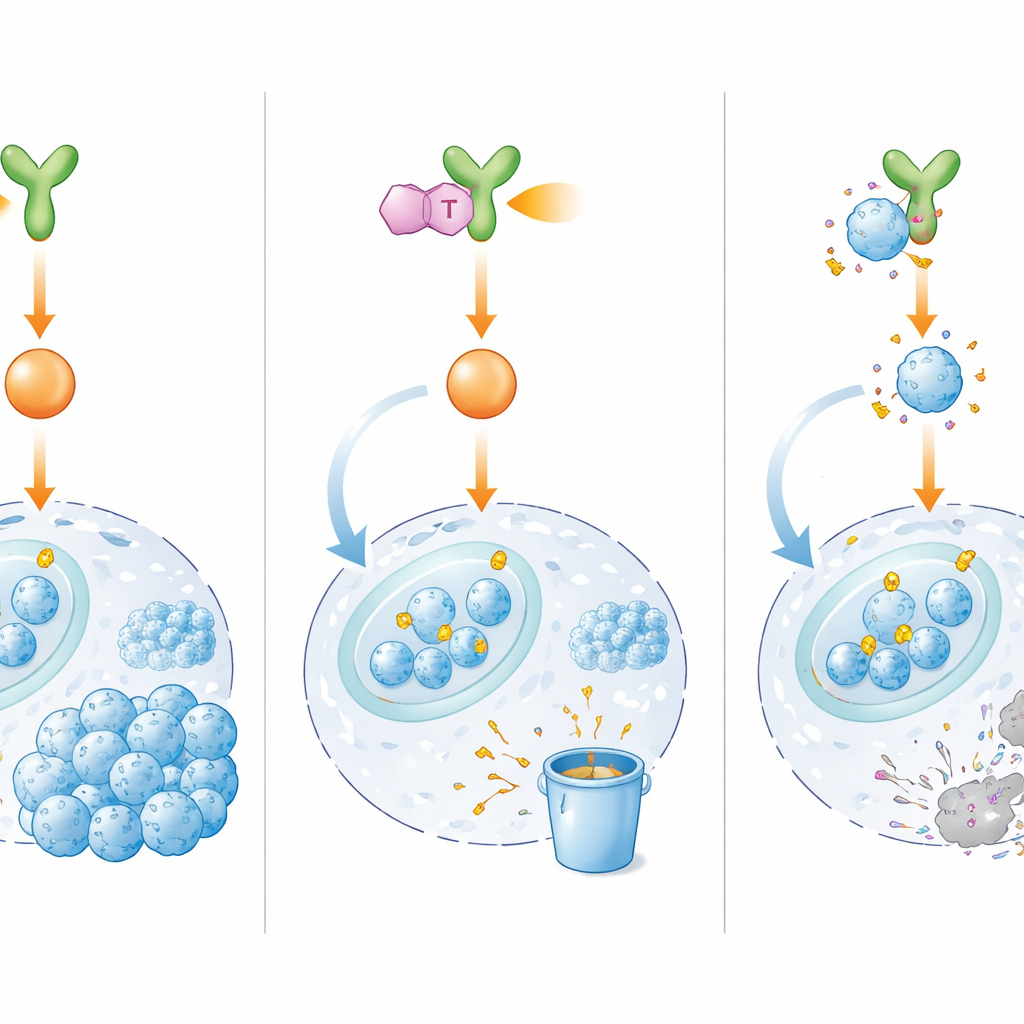
Nowy lek odcinający zasilanie włącznika
Ponieważ bezpośrednie celowanie w E2F1 okazało się trudne, badacze postanowili zablokować jego nadrzędnego regulatora, BMX. Spośród tysięcy kandydatów wyłonili IHMT-15137, małą cząsteczkę, która silnie i selektywnie wiąże się z BMX i wydaje się robić to nieodwracalnie. W testach laboratoryjnych IHMT-15137 wyłączał aktywność BMX i tłumił jego sygnały zstępujące, w tym ERK1/2 i Cyklinę D1/CDK4/6. W rezultacie E2F1 utracił ochronne modyfikacje chemiczne, stał się silniej oznaczany do zniszczenia i był szybko degradowany. W wielu liniach komórek opornych na leki, a także w komórkach pochodzących od pacjentów i trójwymiarowych mini‑guzach, połączenie IHMT-15137 z cisplatiną prowadziło do silniejszego zatrzymania cyklu komórkowego, większych uszkodzeń DNA, wyższych wskaźników śmierci komórek oraz zdecydowanego zahamowania wzrostu, migracji i inwazji w porównaniu z samą chemioterapią.
Dowód korzyści w modelach zwierzęcych i przypominających pacjenta
Zespół następnie przetestował kombinację u myszy z wszczepionymi ludzkimi przeszczepami drobnokomórkowego raka płuca, w tym guzami bezpośrednio pochodzącymi od pacjentów, których choroba nawrociła po chemioterapii. W kilku niezależnych modelach dodanie IHMT-15137 do standardowej terapii cisplatyna–etopozyd znacząco spowolniło wzrost guzów bez powodowania istotnej utraty masy ciała ani ewidentnych uszkodzeń narządów u zwierząt. Guzy z leczonych myszy wykazywały zmniejszoną aktywację BMX i jego współpracowników sygnałowych, niższe poziomy E2F1 oraz więcej markerów uszkodzeń DNA i apoptozy. Badania bezpieczeństwa sugerowały, że IHMT-15137 powoduje mniej krwawień i efektów pozacelowych niż starsze, mniej selektywne leki uderzające również w BMX, co wspiera jego potencjał jako lepiej tolerowanego partnera dla chemioterapii.
Co to oznacza dla przyszłego leczenia
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że badacze zmapowali główną ścieżkę oporności w drobnokomórkowym raku płuca i pokazali, jak ją zamknąć. Komórki nowotworowe używają BMX do stabilizacji E2F1, głównego regulatora wzrostu, co pomaga im naprawiać uszkodzenia wywołane chemioterapią i nadal się dzielić. Nowy inhibitor IHMT-15137 odcina zasilanie tej ścieżki, destabilizuje E2F1 i ponownie czyni długo oporne guzy wrażliwymi na istniejące leki. Choć związek ten będzie wymagał dalszej optymalizacji i badań u ludzi, badanie dostarcza wyraźnego planu dla terapii, które mogłyby wydłużyć i pogłębić odpowiedzi na chemioterapię u pacjentów z tym agresywnym nowotworem.
Cytowanie: Wu, T., Qi, S., Shi, C. et al. BMX inhibition overcomes small cell lung cancer chemoresistance by stabilizing E2F1 via ERK1/2-Cyclin D1/CDK4/6 axis. Sig Transduct Target Ther 11, 125 (2026). https://doi.org/10.1038/s41392-026-02644-1
Słowa kluczowe: drobnokomórkowy rak płuca, odporność na chemioterapię, kinaza BMX, sygnalizacja E2F1, terapia celowana