Clear Sky Science · sv
BMX‑hämning övervinner kemoresistens vid småcellig lungcancer genom att stabilisera E2F1 via ERK1/2‑Cyclin D1/CDK4/6‑axeln
Varför detta är viktigt för personer med lungcancer
Småcellig lungcancer är en av de dödligaste formerna av lungcancer. Den krymper ofta initialt vid kemoterapi för att sedan komma tillbaka i en form som inte längre svarar på behandlingen. Denna studie avslöjar en viktig molekylär ”flyktrutt” som tumörceller använder för att överleva kemoterapi och introducerar en ny läkandekandidat utformad för att blockera den vägen. Genom att visa hur man kan återkänsliggöra envisa tumörer för standardläkemedel, pekar arbetet mot mer hållbara behandlingsalternativ för patienter.
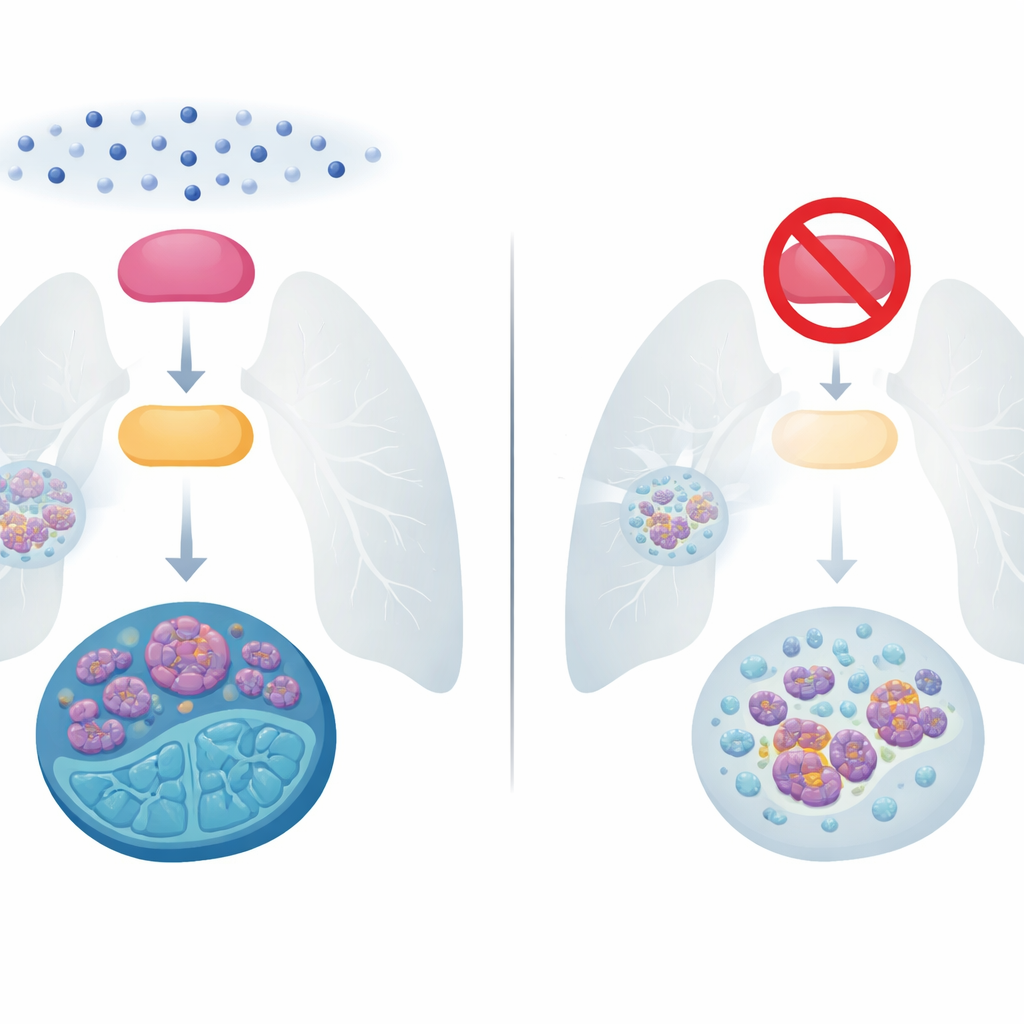
Utmaningen med okontrollerad småcellig lungcancer
Småcellig lungcancer står för ungefär 15 % av alla lungcancerfall men orsakar en oproportionerligt stor andel av dödsfallen eftersom den växer och sprider sig snabbt. I årtionden har huvudbehandlingen varit en kombination av platinabaserad kemoterapi och läkemedlet etoposid. Många patienter svarar initialt väl, men de flesta tumörer återkommer snart i en svårare behandlingsbar form, och femårsöverlevnaden ligger fortfarande under 10 %. Nyare strategier, inklusive immunterapi, har bara förlängt livet måttligt för personer med långt framskriden sjukdom. Att förstå exakt hur dessa tumörer blir resistenta mot kemoterapi är därför en av de mest brådskande frågorna inom fältet.
En överlevnadsväxel inne i tumörcellerna
Forskarna fokuserade på två proteiner som fungerar som en signalväxel inne i cancercellerna. Det ena, kallat BMX, är en kinas — en typ av enzym som slår på eller av andra proteiner. Det andra, E2F1, är en transkriptionsfaktor som aktiverar gener som styr celldelning, DNA‑reparation och cellers förmåga att röra sig och invadera. I prover från 100 patienter och i flera småcelliga lungcancer‑cellinjer fann teamet att aktivt BMX och höga nivåer av E2F1 nästan alltid förekom tillsammans, särskilt i tumörer som slutat svara på kemoterapi. När celler utsattes för vanliga läkemedel som cisplatin eller etoposid ökade både BMX‑aktivitet och E2F1‑nivåer i samklang, och drogresistenta cellinjer visade mycket högre nivåer av båda proteinerna än sina drogkänsliga motsvarigheter.
Hur tumörens inre kopplingar skyddar den mot läkemedel
Vid en närmare granskning avslöjade teamet hur BMX hjälper E2F1 att förbli aktivt. I stället för att binda direkt till E2F1, aktiverar BMX ett relä av andra proteiner — ERK1/2 och Cyclin D1/CDK4/6‑komplexet — som kemiskt modifierar E2F1 på specifika platser. Dessa modifieringar fungerar som ett skyddspansar, vilket gör E2F1 mer stabilt och hjälper det att ackumuleras i cellkärnan, där det kan slå på gener för snabb tillväxt, effektiv DNA‑reparation och cellmigration. Normalt kan E2F1 märkas för nedbrytning av cellens proteinåtervinningsmaskineri. I kemoresistenta celler skärmar dock BMX‑signalering av E2F1 från detta kasseringssystem, så proteinet består kvar och hjälper tumörcellerna att överleva kemoterapins skador.
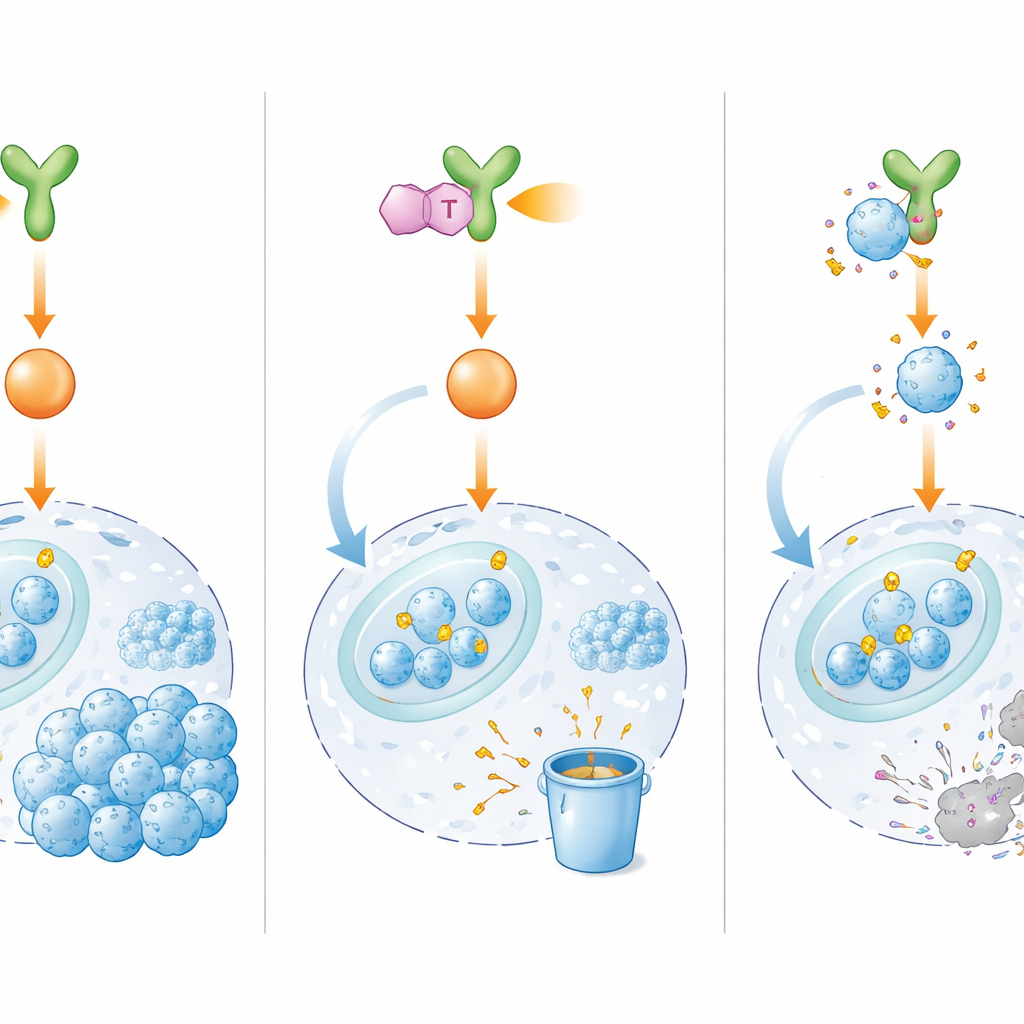
Ett nytt läkemedel som släcker strömmen till växeln
Eftersom det visat sig svårt att rikta in sig direkt på E2F1, gav sig forskarna i kast med att blockera dess upstream‑regulator, BMX. Ur tusentals kandidatmolekyler identifierade de IHMT‑15137, en liten förening som binder starkt och selektivt till BMX och som verkar fästa irreversibelt. I laboratorietester stängde IHMT‑15137 ner BMX‑aktiviteten och dämpade dess nedströmsignaler, inklusive ERK1/2 och Cyclin D1/CDK4/6. Som en följd förlorade E2F1 sina skyddande kemiska markeringar, blev mer märkbar för nedbrytning och bröts snabbt ner. I flera drogresistenta cellinjer, liksom i patient‑härledda celler och tredimensionella mini‑tumörer, ledde kombinationen av IHMT‑15137 och cisplatin till starkare cellcykelarrest, mer DNA‑skada, högre grad av celldöd och markant minskad tillväxt, migration och invasion jämfört med enbart kemoterapi.
Bevis för nytta i djur‑ och patientliknande modeller
Teamet testade sedan kombinationen i möss med mänskliga småcelliga lungcancertransplantat, inklusive tumörer direkt hämtade från patienter vars sjukdom återkommit efter kemoterapi. I flera oberoende modeller bromsade tillsatsen av IHMT‑15137 till standarden cisplatin–etoposid signifikant tumörtillväxt utan att orsaka betydande viktnedgång eller tydliga organskador hos djuren. Tumörer från behandlade möss visade minskad aktivering av BMX och dess signaleringspartners, lägre nivåer av E2F1 samt fler markörer för DNA‑skada och apoptos. Säkerhetsstudier antydde att IHMT‑15137 har färre blödnings‑ och off‑target‑effekter än äldre, mindre selektiva läkemedel som också riktar sig mot BMX, vilket talar för dess potential som en mer tolererbar partner till kemoterapi.
Vad detta betyder för framtida behandling
För en icke‑specialist är huvudbudskapet att forskarna har kartlagt en stor resistensväg i småcellig lungcancer och visat hur man kan stänga ner den. Tumörceller använder BMX för att stabilisera E2F1, en huvudregulator för tillväxt, vilket hjälper dem att reparera kemoterapiinducerad skada och fortsätta dela sig. Den nya hämmaren IHMT‑15137 slår av strömmen till denna väg, destabiliserar E2F1 och gör långvarigt resistenta tumörer sårbara igen för befintliga läkemedel. Även om denna förening behöver ytterligare optimering och studier i människor, ger studien en tydlig ritning för terapier som skulle kunna förlänga och fördjupa kemoterapisvaren för patienter med denna aggressiva cancer.
Citering: Wu, T., Qi, S., Shi, C. et al. BMX inhibition overcomes small cell lung cancer chemoresistance by stabilizing E2F1 via ERK1/2-Cyclin D1/CDK4/6 axis. Sig Transduct Target Ther 11, 125 (2026). https://doi.org/10.1038/s41392-026-02644-1
Nyckelord: småcellig lungcancer, kemoresistens, BMX‑kinas, E2F1‑signalering, målinriktad terapi