Clear Sky Science · ru
Ингибирование BMX преодолевает хеморезистентность при мелкоклеточном раке легкого путем стабилизации E2F1 через ось ERK1/2‑Cyclin D1/CDK4/6
Почему это важно для людей с раком легкого
Мелкоклеточный рак легкого — одна из самых смертельных форм рака легкого. Он часто сначала поддается химиотерапии, но затем рецидивирует в виде, который больше не отвечает на лечение. В этом исследовании выявлен ключевой молекулярный «маршрут побега», которым опухолевые клетки пользуются, чтобы пережить химиотерапию, и представлен новый кандидат на лекарство, разработанный для блокировки этого маршрута. Показав, как повторно сделать упрямые опухоли чувствительными к стандартным препаратам, работа указывает путь к более долговременным вариантам лечения для пациентов.
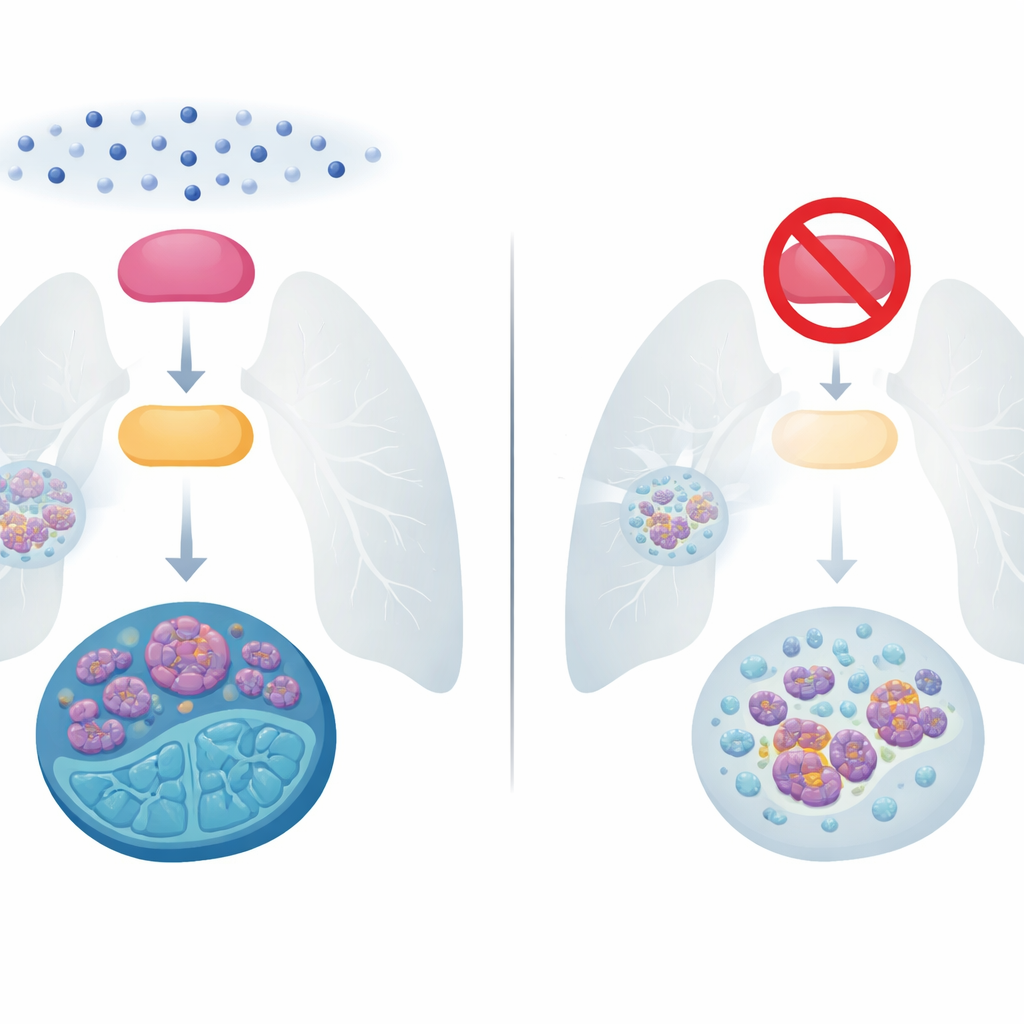
Проблема неукротимого мелкоклеточного рака легкого
Мелкоклеточный рак легкого составляет примерно 15% случаев рака легкого, но вызывает непропорционально большое число смертей, потому что быстро растет и метастазирует. Десятилетиями основным лечением была комбинация препаратов на основе платины и этопозида. Многие пациенты первоначально хорошо отвечают, но большинство опухолей вскоре возвращается в более труднорукотреной форме, и пятилетняя выживаемость остается ниже 10%. Новые подходы, включая иммунотерапию, лишь умеренно продлили жизнь при распространенном заболевании. Поэтому понимание того, как именно эти опухоли становятся резистентными к химиотерапии, является одной из наиболее неотложных задач в этой области.
Переключатель выживания внутри опухолевых клеток
Исследователи сосредоточились на двух белках, которые функционируют как сигнальная распределительная панель внутри раковых клеток. Один, называемый BMX, — это киназа, вид фермента, который включает или выключает другие белки. Другой, E2F1, — транскрипционный фактор, включающий гены, контролирующие деление клеток, восстановление ДНК и способность клеток к миграции и инвазии. В образцах от 100 пациентов и в нескольких линиях клеток мелкоклеточного рака команда обнаружила, что активный BMX и высокие уровни E2F1 почти всегда совпадают, особенно в опухолях, переставших отвечать на химиотерапию. При воздействии на клетки распространенными препаратами, такими как цисплатин или этопозид, активность BMX и уровни E2F1 повышались синхронно, а в лекарственно‑резистентных линиях обе эти величины были значительно выше, чем в чувствительных линиях.
Как внутренняя проводка опухоли защищает ее от препаратов
Углубившись, команда выяснила, как BMX помогает E2F1 оставаться активным. Вместо прямого связывания с E2F1, BMX запускает релейный каскад других белков — ERK1/2 и комплекса Cyclin D1/CDK4/6 — которые химически модифицируют E2F1 в определенных позициях. Эти модификации действуют как защитная броня, делая E2F1 более стабильным и способствуя его накоплению в ядре клетки, где он включает гены, отвечающие за быстрое деление, эффективный ремонт ДНК и миграцию клеток. Обычно E2F1 может помечаться для разрушения системой утилизации белков клетки. Однако в хеморезистентных клетках сигнализация BMX защищает E2F1 от этой системы утилизации, поэтому белок сохраняется и помогает опухолевым клеткам пережить повреждения, вызванные химиотерапией.
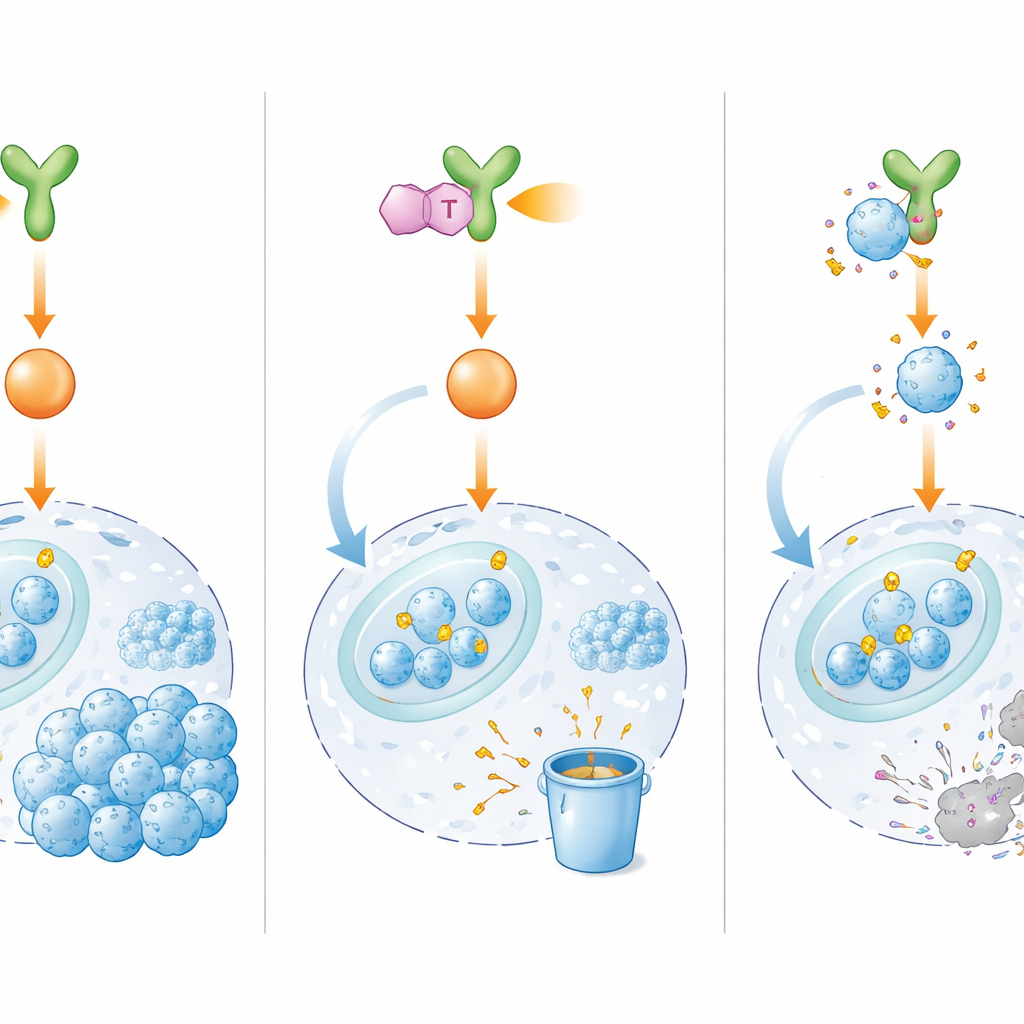
Новый препарат, который отключает питание переключателя
Поскольку прямое нацеливание на E2F1 оказалось сложным, исследователи решили блокировать его верхнеуровневого регулятора — BMX. Из тысяч кандидатов они выделили IHMT‑15137, небольшое соединение, которое сильно и селективно связывается с BMX и, по-видимому, делает это необратимо. В лабораторных тестах IHMT‑15137 подавлял активность BMX и ослаблял его нисходящие сигналы, включая ERK1/2 и Cyclin D1/CDK4/6. В результате E2F1 терял защитные химические метки, все интенсивнее помечался для разрушения и быстро расщеплялся. В нескольких лекарственно‑резистентных линиях клеток, а также в клетках, полученных от пациентов, и трехмерных мини‑опухолях комбинация IHMT‑15137 с цисплатином вызывала более выраженную блокаду клеточного цикла, больше повреждений ДНК, более высокие уровни гибели клеток и резкое снижение роста, миграции и инвазии по сравнению с одной только химиотерапией.
Доказательство пользы в моделях на животных и «пациентоподобных» моделях
Далее команда протестировала комбинацию на мышах с трансплантатами человеческого мелкоклеточного рака легкого, включая опухоли, непосредственно полученные от пациентов с рецидивом после химиотерапии. В нескольких независимых моделях добавление IHMT‑15137 к стандартной терапии цисплатином–этопозидом значительно замедляло рост опухолей без существенной потери веса или явных повреждений органов у животных. Опухоли из обработанных мышей демонстрировали сниженную активацию BMX и его сигнальных партнеров, пониженные уровни E2F1 и больше маркеров повреждения ДНК и апоптоза. Исследования безопасности показали, что IHMT‑15137 вызывает меньше кровотеч и побочных эффектов вне целевого действия, чем старые, менее селективные препараты, также поражающие BMX, что подтверждает его потенциал в качестве более переносимого партнера для химиотерапии.
Что это значит для будущего лечения
Для неспециалиста ключевое послание состоит в том, что исследователи проследили главный путь резистентности при мелкоклеточном раке легкого и показали, как его можно выключить. Опухолевые клетки используют BMX для стабилизации E2F1 — основного регулятора роста — что помогает им ремонтировать повреждения, вызванные химиотерапией, и продолжать деление. Новый ингибитор IHMT‑15137 отключает этот путь, дестабилизируя E2F1 и вновь делая долго‑резистентные опухоли уязвимыми для существующих препаратов. Хотя это соединение потребует дальнейшей оптимизации и клинических испытаний на людях, исследование дает четкую дорожную карту для терапии, способной удлинить и усилить ответы на химиотерапию у пациентов с этим агрессивным раком.
Цитирование: Wu, T., Qi, S., Shi, C. et al. BMX inhibition overcomes small cell lung cancer chemoresistance by stabilizing E2F1 via ERK1/2-Cyclin D1/CDK4/6 axis. Sig Transduct Target Ther 11, 125 (2026). https://doi.org/10.1038/s41392-026-02644-1
Ключевые слова: мелкоклеточный рак легкого, хеморезистентность, киназа BMX, сигнализация E2F1, таргетная терапия