Clear Sky Science · zh
FRA10AC1基因的新型纯合剪接变异:对表型的进一步界定
当基因编辑出错时
大多数人把基因想象成不变的蓝图,但实际上我们的细胞在将遗传信息转化为功能性蛋白之前,持续对这些信息进行裁剪与拼接。本文探讨当这一编辑过程出现微小缺陷并影响名为FRA10AC1的基因时,会引发何种后果,导致儿童严重的发育问题。通过追踪一名年轻患者并将其与全球少数已知病例进行比较,研究者展示了基因信息处理中的细微故障如何波及大脑、肾脏、眼睛及其他器官。
细胞中的微小编辑器
在每个细胞内,长长的原始遗传序列必须被修剪并拼接在一起才能被利用。这个任务由一种称为剪接体的分子机器完成,它切去不用的片段并缝合有用的片段。FRA10AC1基因编码一种位于该机器边缘的辅助蛋白,微调剪接过程的切割与连接方式。早期研究发现,从双亲处各遗传到一个有缺陷的FRA10AC1拷贝的儿童,可能出现特征性的发育迟缓、异常面容、生长不良以及连接大脑两半球的粗大神经纤维束(即胼胝体)发生改变。然而,全球仅有十例此类患者被报道,关于症状的完整范围以及基因中不同类型缺陷如何影响结局仍有许多疑问。
一名儿童的病例补充新线索
作者描述了一名埃及男孩的病例,该儿童出生于双亲近亲婚配且孕期无并发症。自婴儿期起,他在各方面发育均明显落后:八个月时仍未微笑、未能跟随目光、未对声音有反应,亦未能控制头部。医生记录到其肌张力非常低、躯干动作不稳,以及称为眼球震颤的快速不受控眼球运动。面容特征包括面部较长、额头高、内眦赘皮、眼裂较长、鼻梁塌陷、鼻尖圆钝且上唇较长。随着年龄增长,他最终能够站立并发出几段简单音节,但仍严重发育迟缓且极度多动。
隐藏在脑、眼与肾中的改变
对该儿童脑部的影像检查显示若干结构性差异:连接两侧脑半球的桥梁发育不足,神经纤维周围的髓鞘形成延迟,且在称为尾状核的深部区域可见一个小的含液囊肿。眼科检查显示视网膜的锥细胞受损——锥细胞负责清晰的中心视力与色觉,这解释了他较差的视觉反应。腹部影像学还发现另一不寻常情况:双肾融合且位置偏低,位于盆腔而非正常位置。既有的FRA10AC1病例中很少见到肾与眼的这些问题,因此研究团队对该儿童的全部蛋白编码基因进行了仔细筛查以排除其他可能的解释,未发现其他可疑原因。
追踪异常的遗传信息
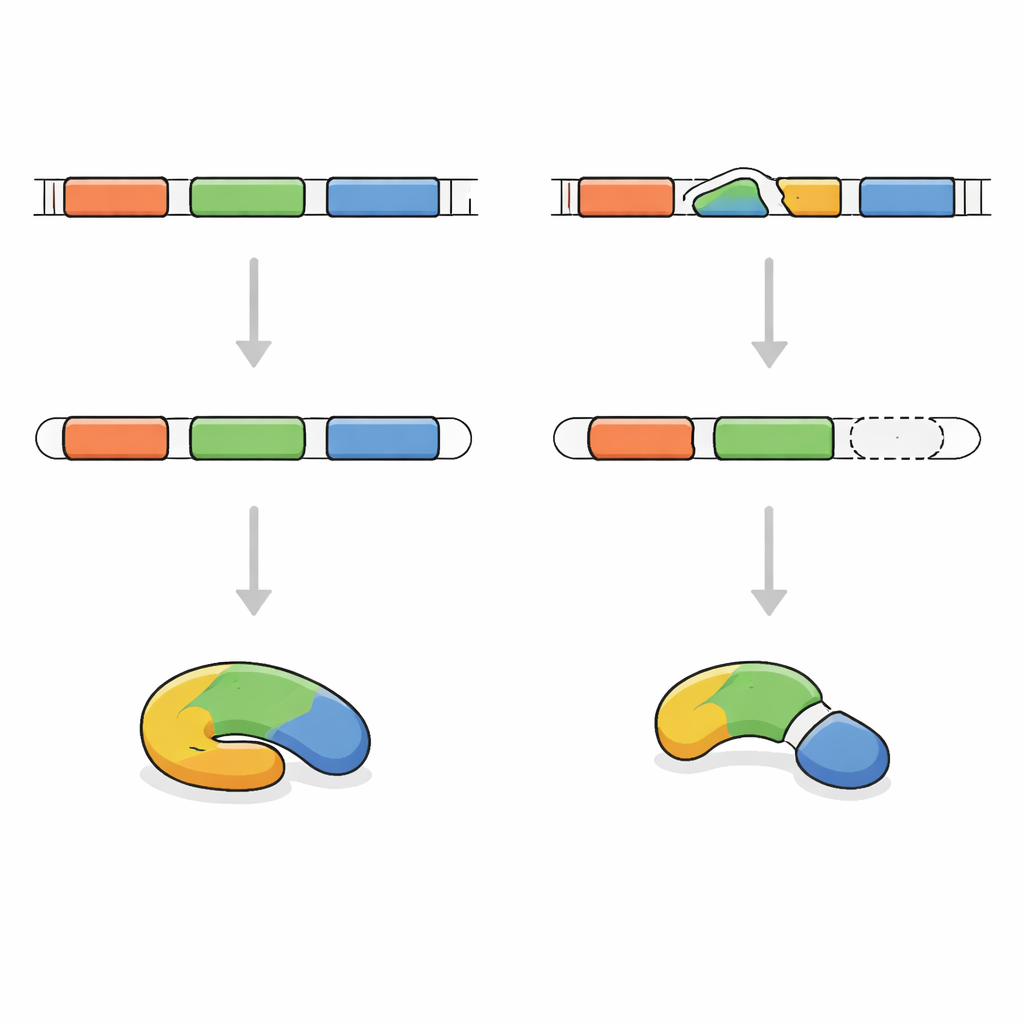
为确定病因,研究者对男孩的蛋白编码DNA区域进行了测序。他们发现其两份FRA10AC1基因均带有同一处发生在信息编辑关键“连接点”的微小改变。其父母均为健康个体,各携带一份变异拷贝和一份正常拷贝。研究团队随后检测了来自男孩血细胞的FRA10AC1转录本。转录本未包含所有预期片段,而是完全跳过了一段,这导致编码框移位,出现早期终止信号,生成一段缩短且很可能失去功能的蛋白。根据国际判定遗传变异的指南,该变异被归类为明确致病。
对家庭的意义
通过将这名男孩的病例纳入已知的少数病例中,研究有助于澄清与FRA10AC1相关疾病的临床图谱。像本例一样完全丧失该蛋白功能的儿童,往往在智力与运动方面受影响更重,并更可能伴随心脏、肾脏、眼睛与皮肤等器官的先天异常。相比之下,以往报道中保留部分功能的FRA10AC1变异患者则学习与发育问题较轻,器官异常较少。对家庭与临床医生而言,这项工作强调单一基因的缺陷可导致一组可识别的面部特征、发育迟缓与脑部改变,一旦怀疑诊断,应对肾脏与眼睛进行细致检查。
引用: Abdel-Hamid, M.S., Abdel-Salam, G.M.H. A novel homozygous splicing variant in FRA10AC1: further delineation of the phenotype. J Hum Genet 71, 363–367 (2026). https://doi.org/10.1038/s10038-025-01447-6
关键词: 神经发育障碍, 剪接体, FRA10AC1基因, 遗传变异, 胼胝体