Clear Sky Science · nl
Een nieuw homozygoot splice-variant in FRA10AC1: nadere afbakening van het fenotype
Wanneer genbewerking misgaat
De meesten van ons zien genen als vaste blauwdrukken, maar in werkelijkheid zijn onze cellen voortdurend bezig genetische berichten te knippen en te plakken voordat ze worden omgezet in werkzame eiwitten. Dit artikel onderzoekt wat er gebeurt wanneer een klein foutje in dit bewerkingsproces een gen genaamd FRA10AC1 aantast, wat leidt tot ernstige ontwikkelingsproblemen bij kinderen. Door één jonge patiënt te volgen en hem te vergelijken met de weinige bekende gevallen wereldwijd, laten de onderzoekers zien hoe een subtiele hapering in de verwerking van genetische informatie zich kan uitbreiden naar de hersenen, nieren, ogen en andere organen.
De kleine redacteuren van de cel
In elke cel moeten lange stukken ruwe genetische code worden ingekort en aan elkaar gekoppeld voordat ze bruikbaar zijn. Deze taak wordt uitgevoerd door een moleculair complex dat het spliceosoom wordt genoemd, dat ongebruikte segmenten eruit knipt en de nuttige stukken aan elkaar naait. Het FRA10AC1-gen maakt een hulpstof die aan de rand van dit complex zit en fijn afstelt hoe het knippen en plakken plaatsvindt. Eerdere studies lieten zien dat kinderen die defecte kopieën van FRA10AC1 van beide ouders erven, een kenmerkend patroon kunnen ontwikkelen van vertraagde ontwikkeling, opvallende gelaatstrekken, slechte groei en veranderingen in het dikke bundel zenuwvezels die de twee hersenhelften verbindt, het corpus callosum genoemd. Echter, slechts tien dergelijke patiënten waren wereldwijd beschreven, waardoor veel vragen over het volledige kraam van symptomen en hoe verschillende soorten fouten in het gen het beloop beïnvloeden, onbeantwoord bleven.
Het verhaal van één kind vult nieuwe stukjes aan
De auteurs beschrijven een Egyptische jongen, geboren uit verwante ouders na een ongecompliceerde zwangerschap. Vanaf de zuigelingentijd liet hij duidelijke achterstand in alle ontwikkelingsgebieden zien: hij lachte niet, volgde niet met zijn ogen, reageerde niet op geluiden en had op acht maanden geen hoofdcontrole. Artsen noteerden zeer lage spierspanning, onstabiele rompbewegingen en snelle, ongecontroleerde oogbewegingen die nystagmus worden genoemd. Zijn gelaatstrekken omvatten een lang gezicht, hoog voorhoofd, huidplooien aan de binnenhoeken van de ogen, lange oogopeningen, een afgeplatte neusrug en een afgeronde neuspunt met een lange bovenlip. Toen hij ouder werd kon hij uiteindelijk staan en een paar eenvoudige lettergrepen uitspreken, maar hij bleef ernstig vertraagd en zeer hyperactief.
Verborgen veranderingen in hersenen, ogen en nieren
Beelden van het brein van het kind toonden meerdere structurele afwijkingen: de verbindende brug tussen de twee hersenhelften was onderontwikkeld, het isolatiemateriaal rond zenuwvezels (myeline) was vertraagd in de vorming, en er was een kleine met vocht gevulde cyste diep in een regio die de nucleus caudatus wordt genoemd. Oogonderzoeken lieten schade zien aan de kegeltjes in het netvlies, die nodig zijn voor scherp centraal zicht en kleurenzicht, wat zijn zwakke visuele reacties verklaart. Beeldvorming van de buik bracht nog een afwijking aan het licht: beide nieren waren met elkaar vergroeid en bevonden zich laag in het bekken in plaats van op de gebruikelijke plaats. Deze nier- en oogproblemen waren eerder slechts zelden gezien in FRA10AC1-gevallen, dus doorzocht het team zorgvuldig het volledige setje eiwitcoderende genen van het kind op andere plausibele verklaringen en vond niets.
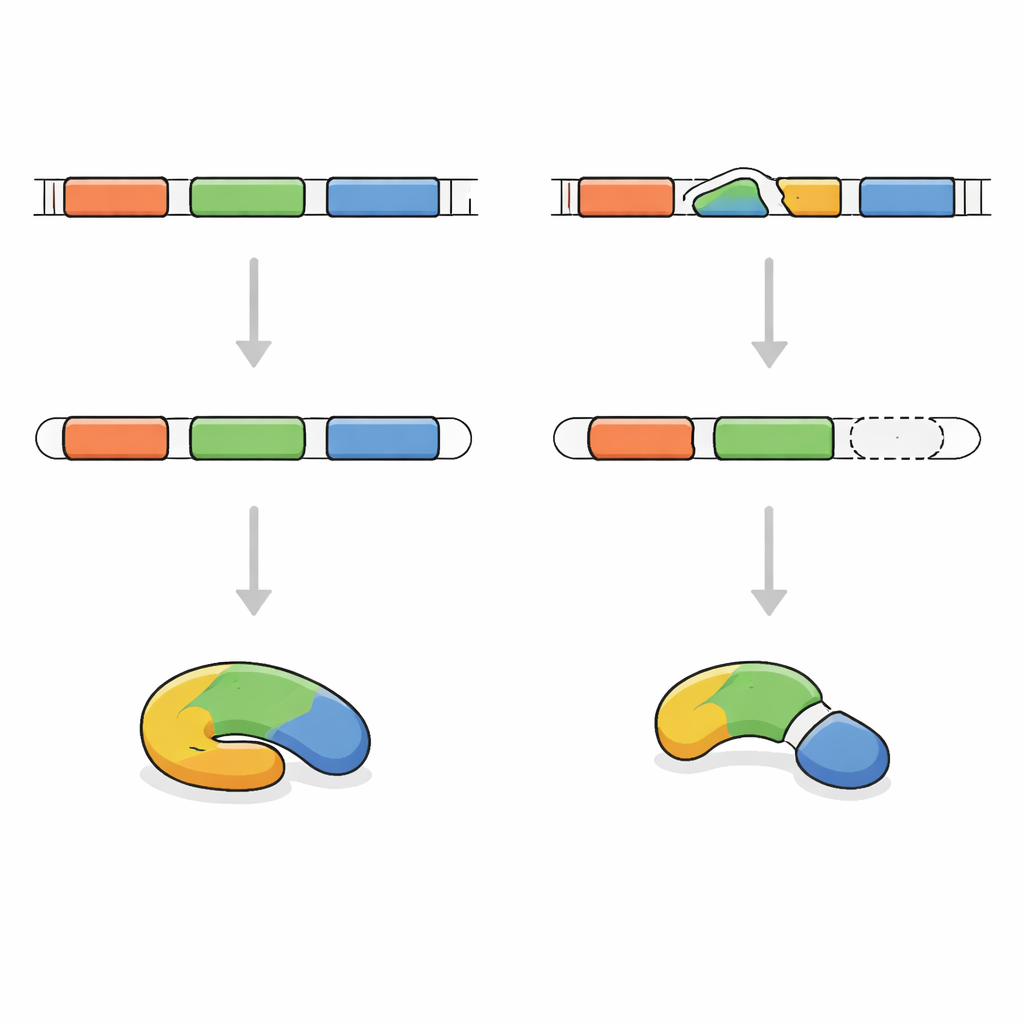
Het spoor van het defecte genetische bericht
Om de oorzaak te achterhalen sequenceden de onderzoekers de eiwitcoderende delen van het DNA van de jongen. Ze ontdekten dat beide kopieën van zijn FRA10AC1-gen dezelfde kleine wijziging droegen op een kritisch "aansluitpunt" dat tijdens de berichtbewerking wordt gebruikt. Zijn ouders, die gezond waren, droegen elk één gewijzigde en één normale kopie. Het team onderzocht vervolgens het FRA10AC1-bericht dat uit zijn bloedcellen werd gemaakt. In plaats van alle verwachte segmenten te bevatten, was het bericht één onderdeel volledig overgeslagen. Dit zorgde ervoor dat de instructies uit de pas raakten, een vroeg stopteken werden ingevoegd en leidde tot een verkort, waarschijnlijk nutteloos eiwit. Op basis van internationale richtlijnen voor het beoordelen van genetische varianten werd deze wijziging als duidelijk ziekteverwekkend geclassificeerd.
Wat dit betekent voor families
Door dit geval van de jongen toe te voegen aan het kleine aantal dat al bekend is, helpt de studie het beeld van de FRA10AC1-gerelateerde aandoening te verhelderen. Kinderen met volledig verlies van dit eiwit, zoals deze patiënt, hebben doorgaans ernstigere verstandelijke en motorische beperkingen en hebben vaker bijkomende aangeboren afwijkingen aan organen zoals het hart, de nieren, de ogen en de huid. Daarentegen hadden eerder beschreven kinderen met een mildere, deels functionerende versie van FRA10AC1 minder ernstige leerproblemen en minder orgaanafwijkingen. Voor families en clinici benadrukt dit onderzoek dat een fout in dit ene gen ten grondslag kan liggen aan een herkenbare combinatie van gelaatstrekken, ontwikkelingsachterstanden en hersenveranderingen, en dat zorgvuldige controle van nieren en ogen belangrijk is zodra de diagnose wordt vermoed.
Bronvermelding: Abdel-Hamid, M.S., Abdel-Salam, G.M.H. A novel homozygous splicing variant in FRA10AC1: further delineation of the phenotype. J Hum Genet 71, 363–367 (2026). https://doi.org/10.1038/s10038-025-01447-6
Trefwoorden: neuro-ontwikkelingsstoornis, spliceosoom, FRA10AC1-gen, genetische varianten, corpus callosum