Clear Sky Science · it
Una variante di splicing omozigote in FRA10AC1: ulteriore delimitazione del fenotipo
Quando la modifica genica va storta
La maggior parte di noi pensa ai geni come a progetti statici, ma in realtà le nostre cellule tagliano e incollano continuamente i messaggi genetici prima di trasformarli in proteine funzionanti. Questo articolo esplora cosa accade quando una piccola anomalia in questo processo di modifica interessa un gene chiamato FRA10AC1, provocando gravi problemi di sviluppo nei bambini. Seguendo un giovane paziente e confrontandolo con i pochi casi noti in tutto il mondo, i ricercatori mostrano come un sottile difetto nell’elaborazione dell’informazione genetica possa riverberare sul cervello, i reni, gli occhi e altri organi.
I piccoli editor della cellula
All’interno di ogni cellula, lunghe porzioni di codice genetico grezzo devono essere ritagliate e unite prima di poter essere utilizzate. Questo compito è svolto da una macchina molecolare nota come spliceosoma, che elimina segmenti non utilizzati e cuce insieme quelli utili. Il gene FRA10AC1 produce una proteina ausiliaria che si trova ai margini di questa macchina e ne regola finemente il modo in cui avvengono i tagli e le giunzioni. Studi precedenti avevano riscontrato che bambini che ereditano copie difettose di FRA10AC1 da entrambi i genitori possono sviluppare un quadro caratteristico di ritardo dello sviluppo, caratteristiche facciali insolite, scarsa crescita e alterazioni del fascio spesso di fibre nervose che collega i due emisferi cerebrali, chiamato corpo calloso. Tuttavia, solo dieci pazienti di questo tipo erano stati descritti in tutto il mondo, lasciando molte domande sull’intera gamma di sintomi e su come i diversi tipi di difetti nel gene influenzino l’esito.
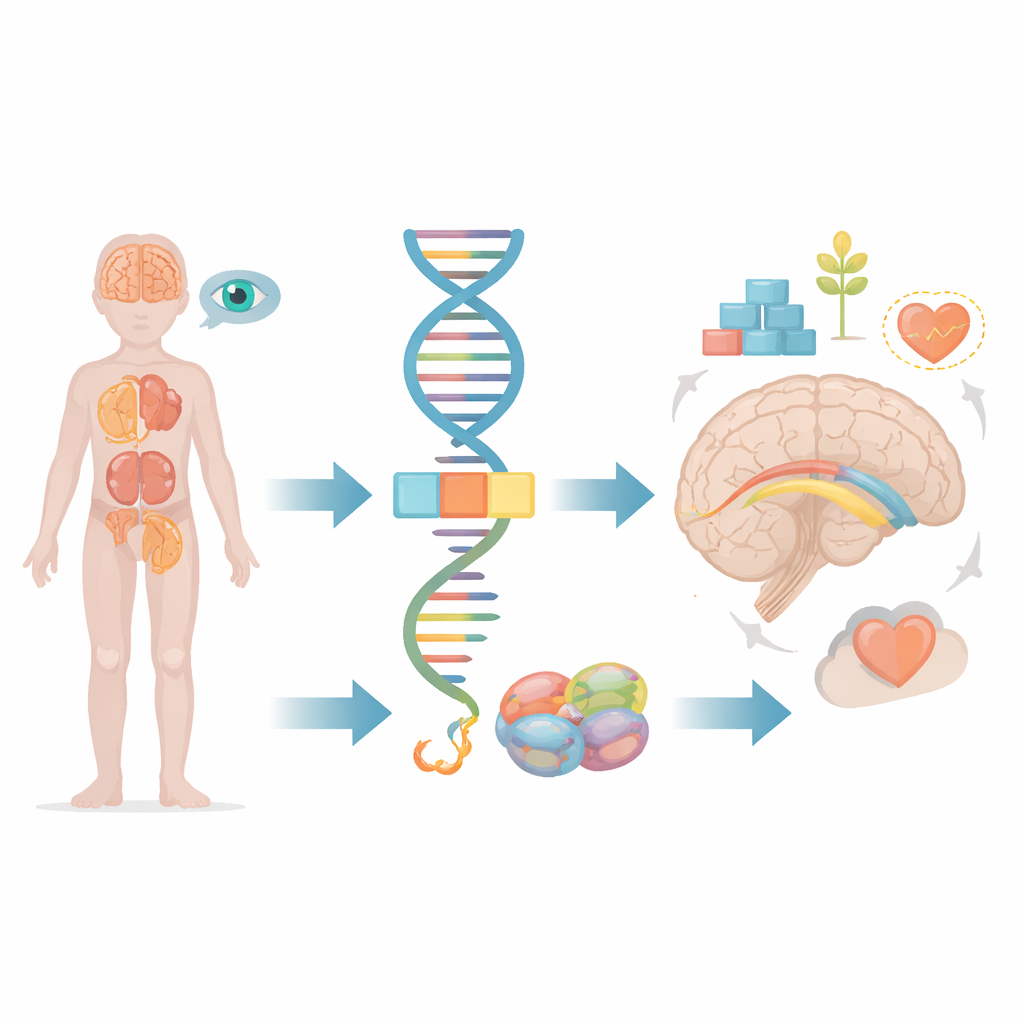
La storia di un bambino aggiunge nuovi elementi
Gli autori descrivono un bambino egiziano nato da genitori consanguinei dopo una gravidanza senza complicazioni. Fin dalla prima infanzia ha mostrato un marcato ritardo in tutte le aree dello sviluppo: non sorrideva, non seguiva con gli occhi, non rispondeva ai suoni e non aveva acquisito il controllo del capo a otto mesi. I medici hanno notato tono muscolare molto basso, movimenti del tronco instabili e rapidi movimenti oculari incontrollati detti nistagmo. L’aspetto facciale comprendeva un volto allungato, fronte alta, pieghe cutanee agli angoli interni degli occhi, aperture oculari lunghe, ponte nasale appiattito e punta del naso arrotondata con un labbro superiore lungo. Con l’età è riuscito a stare in piedi ed emettere alcune sillabe semplici, ma è rimasto gravemente ritardato e molto iperattivo.
Alterazioni nascoste in cervello, occhi e reni
Le scansioni del cervello del bambino hanno rivelato diverse differenze strutturali: il ponte di collegamento tra i due emisferi cerebrali era sottosviluppato, il materiale isolante attorno alle fibre nervose era in ritardo nella formazione, e vi era una piccola cisti contenente liquido in una regione profonda chiamata nucleo caudato. Gli esami oculari hanno mostrato danni alle cellule cono della retina, necessarie per la visione centrale nitida e per i colori, spiegando le sue scarse risposte visive. Le immagini dell’addome hanno evidenziato un altro reperto insolito: entrambi i reni risultavano fusi tra loro e situati in posizione bassa nel bacino invece che nelle loro sedi consuete. Questi problemi renali e oculari erano stati osservati solo raramente nei precedenti casi di FRA10AC1, perciò il team ha esaminato attentamente l’intero insieme di geni codificanti proteine del bambino alla ricerca di altre spiegazioni plausibili e non ne ha trovate.
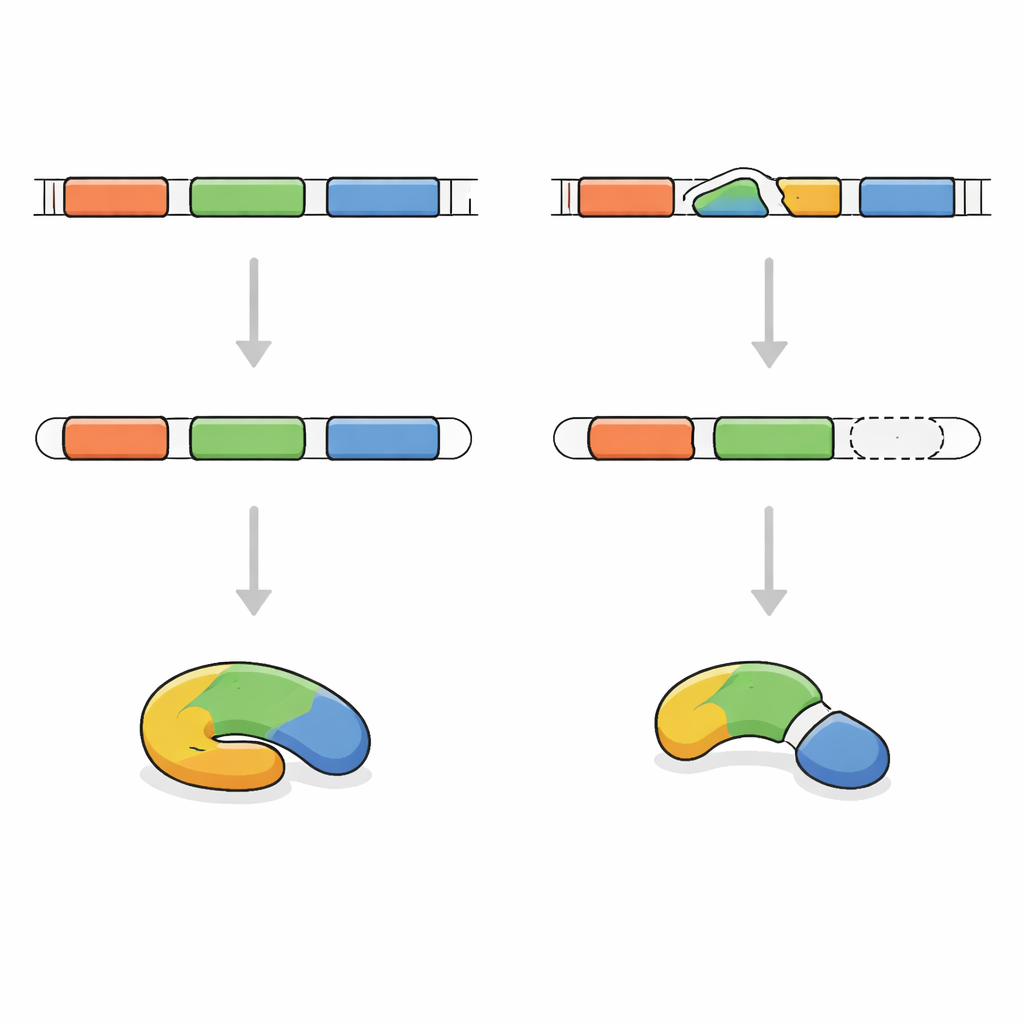
Tracciare il messaggio genetico difettoso
Per individuare la causa, i ricercatori hanno sequenziato le porzioni codificanti delle proteine del DNA del bambino. Hanno scoperto che entrambe le copie del suo gene FRA10AC1 presentavano la stessa piccola alterazione in un punto critico di “giunzione” utilizzato durante la modifica del messaggio. I suoi genitori, sani, portavano ciascuno una copia alterata e una normale. Il gruppo ha quindi esaminato il messaggio di FRA10AC1 prodotto dalle sue cellule del sangue. Invece di includere tutti i segmenti attesi, il messaggio aveva saltato completamente un pezzo. Questo ha causato lo spostamento delle istruzioni fuori fase, introducendo un segnale di stop precoce e portando a una proteina accorciata, probabilmente non funzionale. Sulla base delle linee guida internazionali per la valutazione delle varianti genetiche, questa alterazione è stata classificata come chiaramente patogenica.
Cosa significa per le famiglie
Aggiungendo il caso di questo bambino al piccolo numero già noto, lo studio contribuisce a chiarire il quadro del disturbo correlato a FRA10AC1. I bambini con perdita completa della proteina, come il paziente descritto, tendono ad avere difficoltà intellettive e motorie più severe e sono più propensi ad avere difetti congeniti aggiuntivi che interessano organi come cuore, reni, occhi e pelle. Al contrario, i bambini descritti in precedenza con una versione più lieve e parzialmente funzionante di FRA10AC1 presentavano problemi di apprendimento meno gravi e meno anomalie d’organo. Per le famiglie e i clinici, questo lavoro sottolinea che un difetto in questo singolo gene può essere all’origine di una combinazione riconoscibile di caratteristiche facciali, ritardi nello sviluppo e alterazioni cerebrali, e che controlli accurati di reni e occhi sono importanti una volta sospettata la diagnosi.
Citazione: Abdel-Hamid, M.S., Abdel-Salam, G.M.H. A novel homozygous splicing variant in FRA10AC1: further delineation of the phenotype. J Hum Genet 71, 363–367 (2026). https://doi.org/10.1038/s10038-025-01447-6
Parole chiave: disturbo dello sviluppo neurologico, spliceosoma, gene FRA10AC1, varianti genetiche, corpo calloso