Clear Sky Science · tr
NV716, Pseudomonas aeruginosa’da antibiyotik birikimini artıran zarf-etkin bir adjuvan olarak davranır
Gelecekteki antibiyotikler için bu araştırma neden önemli
İlaçlara dirençli bakteriyel enfeksiyonlar, yeni antibiyotiklerin keşfinden daha hızlı artıyor ve en zorlu suçlulardan bazıları Pseudomonas aeruginosa gibi Gram-negatif bakteriler. Bu mikroplar birçok ilacı dışarıda tutan güçlü bir dış kabukla çevrilidir. Bu çalışma, tek başına bakteriyi öldürmeyen ancak belirli mevcut antibiyotiklere karşı çok daha savunmasız hâle getiren NV716 adlı bir yardımcı bileşiği inceliyor. Böyle bir yardımcının nasıl çalıştığını anlamak, tamamen yeni ilaçlar için onlarca yıl beklemek yerine elimizdeki ilaçları kurtarmaya yönelik pratik bir yol açabilir.
Antibiyotikleri içeri sokmaya yardımcı bir kimyasal ortak
Araştırmacılar, Gram-negatif bakterilere karşı birkaç antibiyotiğin etkinliğini artırdığı daha önce bilinen, pozitif yüklü ve membrana yönelen NV716 üzerine odaklandı. NV716’yi tetrasiklinler ve florokinolonlar gibi farklı ailelerden ilaçlarla birlikte P. aeruginosa ve Escherichia coli karşısında test ettiler. En çarpıcı etki doksisiklin ile görüldü: NV716 ile birlikte kullanıldığında P. aeruginosada bakteriyel büyümeyi durdurmak için gereken doksisiklin miktarı yüz katın üzerinde azaldı. Antibiyotik fluoresansını bakteriyel hücre içinde ölçerek, bu öldürme gücündeki artışın doksisiklinin mikroplar içinde gerçekte ne kadar biriktiğiyle yakından ilişkili olduğunu gösterdiler.
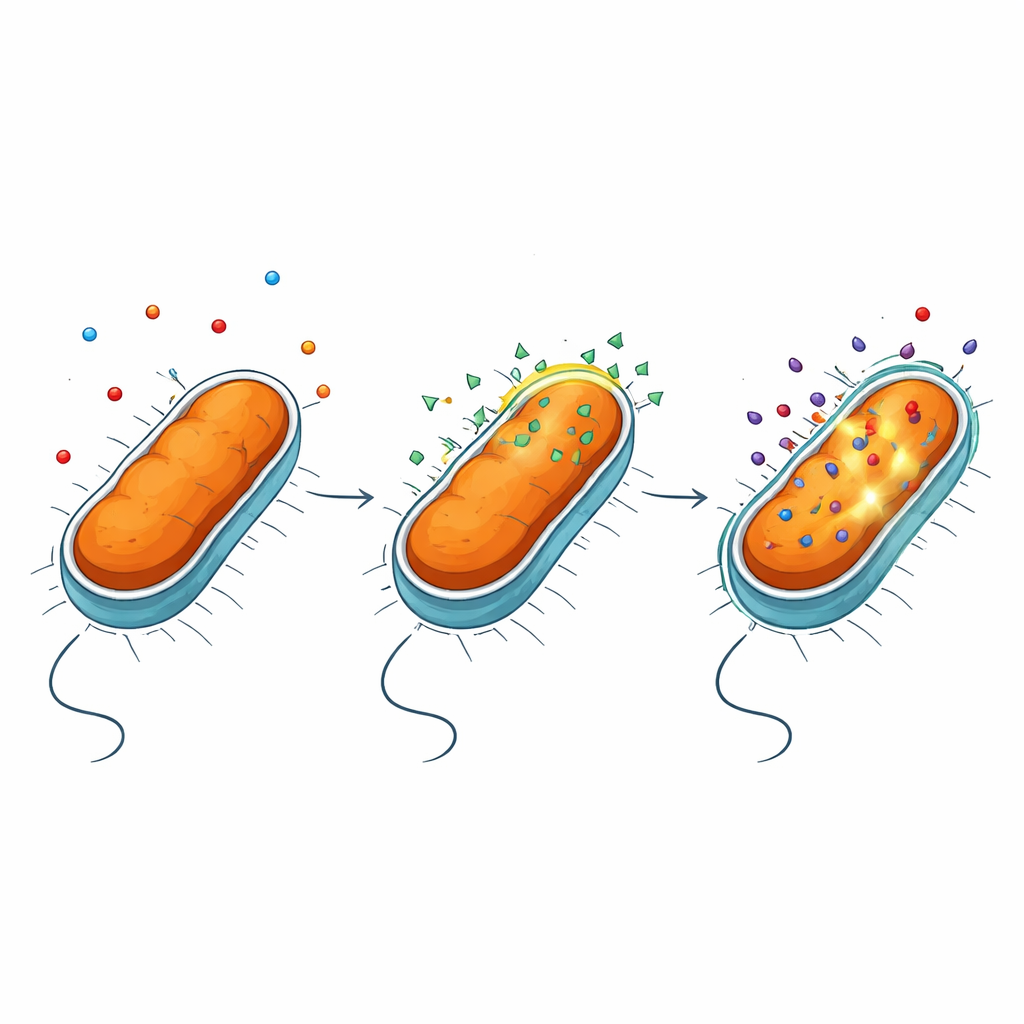
Hücreyi yırtmadan dış kalkanı açmak
Gram-negatif bakteriler, lipopolisakkarit (LPS) adı verilen karmaşık bir molekülden zengin bir dış membranla korunur. Bu katman, birçok ilacı engelleyen son derece seçici bir filtre gibi davranır. Bir dizi floresan deneyi ve mutan suş kullanarak yazarlar, NV716’nın bakterilerin antibiyotikleri dışarı atan moleküler makineleri olan ekzos pompa (efflux pump)larını belirgin şekilde kapatmadığını buldu. Bunun yerine NV716 dış membranın davranışını değiştiriyor. Hücre yüzeyinde LPS’ye bağlanıyor ve bu moleküllerin paketlenmesini gevşetiyor; özellikle LPS’nin şeker “çekirdeği” kısaltıldığında ve altında yatan lipit kısmı daha fazla açığa çıktığında bu etki belirginleşiyor. Bu kontrollü huzursuzluk, hücreyi yırtmadan veya iç zarın—hayati süreçlerin gerçekleştiği yerin—zarar görmesini sağlamadan doksisiklin ve bazı diğer antibiyotiklerin membranı daha kolay geçmesine olanak tanıyor.
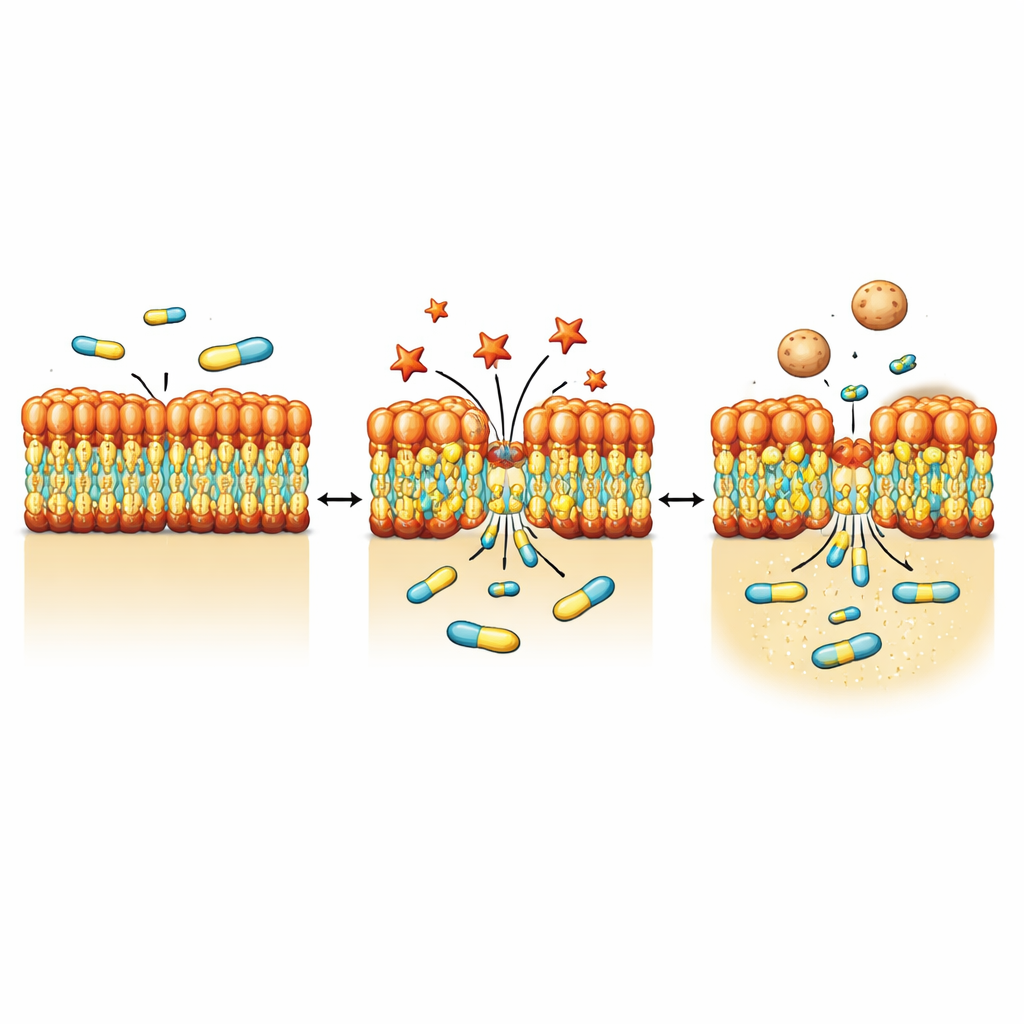
Membran stresini ve kabarcık benzeri dökülmeyi görselleştirmek
Bakterilerin NV716’ye fiziksel tepkisini görmek için ekip, elektron mikroskopisi ve yumuşak X-ışını tomografisi dahil yüksek çözünürlüklü görüntüleme yöntemlerine başvurdu. NV716’ye maruz kaldıktan sonra P. aeruginosa küçük çıkıntılar ve yüzeyden tomurcuklanıp kopan yamalar gösterdi; bu, dış zardan yapılmış çok sayıda dış membran vezikülünün—aynı malzemeden oluşan küçük küresel kabarcıkların—oluştuğunu gösteriyordu. Popülasyon ölçeğindeki ölçümler, vezikül üretiminin kabaca bir mertebe arttığını doğruladı. Ayrıntılı görüntüleme ve protein analizleri, bu veziküllerin porin proteinleri ve LPS gibi dış membran bileşenlerini taşıdığını, ancak içerden patlayarak oluşmuş olsaydı beklenebilecek düzeyde DNA taşımadığını gösterdi; bu, veziküllerin yüzeyden tomurcuklandığını destekliyor. Aynı zamanda, bakır etiketli bir NV716 versiyonu bileşiğin hücre içi serbestçe diffüzleşmek yerine membran bölgesinde yoğunlaştığını ortaya koydu.
Petriden canlı konaklara
Deney tüplerindeki güçlü etkiler her zaman canlı organizmalara çevrilemeyebileceği için, araştırmacılar NV716–doksisiklin eşleştirmesini balmumu güvesi Galleria mellonella larvaları kullanarak bir enfeksiyon modelinde değerlendirdiler. Kombinasyonla tedavi edilen larvalar doksisiklin tek başına verilenlere kıyasla daha iyi hayatta kalma eğilimi gösterdi, ancak test edilen koşullar altında iyileşme istatistiksel olarak anlamlı değildi. Bilgisayar tabanlı ilaç benzeri özellik tahminleri NV716’nın membranlarla etkileşime uygun özellikler gösterdiğini ve hayvanlarda tolere edilebilir olabileceğini düşündürüyor, ancak kapsamlı güvenlik ve dozlama çalışmaları yapılması gerekiyor. Yazarlar NV716’yı esasen bir kavram ispatı olarak görüyor: bakteriyel zarfın yok edilmesi yerine seçici olarak modüle edildiğinde nelerin mümkün olabileceğini gösteren bir molekül.
Zorlu enfeksiyonlarla mücadele açısından ne anlama geliyor
Günlük anlatımla, bu çalışma P. aeruginosa gibi zor nüfuz edilen bir bakterinin “kilidini” kapıyı kırmadan açmanın mümkün olduğunu gösteriyor. NV716 mikrobun dış kabuğuna yerleşerek yapısını ince şekilde yeniden düzenliyor; böylece özellikle doksisiklin gibi bazı antibiyotikler daha hızlı ve daha yüksek miktarlarda içeri süzülebiliyor. Bakteriler, fazladan dış kabuk parçalarını vezikül formunda dökerek yanıt veriyor—bunlar çöküşten ziyade stres işaretleri. İlk hayvan testleri ılımlı olmakla birlikte, çalışma dış membranı hedef alan yeni yardımcı moleküller ve hibrit ilaçlar tasarlamak için nicel bir yol haritası sunuyor. Bu tür stratejiler mevcut antibiyotikleri daha uzun süre kullanışlı kılabilir ve klinisyenlere hastane kaynaklı en inatçı enfeksiyonlara karşı yeni seçenekler sağlayabilir.
Atıf: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Anahtar kelimeler: antimikrobiyal direnç, Pseudomonas aeruginosa, dış zar, antibiyotik adjuvanı, doksisiklin