Clear Sky Science · nl
NV716 werkt als een envelop-actieve adjuvans die de ophoping van antibiotica in Pseudomonas aeruginosa vergroot
Waarom dit onderzoek belangrijk is voor toekomstige antibiotica
Door geneesmiddelresistente bacteriële infecties stijgt het aantal sneller dan er nieuwe antibiotica worden ontdekt, en enkele van de hardnekkigste daders zijn Gram-negatieve bacteriën zoals Pseudomonas aeruginosa. Deze microben omringen zich met een formidabele buitenlaag die veel medicijnen buiten houdt. Deze studie onderzoekt een hulpstof, NV716 genoemd, die op zichzelf de bacteriën niet doodt maar ze veel kwetsbaarder maakt voor bepaalde bestaande antibiotica. Begrijpen hoe zo’n hulpstof werkt kan een praktische weg openen om medicijnen die we al hebben te redden, in plaats van tientallen jaren te moeten wachten op volledig nieuwe middelen.
Een chemische partner die antibiotica helpt binnendringen
De onderzoekers concentreerden zich op NV716, een positief geladen, membraanzoekende molecule die eerder bekend stond om het versterken van de werking van meerdere antibiotica tegen Gram-negatieve bacteriën. Ze testten NV716 samen met middelen uit verschillende klassen, zoals tetracyclines en fluoroquinolonen, tegen P. aeruginosa en Escherichia coli. Het meest dramatische effect werd gezien met het antibioticum doxycycline: in combinatie met NV716 daalde de hoeveelheid doxycycline die nodig was om bacteriegroei te remmen met meer dan honderd keer in P. aeruginosa. Door de fluorescentie van het antibioticum binnen bacteriële cellen te meten, liet het team zien dat deze toename in effectiviteit nauw samenhangt met een sterke stijging van de hoeveelheid doxycycline die zich daadwerkelijk in de microben ophoopt.
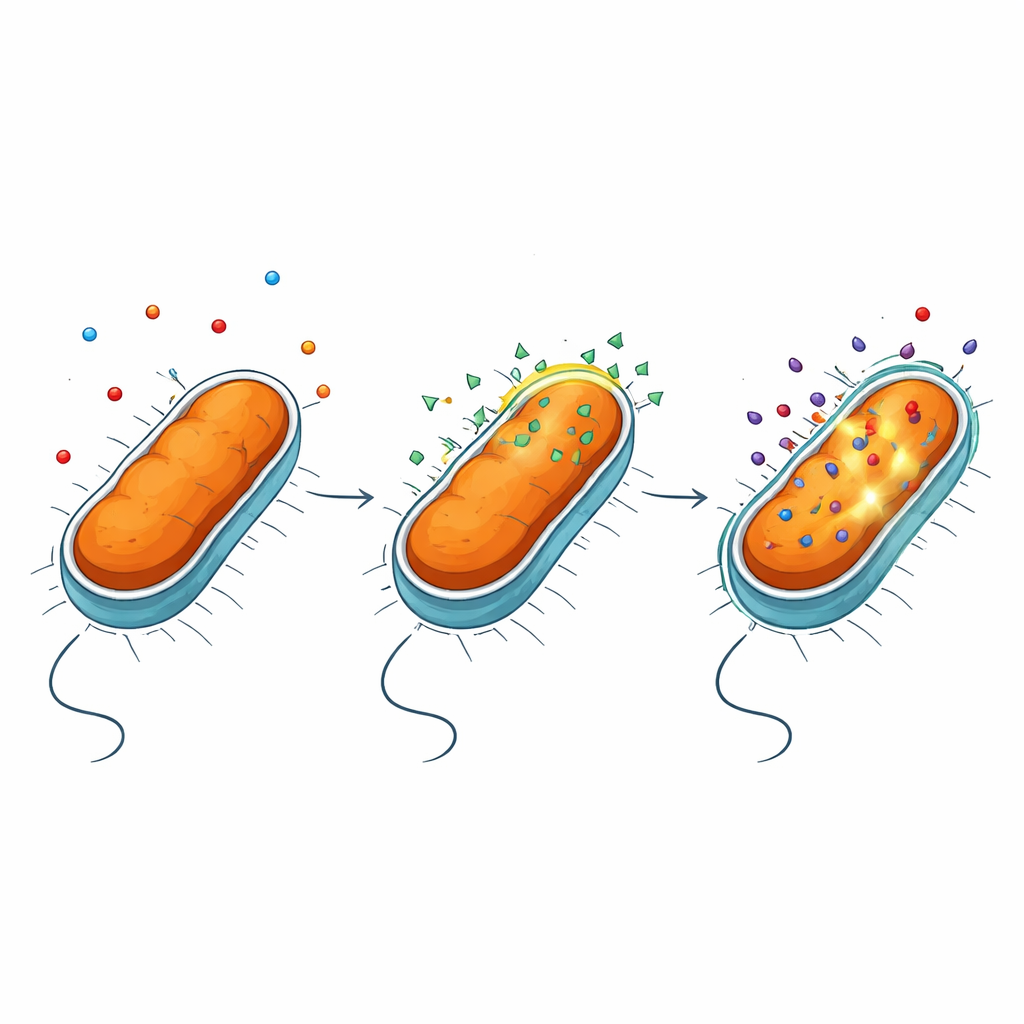
De buitenste schild openen zonder de cel te doen barsten
Gram-negatieve bacteriën worden beschermd door een buitenmembraan rijk aan een complex molecuul dat lipopolysaccharide (LPS) heet. Deze laag fungeert als een zeer selectief filter en blokkeert veel geneesmiddelen. Met een reeks fluorescentie-assays en mutanten vonden de auteurs dat NV716 de effluxpompen van de bacteriën—de moleculaire machines die antibiotica uitpompen—niet opvallend uitschakelt. In plaats daarvan verandert NV716 het gedrag van het buitenmembraan zelf. Het bindt aan LPS aan het celoppervlak en maakt de dichtheid van deze moleculen losser, vooral wanneer de suikerkern van LPS is verkort en het onderliggende lipidegedeelte meer blootligt. Deze gecontroleerde verstoring maakt het membraan gemakkelijker te passeren voor doxycycline en sommige andere antibiotica, zonder de cel open te scheuren of het binnenmembraan te beschadigen waar vitale processen plaatsvinden.
Membranspanning en blaasjesvorming visualiseren
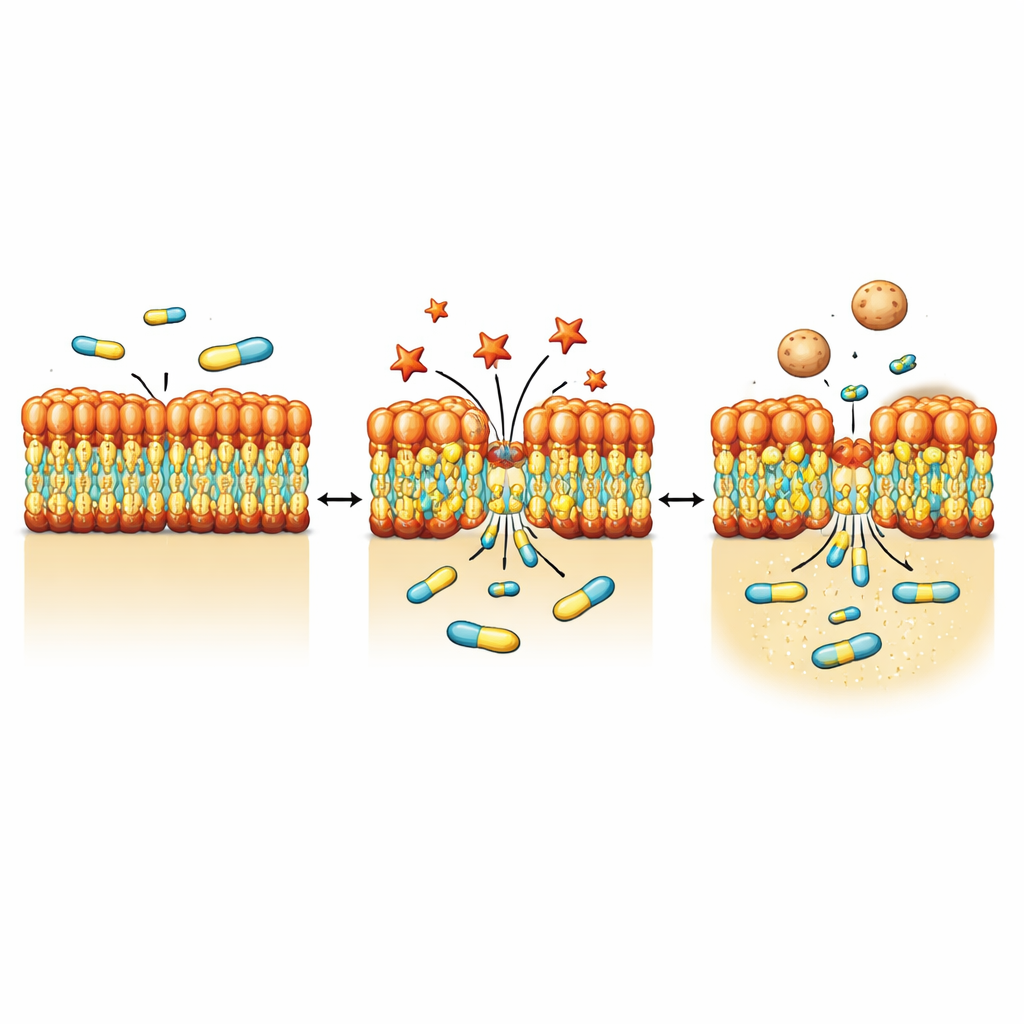
Om te zien hoe bacteriën fysiek reageren op NV716, gebruikte het team hoogresolutie-beeldvormingstechnieken, waaronder elektronenmicroscopie en zachte röntgentomografie. Na blootstelling aan NV716 vertoonde P. aeruginosa kleine uitstulpingen en plekjes die van het oppervlak afsnoerden, waarbij talrijke outer membrane vesicles ontstonden—kleine bolvormige blaasjes gemaakt van hetzelfde materiaal als de buitenste laag. Metingen op populatieniveau bevestigden dat de productie van vesicles ongeveer met een orde van grootte toenam. Gedetailleerde beeldvorming en proteïneanalyses wezen uit dat deze blaasjes componenten van het buitenmembraan zoals porineiwitten en LPS bevatten, maar weinig detecteerbaar DNA, wat consistent is met het afsnoeren van het oppervlak in plaats van barsten van binnenuit. Tegelijkertijd toonde een koper-getagde versie van NV716 aan dat de verbinding zich concentreert in het membraangebied in plaats van vrij door het celinterieur te diffunderen.
Van petrischaaltjes naar levende gastheren
Aangezien sterke effecten in reageerbuizen niet altijd vertaald worden naar levende organismen, evalueerden de onderzoekers de combinatie NV716–doxycycline in een infectiemodel met larven van de wasmot Galleria mellonella. Larven behandeld met de combinatie toonden een trend naar betere overleving vergeleken met alleen doxycycline, hoewel de verbetering onder de geteste condities niet statistisch significant was. Computergebaseerde voorspellingen van medicijnachtige eigenschappen suggereren dat NV716 kenmerken heeft die overeenkomen met interactie met membranen en mogelijk verdraagbaar zijn in dieren, maar grondige veiligheids- en doseringsstudies moeten nog worden uitgevoerd. De auteurs zien NV716 vooral als een proof-of-concept: een molecule die aantoont wat mogelijk is wanneer de bacteriële envelop selectief wordt gemoduleerd in plaats van vernietigd.
Wat dit betekent voor het bestrijden van hardnekkige infecties
In gewone bewoordingen toont dit werk aan dat het mogelijk is het slot te ‘kraken’ van een moeilijk te penetreren bacterie zoals P. aeruginosa zonder de deur te forceren. NV716 nestelt zich in de buitenste schaal van de microbe en herschikt subtiel de structuur zodat bepaalde antibiotica, vooral doxycycline, sneller en in grotere hoeveelheden naar binnen kunnen glippen. De bacteriën reageren door extra stukjes van hun buitenlaag af te werpen in de vorm van vesicles—signalen van stress maar geen totale ineenstorting. Hoewel de eerste dierproeven bescheiden zijn, levert de studie een kwantitatief stappenplan voor het ontwerpen van nieuwe hulpmoleculen en hybride medicijnen die het buitenmembraan als doel hebben. Zulke strategieën kunnen de bruikbare levensduur van bestaande antibiotica verlengen en artsen nieuwe opties bieden tegen enkele van de meest hardnekkige ziekenhuisinfecties.
Bronvermelding: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Trefwoorden: antimicrobiële resistentie, Pseudomonas aeruginosa, buitenmembraan, antibioticum-adjuvans, doxycycline