Clear Sky Science · pt
NV716 age como um adjuvante que atua na envelopagem e aumenta o acúmulo de antibiótico em Pseudomonas aeruginosa
Por que esta pesquisa importa para os antibióticos do futuro
Infecções bacterianas resistentes a medicamentos estão aumentando mais rápido do que novos antibióticos podem ser descobertos, e alguns dos agentes mais difíceis são bactérias Gram‑negativas como Pseudomonas aeruginosa. Esses microrganismos se envolvem com uma capa externa formidável que mantém muitos medicamentos do lado de fora. Este estudo investiga um composto auxiliar, chamado NV716, que por si só não mata bactérias, mas as deixa muito mais vulneráveis a certos antibióticos existentes. Entender como um auxiliar desses funciona pode abrir uma via prática para resgatar drogas que já possuímos em vez de esperar décadas por novas totalmente inéditas.
Um parceiro químico que ajuda os antibióticos a entrar
Os pesquisadores focaram no NV716, uma molécula carregada positivamente e com afinidade por membranas, conhecida por aumentar a atividade de vários antibióticos contra bactérias Gram‑negativas. Eles testaram NV716 em combinação com drogas de famílias diferentes, como tetraciclinas e fluoroquinolonas, contra P. aeruginosa e Escherichia coli. O efeito mais dramático foi observado com a doxiciclina: quando combinada com NV716, a quantidade de doxiciclina necessária para interromper o crescimento bacteriano caiu em mais de cem vezes em P. aeruginosa. Ao medir a fluorescência do antibiótico dentro das células bacterianas, a equipe mostrou que esse aumento no poder de matar acompanha de perto uma elevação em quanto da doxiciclina realmente se acumula nos microrganismos.
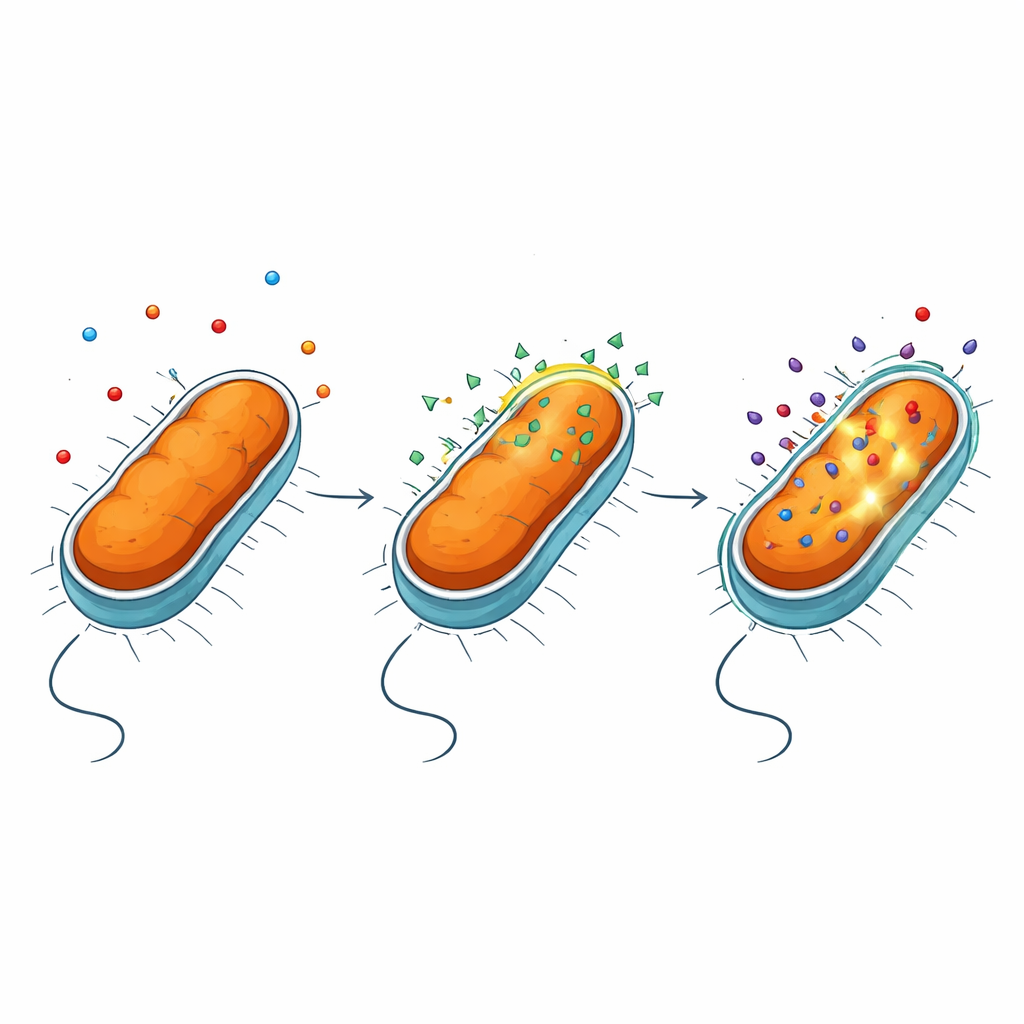
Abrindo o escudo externo sem romper a célula
Bactérias Gram‑negativas são protegidas por uma membrana externa rica em uma molécula complexa chamada lipopolissacarídeo, ou LPS. Essa camada age como um filtro altamente seletivo, bloqueando muitos medicamentos. Usando uma série de ensaios de fluorescência e linhagens mutantes, os autores descobriram que NV716 não desativa de forma perceptível as bombas de efluxo bacterianas—as máquinas moleculares que expulsam antibióticos. Em vez disso, NV716 altera o comportamento da própria membrana externa. Ele se liga ao LPS na superfície celular e afrouxa o empacotamento dessas moléculas, especialmente quando o “core” de açúcar do LPS é encurtado e a porção lipídica subjacente fica mais exposta. Essa perturbação controlada torna a membrana mais fácil de ser atravessada pela doxiciclina e por alguns outros antibióticos, sem rasgar a célula ou danificar a membrana interna onde ocorrem processos vitais.
Visualizando estresse na membrana e desprendimento em forma de bolhas
Para ver como as bactérias respondem fisicamente ao NV716, a equipe recorreu a métodos de imagem de alta resolução, incluindo microscopia eletrônica e tomografia por raios X suaves. Após a exposição ao NV716, P. aeruginosa apresentou pequenas protrusões e áreas que brotam da superfície, formando numerosas vesículas da membrana externa—minúsculas bolhas esféricas feitas do mesmo material da camada externa. Medições em escala populacional confirmaram que a produção de vesículas aumentou em aproximadamente uma ordem de grandeza. Imagens detalhadas e análises proteicas indicaram que essas vesículas carregam componentes da membrana externa, como proteínas porinas e LPS, mas pouco DNA detectável, consistente com um processo de brotamento da superfície em vez de ruptura a partir do interior. Ao mesmo tempo, uma versão marcada com cobre do NV716 revelou que o composto se concentra na região da membrana em vez de difundir livremente pelo interior da célula.
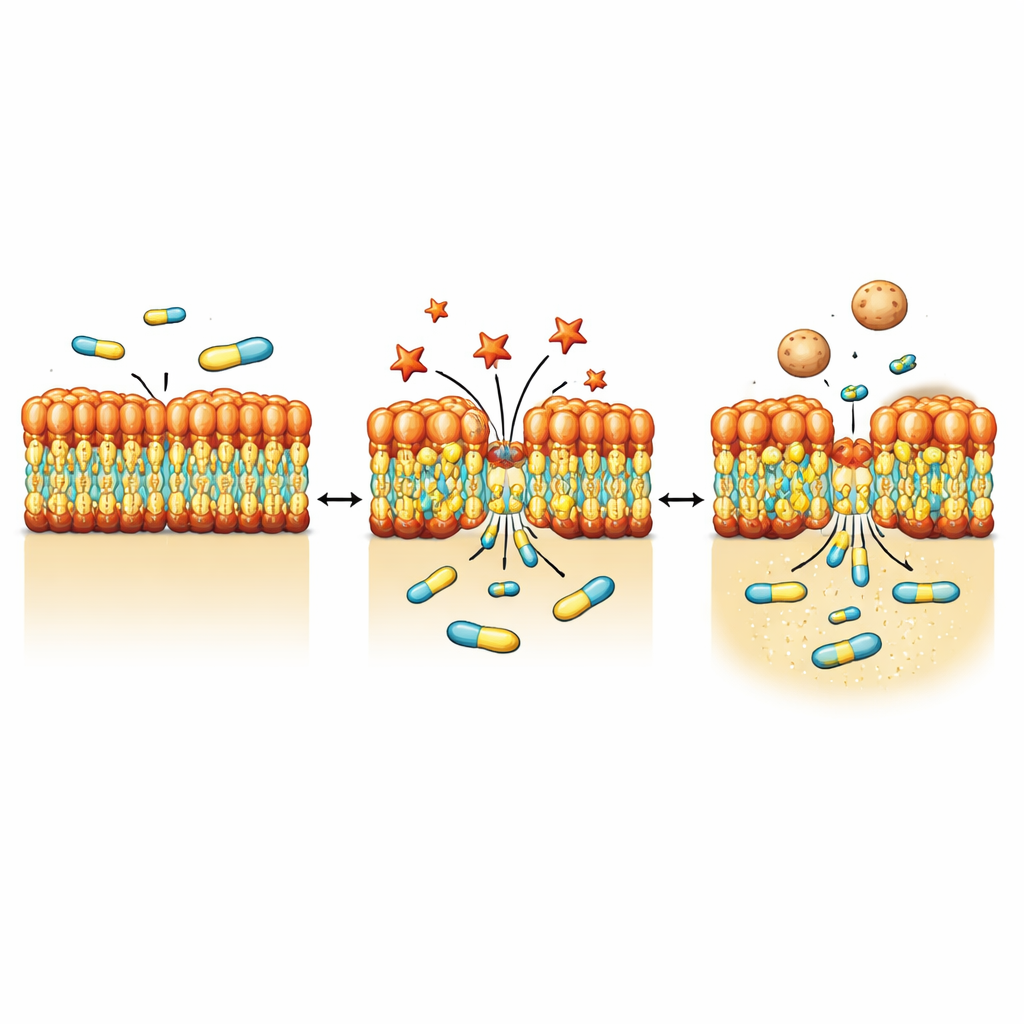
Do ambiente de placa para hospedeiros vivos
Como efeitos fortes em tubos de ensaio nem sempre se traduzem em organismos vivos, os pesquisadores avaliaram a combinação NV716–doxiciclina em um modelo de infecção usando larvas da mariposa cera Galleria mellonella. Larvas tratadas com a combinação mostraram uma tendência a maior sobrevivência em comparação com a doxiciclina isolada, embora a melhora não tenha sido estatisticamente significativa nas condições testadas. Previsões computacionais de propriedades tipo‑fármaco sugerem que o NV716 tem características compatíveis com interação com membranas e pode ser tolerável em animais, mas estudos completos de segurança e dosagem ainda precisam ser realizados. Os autores veem o NV716 principalmente como uma prova de conceito: uma molécula que demonstra o que é possível quando a envoltura bacteriana é modulada seletivamente em vez de destruída.
O que isso significa para enfrentar infecções difíceis
Em termos práticos, este trabalho mostra que é possível “abrir a fechadura” de uma bactéria de difícil penetração como P. aeruginosa sem derrubar a porta. NV716 se instala na capa externa do microrganismo, reorganizando sutilmente sua estrutura para que certos antibióticos, especialmente a doxiciclina, possam entrar mais rápido e em quantidades maiores. As bactérias respondem desprendendo fragmentos extras de seu revestimento externo na forma de vesículas—sinais de estresse, mas não de colapso total. Embora os primeiros testes em animais sejam modestos, o estudo fornece um roteiro quantitativo para projetar novas moléculas auxiliares e fármacos híbridos que tenham como alvo a membrana externa. Estratégias assim poderiam estender a vida útil de antibióticos existentes e dar aos clínicos novas opções contra algumas das infecções hospitalares mais persistentes.
Citação: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Palavras-chave: resistência antimicrobiana, Pseudomonas aeruginosa, membrana externa, adjuvante de antibiótico, doxiciclina