Clear Sky Science · fr
NV716 agit comme un adjuvant actif sur l’enveloppe qui augmente l’accumulation d’antibiotique dans Pseudomonas aeruginosa
Pourquoi cette recherche compte pour les antibiotiques de demain
Les infections bactériennes résistantes aux médicaments augmentent plus vite que la découverte de nouveaux antibiotiques, et certains des agents les plus redoutables sont des bactéries à Gram négatif comme Pseudomonas aeruginosa. Ces microbes se protègent par une enveloppe externe redoutable qui empêche l’entrée de nombreux médicaments. Cette étude explore un composé auxiliaire, nommé NV716, qui ne tue pas les bactéries à lui seul mais les rend beaucoup plus vulnérables à certains antibiotiques existants. Comprendre comment fonctionne un tel auxiliaire pourrait ouvrir une voie pratique pour sauver des médicaments que nous possédons déjà, plutôt que d’attendre des décennies pour en développer de tout nouveaux.
Un partenaire chimique qui aide les antibiotiques à pénétrer
Les chercheurs se sont concentrés sur NV716, une molécule chargée positivement et attirée par les membranes, connue auparavant pour potentialiser l’activité de plusieurs antibiotiques contre les bactéries à Gram négatif. Ils ont testé NV716 conjointement avec des médicaments de familles différentes, comme les tétracyclines et les fluoroquinolones, contre P. aeruginosa et Escherichia coli. L’effet le plus spectaculaire a été observé avec la doxycycline : combinée à NV716, la quantité de doxycycline nécessaire pour arrêter la croissance bactérienne a chuté de plus de cent fois chez P. aeruginosa. En mesurant la fluorescence de l’antibiotique à l’intérieur des cellules bactériennes, l’équipe a montré que cette augmentation de l’efficacité coïncide étroitement avec une hausse de l’accumulation réelle de doxycycline au sein des microbes.
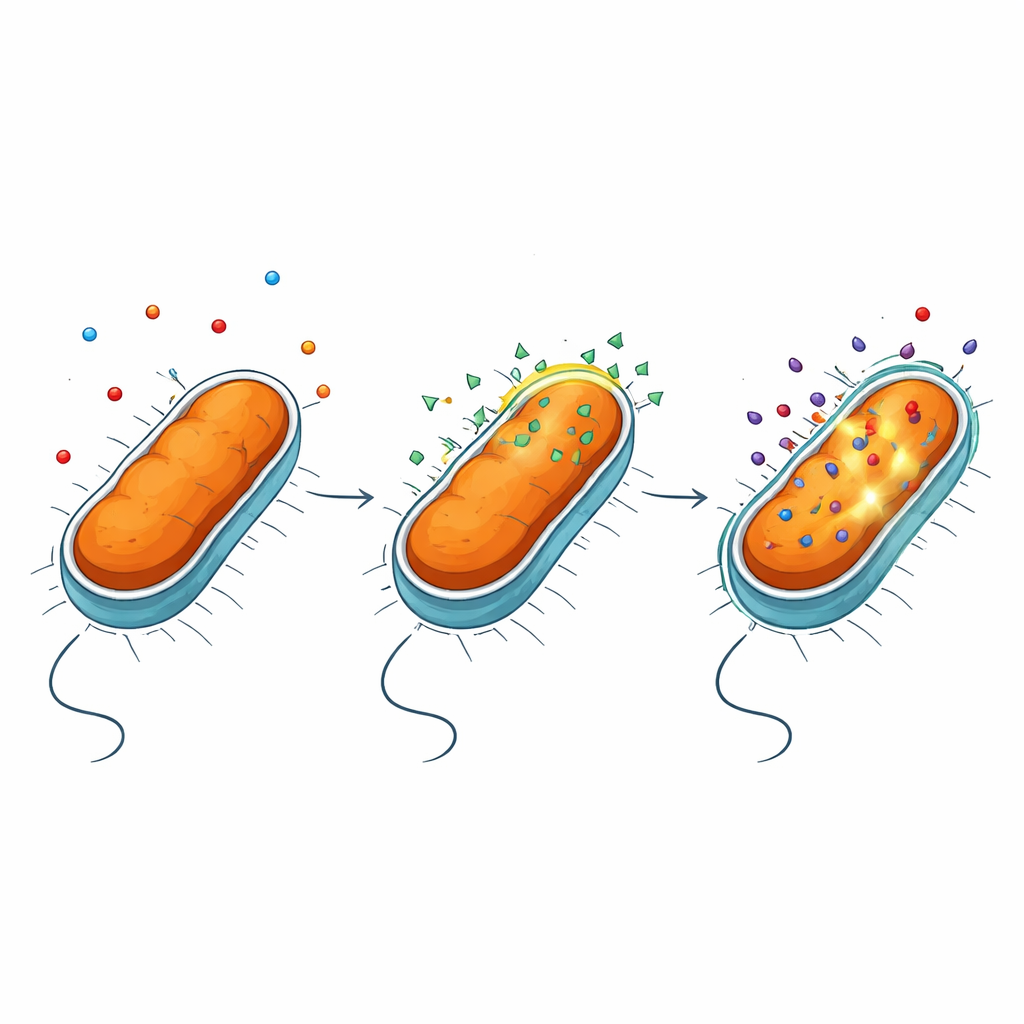
Ouvrir le bouclier externe sans rompre la cellule
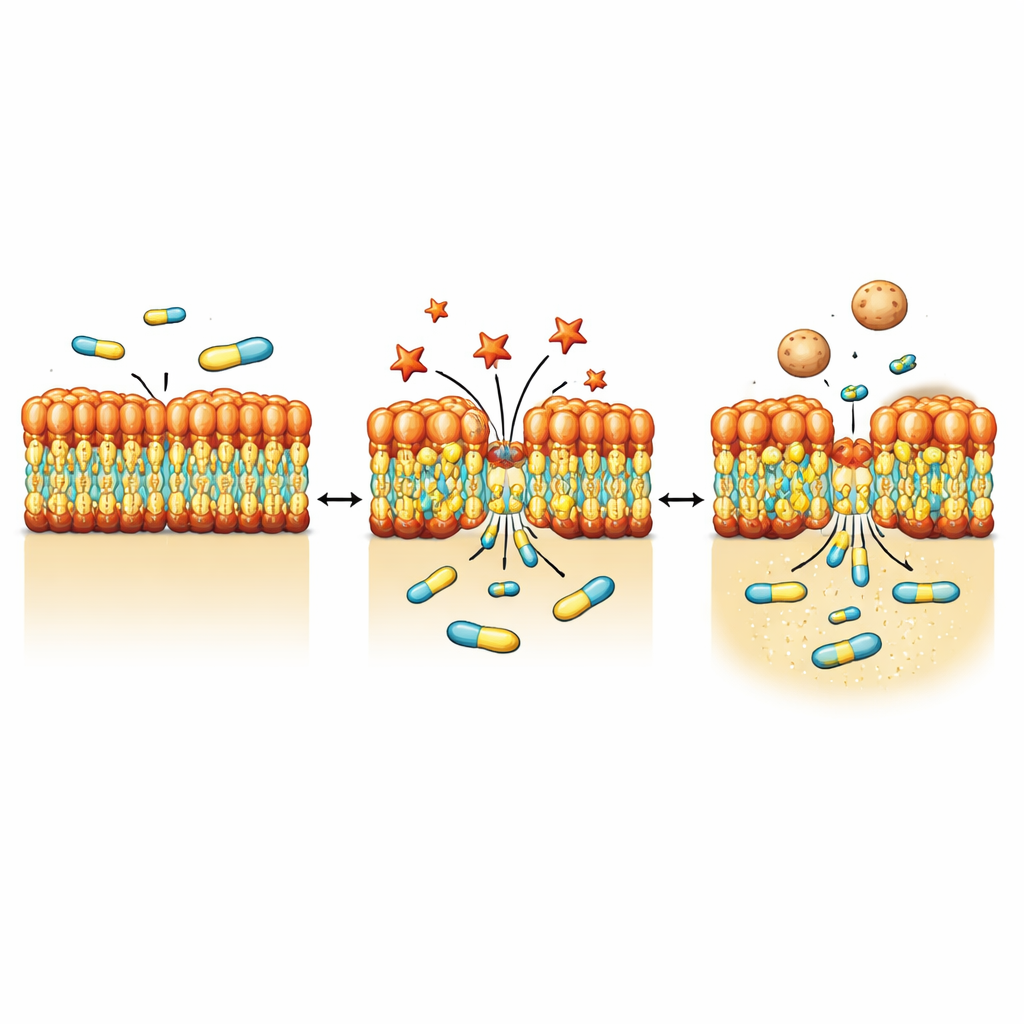
Les bactéries à Gram négatif sont protégées par une membrane externe riche en une molécule complexe appelée lipopolysaccharide, ou LPS. Cette couche agit comme un filtre hautement sélectif, bloquant de nombreux médicaments. À l’aide d’une série de tests de fluorescence et de souches mutantes, les auteurs ont constaté que NV716 ne bloque pas de manière notable les pompes d’efflux bactériennes — les machines moléculaires qui expulsent les antibiotiques. Au contraire, NV716 modifie le comportement de la membrane externe elle‑même. Il se lie au LPS à la surface cellulaire et desserre le compactage de ces molécules, en particulier lorsque le noyau sucré du LPS est raccourci et que la partie lipidique sous‑jacente est plus exposée. Cette perturbation contrôlée rend la membrane plus perméable à la doxycycline et à certains autres antibiotiques, sans déchirer la cellule ni endommager la membrane interne où se déroulent des processus vitaux.
Visualiser le stress membranaire et l’exfoliation en vésicules
Pour observer la réponse physique des bactéries à NV716, l’équipe a eu recours à des méthodes d’imagerie haute résolution, notamment la microscopie électronique et la tomographie par rayons X mous. Après exposition à NV716, P. aeruginosa présentait de petites protrusions et des zones qui bourgeonnent à la surface, formant de nombreuses vésicules de membrane externe — de minuscules bulles sphériques constituées du même matériau que la coque externe. Des mesures à l’échelle de la population ont confirmé que la production de vésicules augmentait d’environ un ordre de grandeur. L’imagerie détaillée et les analyses protéiques ont indiqué que ces vésicules transportent des composants de la membrane externe tels que des porines et du LPS, mais peu d’ADN détectable, ce qui est cohérent avec un bourgeonnement depuis la surface plutôt qu’une rupture interne. Parallèlement, une version de NV716 marquée au cuivre a révélé que le composé se concentre dans la région membranaire plutôt que de diffuser librement à l’intérieur de la cellule.
Des boîtes de Pétri aux organismes vivants
Parce que des effets marqués en éprouvette ne se traduisent pas toujours chez des organismes vivants, les chercheurs ont évalué l’association NV716–doxycycline dans un modèle d’infection utilisant des larves de la teigne de la cire Galleria mellonella. Les larves traitées par la combinaison ont montré une tendance à une meilleure survie par rapport à la doxycycline seule, bien que l’amélioration n’ait pas été statistiquement significative dans les conditions testées. Des prédictions informatiques des propriétés « drug‑like » suggèrent que NV716 présente des caractéristiques compatibles avec une interaction avec les membranes et pourrait être tolérable chez les animaux, mais des études approfondies de sécurité et de posologie restent nécessaires. Les auteurs considèrent NV716 principalement comme une preuve de concept : une molécule qui démontre ce qui est possible lorsque l’enveloppe bactérienne est modulée de façon sélective plutôt que détruite.
Ce que cela signifie pour combattre les infections tenaces
En termes simples, ce travail montre qu’il est possible de « crocheter » la serrure d’une bactérie difficile à pénétrer comme P. aeruginosa sans enfoncer la porte. NV716 s’insère dans la coque externe du microbe, réorganisant subtilement sa structure de sorte que certains antibiotiques, en particulier la doxycycline, puissent s’y introduire plus rapidement et en plus grande quantité. Les bactéries réagissent en perdant des morceaux supplémentaires de leur manteau externe sous forme de vésicules — signes de stress mais non d’effondrement total. Bien que les premiers tests sur animaux soient modestes, l’étude fournit une feuille de route quantitative pour concevoir de nouveaux agents auxiliaires et des médicaments hybrides ciblant la membrane externe. De telles stratégies pourraient prolonger la durée d’efficacité des antibiotiques existants et offrir aux cliniciens de nouvelles options contre certaines des infections nosocomiales les plus tenaces.
Citation: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Mots-clés: résistance aux antimicrobiens, Pseudomonas aeruginosa, membrane externe, adjuvant d’antibiotique, doxycycline