Clear Sky Science · ru
NV716 действует как адъювант, активный на оболочку, который усиливает накопление антибиотика в Pseudomonas aeruginosa
Почему это исследование важно для будущих антибиотиков
Инфекции, вызванные лекарственно-устойчивыми бактериями, растут быстрее, чем удаётся открывать новые антибиотики; одними из самых труднопреодолимых являются грамотрицательные бактерии, такие как Pseudomonas aeruginosa. Эти микроорганизмы окружены прочной наружной оболочкой, которая препятствует проникновению многих лекарств. В работе исследуют вспомогательное соединение NV716, которое само по себе не убивает бактерии, но значительно повышает их чувствительность к некоторым существующим антибиотикам. Понимание механизма действия такого помощника может открыть практический путь к спасению уже имеющихся препаратов, не дожидаясь десятилетий создания совершенно новых.
Химический партнёр, который помогает антибиотикам проникнуть внутрь
Исследователи сосредоточились на NV716 — положительно заряженной молекуле, стремящейся к мембранам, ранее показавшей способность усиливать действие ряда антибиотиков против грамотрицательных бактерий. Они тестировали NV716 в сочетании с препаратами из разных семейств, такими как тетрациклины и фторхинолоны, против P. aeruginosa и Escherichia coli. Наиболее впечатляющий эффект наблюдался с антибиотиком доксициклином: в сочетании с NV716 количество доксициклина, необходимое для остановки роста бактерий, снизилось более чем в сто раз в P. aeruginosa. Измеряя флуоресценцию антибиотика внутри бактериальных клеток, команда показала, что усиление бактерицидного эффекта тесно коррелирует с резким увеличением накопления доксициклина внутри микробов.
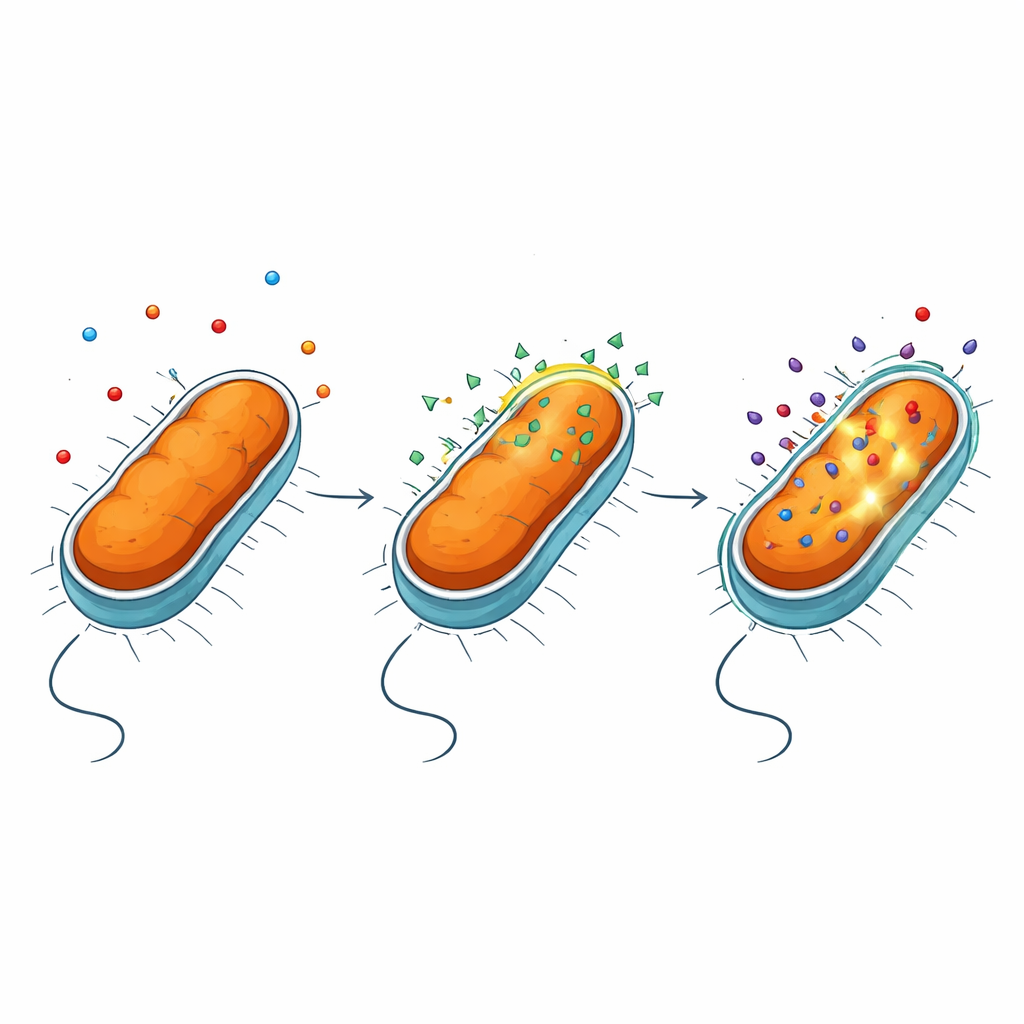
Открывая внешнюю защиту без разрушения клетки
Грамотрицательные бактерии защищены внешней мембраной, богатой сложной молекулой липополисахаридом (LPS). Этот слой действует как высокоселективный фильтр, блокируя многие лекарства. С помощью серии флуоресцентных анализов и мутантных штаммов авторы установили, что NV716 заметно не подавляет работу выталкивающих помп — молекулярных машин, выводящих антибиотики. Вместо этого NV716 изменяет свойства самой внешней мембраны. Он связывается с LPS на поверхности клетки и ослабляет упаковку этих молекул, особенно когда «ядро» сахара в LPS укорочено и обнажается липидная часть. Такое контролируемое нарушение делает мембрану более проницаемой для доксициклина и некоторых других антибиотиков, не разрывая клетку и не повреждая внутреннюю мембрану, где происходят жизненно важные процессы.
Визуализация стресса мембраны и образования пузырьковидных везикул
Чтобы увидеть, как бактерии физически реагируют на NV716, команда использовала методы высокоразрешающей визуализации, включая электронную микроскопию и мягкотельную рентгеновскую томографию. После воздействия NV716 у P. aeruginosa появились небольшие выступы и участки, отщепляющиеся от поверхности, формируя многочисленные везикулы внешней мембраны — крошечные сферические пузырьки из того же материала, что и наружная оболочка. Измерения на уровне популяции подтвердили, что производство везикул возросло примерно в десять раз. Детальная визуализация и белковый анализ показали, что эти везикулы содержат компоненты внешней мембраны, такие как пориновые белки и LPS, но мало обнаруживаемой ДНК, что согласуется с их образованием путём отщепления с поверхности, а не разрыва изнутри. В то же время медью меченая версия NV716 показала, что само соединение концентрируется в области мембраны, а не свободно диффундирует по внутреннему объёму клетки.
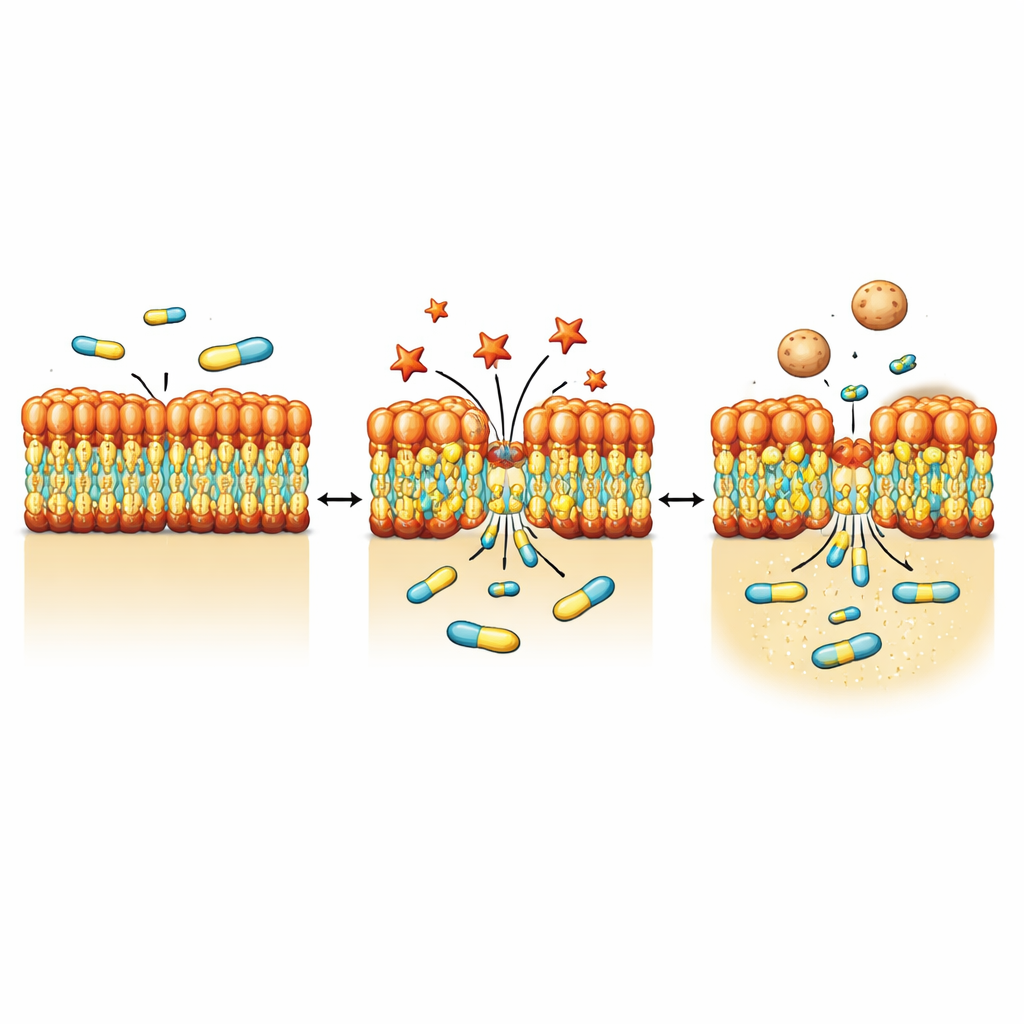
От лабораторных чашек к живым хозяевам
Поскольку сильные эффекты в пробирке не всегда переносятся на живые организмы, исследователи оценили сочетание NV716 и доксициклина в модели инфекции на личинках восковой моли Galleria mellonella. Личинки, получавшие комбинацию, продемонстрировали тенденцию к повышению выживаемости по сравнению с доксициклином в одиночку, хотя улучшение не было статистически значимым при исследованных условиях. Компьютерные предсказания лекароподобных свойств указывают, что NV716 обладает чертами, совместимыми с взаимодействием с мембранами и потенциально переносим в животных, но тщательные исследования безопасности и дозирования ещё предстоят. Авторы рассматривают NV716 в первую очередь как доказательство концепции: молекулу, демонстрирующую, что возможно выборочное модулирование бактериальной оболочки вместо её разрушения.
Что это значит для борьбы с тяжёлыми инфекциями
Проще говоря, эта работа показывает, что можно «подобрать ключ» к трудно проницаемой бактерии, такой как P. aeruginosa, не выламывая дверь. NV716 внедряется в наружную оболочку микроба, тонко перестраивая её структуру, так что определённые антибиотики, особенно доксициклин, могут проникать быстрее и в больших количествах. Бактерии отвечают сбрасыванием дополнительных фрагментов внешнего покрова в виде везикул — признаков стресса, но не полного разрушения. Несмотря на то, что первые испытания на животных дали умеренные результаты, исследование предоставляет количественный план для разработки новых вспомогательных молекул и гибридных лекарств, нацеленных на внешнюю мембрану. Такие стратегии могут продлить полезность существующих антибиотиков и дать клиницистам дополнительные варианты против одних из самых упорных внутрибольничных инфекций.
Цитирование: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Ключевые слова: антибиотикорезистентность, Pseudomonas aeruginosa, внешняя мембрана, адъювант для антибиотиков, доксициклин