Clear Sky Science · it
NV716 agisce come un adiuvante che agisce sulla membrana esterna e aumenta l’accumulo di antibiotico in Pseudomonas aeruginosa
Perché questa ricerca conta per i futuri antibiotici
Le infezioni batteriche resistenti ai farmaci stanno crescendo più rapidamente di quanto si scoprano nuovi antibiotici, e alcuni dei colpevoli più difficili sono batteri Gram‑negativi come Pseudomonas aeruginosa. Questi microrganismi si circondano di un robusto involucro esterno che impedisce l’ingresso di molti farmaci. Questo studio esplora un composto aiutante, chiamato NV716, che di per sé non uccide i batteri ma li rende molto più vulnerabili ad alcuni antibiotici esistenti. Capire come funziona un tale aiutante potrebbe aprire una via pratica per recuperare farmaci che già abbiamo invece di aspettare decenni per crearne di completamente nuovi.
Un partner chimico che aiuta gli antibiotici a entrare
I ricercatori si sono concentrati su NV716, una molecola caricata positivamente e che si dirige verso le membrane, già nota per potenziare l’attività di vari antibiotici contro i batteri Gram‑negativi. Hanno testato NV716 insieme a farmaci di famiglie diverse, come le tetracicline e i fluorochinoloni, contro P. aeruginosa e Escherichia coli. L’effetto più drammatico è stato osservato con la doxiciclina: in combinazione con NV716, la quantità di doxiciclina necessaria per arrestare la crescita batterica è diminuita di oltre cento volte in P. aeruginosa. Misurando la fluorescenza dell’antibiotico all’interno delle cellule batteriche, il gruppo ha mostrato che questo aumento di potenza uccidente corrisponde strettamente a un’impennata di quanto effettivamente la doxiciclina si accumula nei microrganismi.
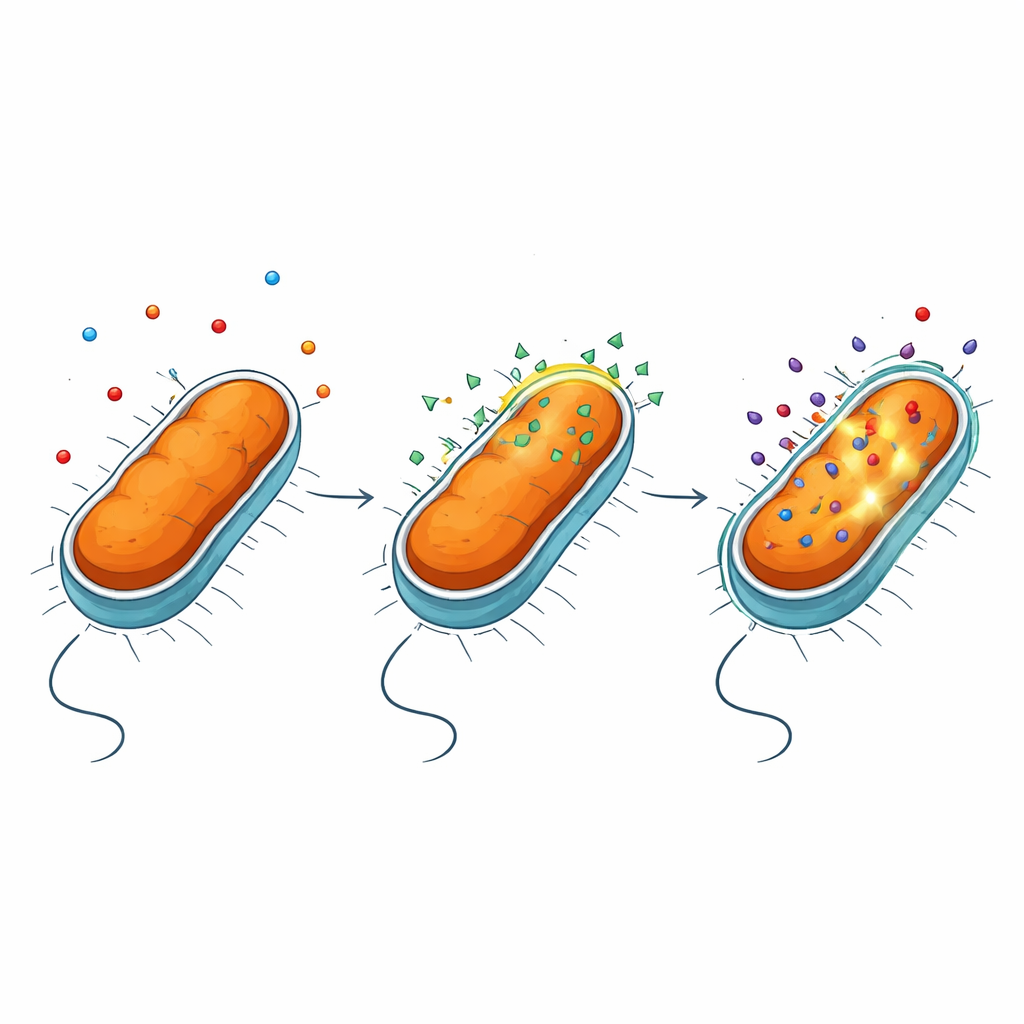
Aprire lo scudo esterno senza lacerare la cellula
I batteri Gram‑negativi sono protetti da una membrana esterna ricca di una molecola complessa chiamata lipopolisaccaride, o LPS. Questo strato funziona come un filtro altamente selettivo, bloccando molti farmaci. Utilizzando una serie di saggi a fluorescenza e ceppi mutanti, gli autori hanno scoperto che NV716 non inibisce in modo significativo le pompe di efflusso dei batteri—le macchine molecolari che espellono gli antibiotici. Al contrario, NV716 modifica il comportamento della membrana esterna stessa. Si lega all’LPS sulla superficie cellulare e allenta l’impacchettamento di queste molecole, soprattutto quando il «core» zuccherino dell’LPS è accorciato e la porzione lipidica sottostante risulta più esposta. Questa perturbazione controllata rende la membrana più permeabile alla doxiciclina e ad alcuni altri antibiotici, senza lacerare la cellula o danneggiare la membrana interna dove avvengono processi vitali.
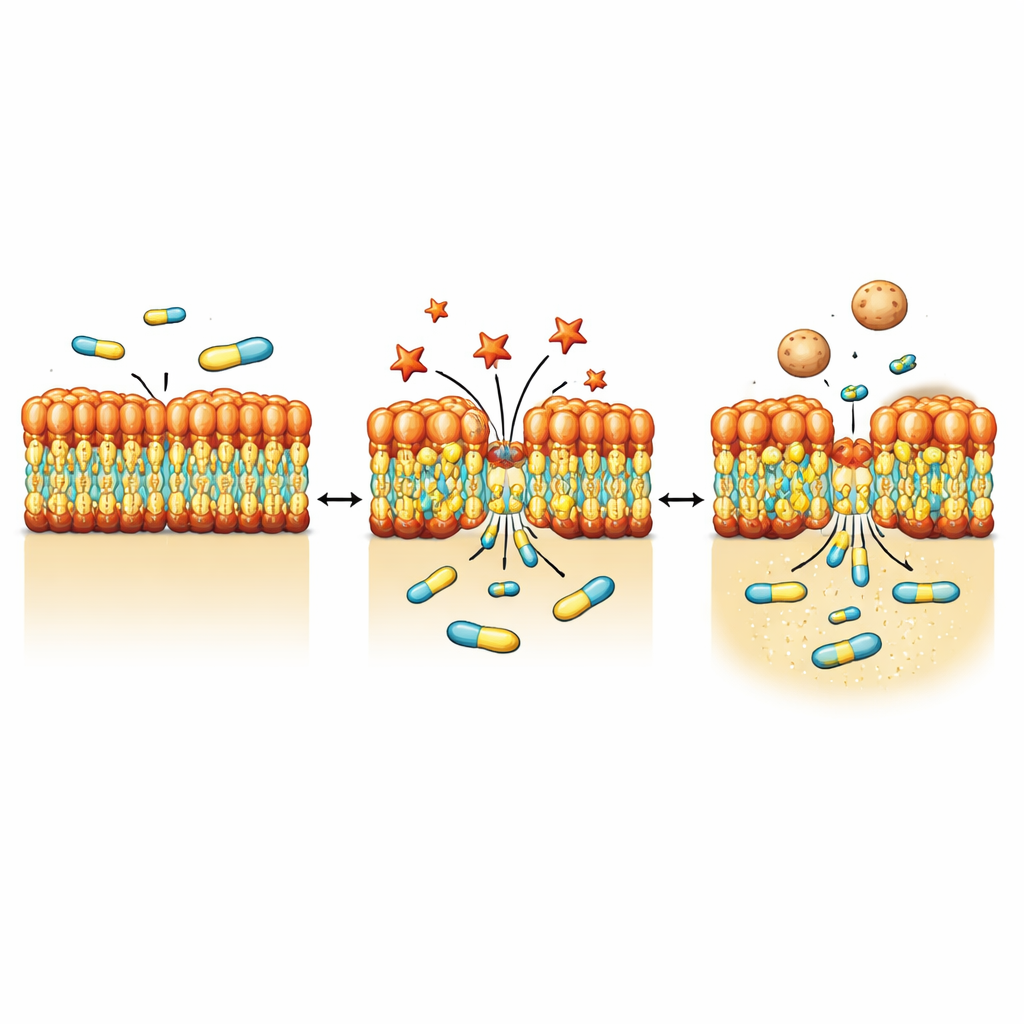
Visualizzare lo stress della membrana e il distacco a forma di bolle
Per vedere come i batteri rispondono fisicamente a NV716, il team ha utilizzato metodi di imaging ad alta risoluzione, tra cui microscopia elettronica e tomografia soft X‑ray. Dopo l’esposizione a NV716, P. aeruginosa ha mostrato piccole protuberanze e zone che si staccano dalla superficie, formando numerose vescicole della membrana esterna—minuscole bolle sferiche fatte dello stesso materiale dell’involucro esterno. Misurazioni su scala di popolazione hanno confermato che la produzione di vescicole è aumentata di circa un ordine di grandezza. Immagini dettagliate e analisi proteiche hanno indicato che queste vescicole contengono componenti della membrana esterna come proteine porine e LPS, ma poco DNA rilevabile, coerente con un loro gemmazione dalla superficie piuttosto che con rotture dall’interno. Allo stesso tempo, una versione di NV716 marcata con rame ha rivelato che il composto si concentra nella regione della membrana piuttosto che diffondere liberamente all’interno della cellula.
Dagli esperimenti in provetta agli ospiti viventi
Poiché effetti forti in provetta non sempre si traducono negli organismi viventi, i ricercatori hanno valutato l’abbinamento NV716–doxiciclina in un modello d’infezione usando larve della falena della cera Galleria mellonella. Le larve trattate con la combinazione hanno mostrato una tendenza a una migliore sopravvivenza rispetto alla doxiciclina da sola, sebbene il miglioramento non fosse statisticamente significativo nelle condizioni testate. Previsioni al computer delle proprietà simili a farmaci suggeriscono che NV716 possiede caratteristiche coerenti con l’interazione con le membrane e potrebbe essere tollerabile negli animali, ma rimangono da svolgere studi approfonditi su sicurezza e dosaggio. Gli autori considerano NV716 principalmente come una prova di principio: una molecola che dimostra cosa è possibile quando l’involucro batterico viene modulato selettivamente anziché distrutto.
Cosa significa per affrontare infezioni difficili
In termini pratici, questo studio mostra che è possibile «scassinare» un batterio difficile da penetrare come P. aeruginosa senza sfondare la porta. NV716 si inserisce nell’involucro esterno del microrganismo, riorganizzandone sottilmente la struttura in modo che certi antibiotici, in particolare la doxiciclina, possano penetrare più rapidamente e in quantità maggiori. I batteri rispondono scartando parti extra del loro rivestimento esterno sotto forma di vescicole—segni di stress ma non di collasso totale. Sebbene i primi test su animali siano modesti, lo studio fornisce un progetto quantitativo per progettare nuovi aiuti molecolari e farmaci ibridi che prendono di mira la membrana esterna. Tali strategie potrebbero prolungare la vita utile degli antibiotici esistenti e offrire ai clinici nuove opzioni contro alcune delle infezioni ospedaliere più ostinate.
Citazione: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Parole chiave: resistenza antimicrobica, Pseudomonas aeruginosa, membrana esterna, adiuvante antibiotico, doxiciclina