Clear Sky Science · de
NV716 wirkt als hüllenwirksamer Adjuvans, das die Antibiotikaakkumulation in Pseudomonas aeruginosa steigert
Warum diese Forschung für künftige Antibiotika wichtig ist
Infektionen durch resistente Bakterien nehmen schneller zu, als neue Antibiotika entdeckt werden, und zu den härtesten Gegnern zählen gramnegative Bakterien wie Pseudomonas aeruginosa. Diese Mikroben umgeben sich mit einer robusten äußeren Hülle, die viele Medikamente draußen hält. In der Studie wird eine Hilfssubstanz, NV716 genannt, untersucht: Sie tötet Bakterien nicht direkt, macht sie aber deutlich verwundbarer gegenüber bestimmten vorhandenen Antibiotika. Zu verstehen, wie ein solcher Helfer wirkt, könnte einen praktischen Weg eröffnen, bereits vorhandene Wirkstoffe zu retten, anstatt Jahrzehnte auf völlig neue zu warten.
Ein chemischer Partner, der Antibiotika ins Innere hilft
Die Forschenden konzentrierten sich auf NV716, ein positiv geladenes, membranaffines Molekül, das bereits vorher dafür bekannt war, die Aktivität mehrerer Antibiotika gegen gramnegative Bakterien zu verstärken. Sie testeten NV716 zusammen mit Wirkstoffen aus verschiedenen Familien, etwa Tetrazykline und Fluorchinolone, gegen P. aeruginosa und Escherichia coli. Den dramatischsten Effekt zeigte das Antibiotikum Doxycyclin: In Kombination mit NV716 sank die Menge an Doxycyclin, die zum Stillstand des bakteriellen Wachstums nötig war, in P. aeruginosa um mehr als das Hundertfache. Durch Messung der Antibiotika‑Fluoreszenz innerhalb bakterieller Zellen zeigte das Team, dass dieser Anstieg der Wirksamkeit eng mit einer Zunahme der tatsächlichen Doxycyclin‑Akkumulation in den Mikroben korreliert.
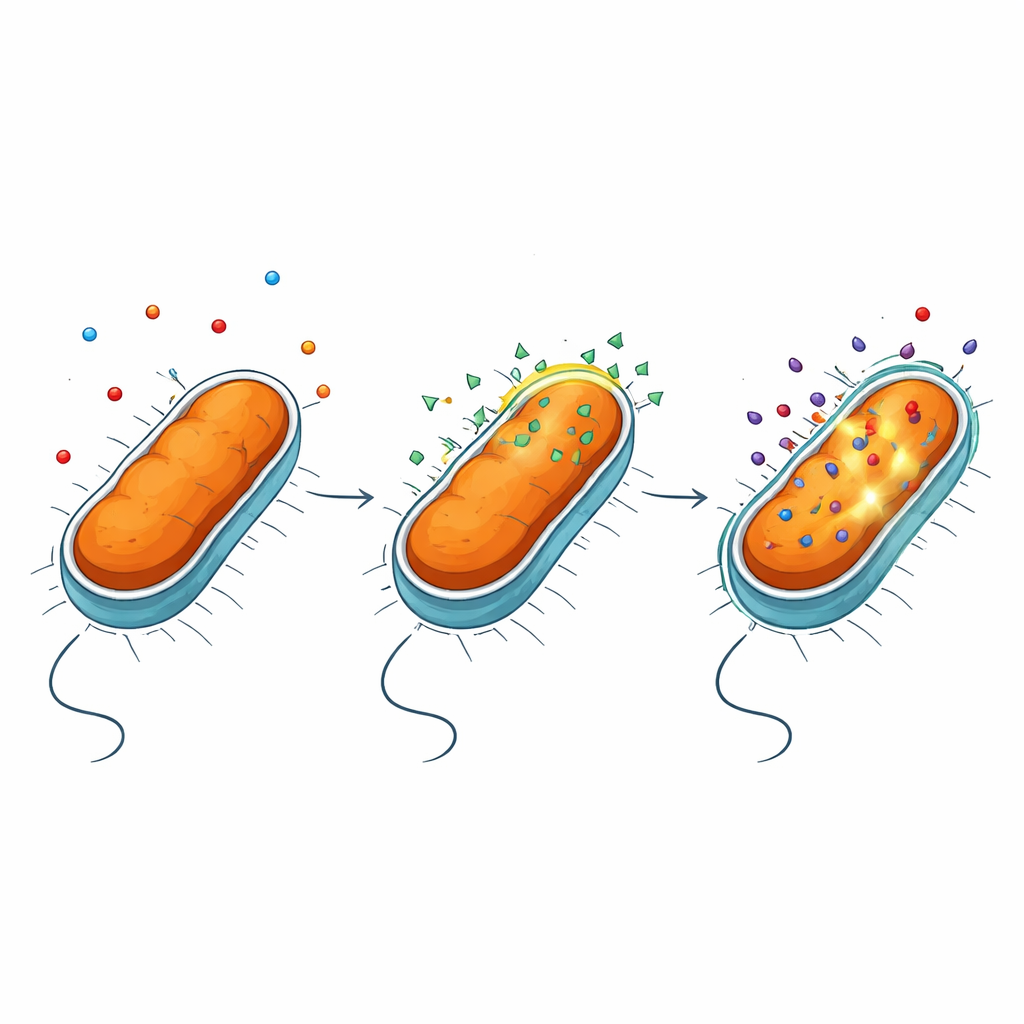
Die äußere Schutzschicht öffnen, ohne die Zelle zu zerstören
Gramnegative Bakterien sind durch eine äußere Membran geschützt, die reich an einem komplexen Molekül namens Lipopolysaccharid (LPS) ist. Diese Schicht wirkt wie ein hochselektiver Filter und blockiert viele Wirkstoffe. Mit einer Reihe von Fluoreszenzassays und Mutantenstämmen fanden die Autorinnen und Autoren heraus, dass NV716 die Effluxpumpen—die molekularen Maschinen, die Antibiotika ausstoßen—nicht merklich hemmt. Stattdessen verändert NV716 das Verhalten der äußeren Membran selbst. Es bindet an LPS an der Zelloberfläche und lockert die Packung dieser Moleküle, insbesondere wenn der Zucker‑„Core“ von LPS verkürzt ist und der zugrunde liegende Lipidanteil stärker exponiert wird. Diese kontrollierte Störung macht die Membran durchlässiger für Doxycyclin und einige andere Antibiotika, ohne die Zelle aufzureißen oder die innere Membran zu schädigen, in der lebenswichtige Prozesse ablaufen.
Membranstress und blasenartiges Abschilfern sichtbar machen
Um zu sehen, wie Bakterien physikalisch auf NV716 reagieren, nutzte das Team hochauflösende Bildgebungsverfahren wie Elektronenmikroskopie und weiche Röntgentomographie. Nach Exposition gegenüber NV716 zeigten P. aeruginosa kleine Vorwölbungen und Abschnürungen an der Oberfläche, die zahlreiche Außenmembranvesikel bildeten—winzige kugelförmige Bläschen aus dem gleichen Material wie die äußere Hülle. Messungen auf Populationsniveau bestätigten, dass die Vesikelproduktion etwa um eine Größenordnung anstieg. Detaillierte Bilder und Proteinanalysen deuteten darauf hin, dass diese Vesikel Bausteine der äußeren Membran wie Porinproteine und LPS enthalten, aber wenig nachweisbare DNA—was konsistent mit einem Abschnüren von der Oberfläche und nicht mit einem Zerplatzen von innen ist. Gleichzeitig zeigte eine kupfermarkierte Version von NV716, dass sich die Verbindung selbst in der Membranregion anreichert statt frei in das Zellinnere zu diffundieren.
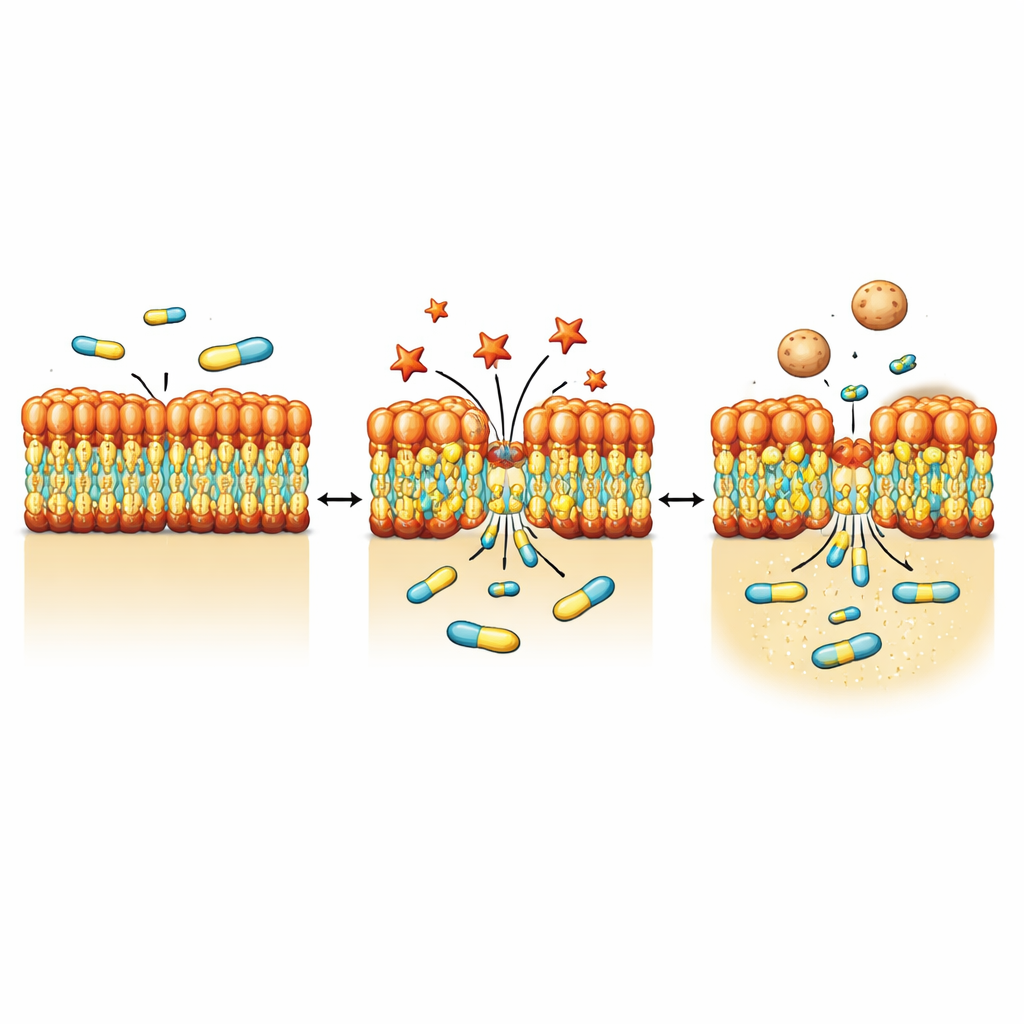
Von Reagenzgläsern zu lebenden Wirten
Weil starke Effekte im Reagenzglas nicht immer auf lebende Organismen übertragbar sind, prüften die Forschenden die Kombination NV716–Doxycyclin in einem Infektionsmodell mit Larven der Wachsraupe Galleria mellonella. Larven, die mit der Kombination behandelt wurden, zeigten einen Trend zu besserem Überleben im Vergleich zu Doxycyclin allein, wobei die Verbesserung unter den getesteten Bedingungen jedoch nicht statistisch signifikant war. Computerbasierte Vorhersagen zu arzneimittelähnlichen Eigenschaften legen nahe, dass NV716 Merkmale aufweist, die mit Membraninteraktionen vereinbar sind und möglicherweise in Tieren tolerierbar sein könnten, aber gründliche Sicherheits‑ und Dosisstudien stehen noch aus. Die Autorinnen und Autoren sehen NV716 vor allem als Konzept‑Beweis: ein Molekül, das demonstriert, was möglich ist, wenn die bakterielle Hülle selektiv moduliert statt zerstört wird.
Was das für die Bekämpfung hartnäckiger Infektionen bedeutet
Alltagsnah ausgedrückt zeigt diese Arbeit, dass es möglich ist, das „Schloss“ einer schwer durchdringbaren Bakterie wie P. aeruginosa zu „knacken“, ohne die Tür einzuschlagen. NV716 nistet sich in die Außenhülle des Erregers ein und verändert deren Struktur so subtil, dass bestimmte Antibiotika, besonders Doxycyclin, schneller und in größeren Mengen eindringen können. Die Bakterien reagieren, indem sie zusätzliche Teile ihrer äußeren Schicht in Form von Vesikeln abstoßen—Anzeichen von Stress, aber kein vollständiger Zusammenbruch. Obwohl die ersten Tierversuche moderat ausfallen, liefert die Studie eine quantitative Blaupause für das Design neuer Helfermoleküle und Hybridwirkstoffe, die die äußere Membran gezielt ansprechen. Solche Strategien könnten die Nutzungsdauer vorhandener Antibiotika verlängern und Klinikerinnen und Klinikern neue Optionen gegen einige der hartnäckigsten Krankenhauskeime bieten.
Zitation: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Schlüsselwörter: antimikrobielle Resistenz, Pseudomonas aeruginosa, äußere Membran, Antibiotika‑Adjuvans, Doxycyclin