Clear Sky Science · pl
NV716 działa jako adjuwant aktywny wobec otoczki, który zwiększa kumulację antybiotyku w Pseudomonas aeruginosa
Dlaczego te badania mają znaczenie dla przyszłych antybiotyków
Zakażenia bakteryjne oporne na leki rosną szybciej niż tempo odkrywania nowych antybiotyków, a jednymi z najtrudniejszych przeciwników są bakterie Gram‑ujemne, takie jak Pseudomonas aeruginosa. Mikroby te otaczają się silną zewnętrzną powłoką, która zatrzymuje wiele leków. W badaniu analizowano związek wspomagający, nazwany NV716, który sam w sobie nie zabija bakterii, ale sprawia, że stają się one znacznie bardziej wrażliwe na niektóre istniejące antybiotyki. Zrozumienie, jak działa taki pomocnik, może otworzyć praktyczną drogę do uratowania leków, które już mamy, zamiast czekać dekady na zupełnie nowe związki.
Chemiczny partner, który pomaga antybiotykom dostać się do wnętrza
Badacze skoncentrowali się na NV716, naładowanej dodatnio, do membran przyciągającej cząsteczce, znanej wcześniej z tego, że wzmacnia aktywność kilku antybiotyków przeciw bakteriom Gram‑ujemnym. Testowano NV716 w połączeniu z lekami z różnych rodzin, takimi jak tetracykliny i fluorochinolony, przeciwko P. aeruginosa i Escherichia coli. Najbardziej dramatyczny efekt zaobserwowano z antybiotykiem doksycykliną: w połączeniu z NV716 ilość doksycykliny potrzebna do zahamowania wzrostu bakterii spadła w P. aeruginosa o ponad sto razy. Poprzez pomiar fluorescencji antybiotyku wewnątrz komórek bakteryjnych zespół wykazał, że wzrost skuteczności leczenia koreluje z ogromnym wzrostem kumulacji doksycykliny wewnątrz drobnoustrojów.
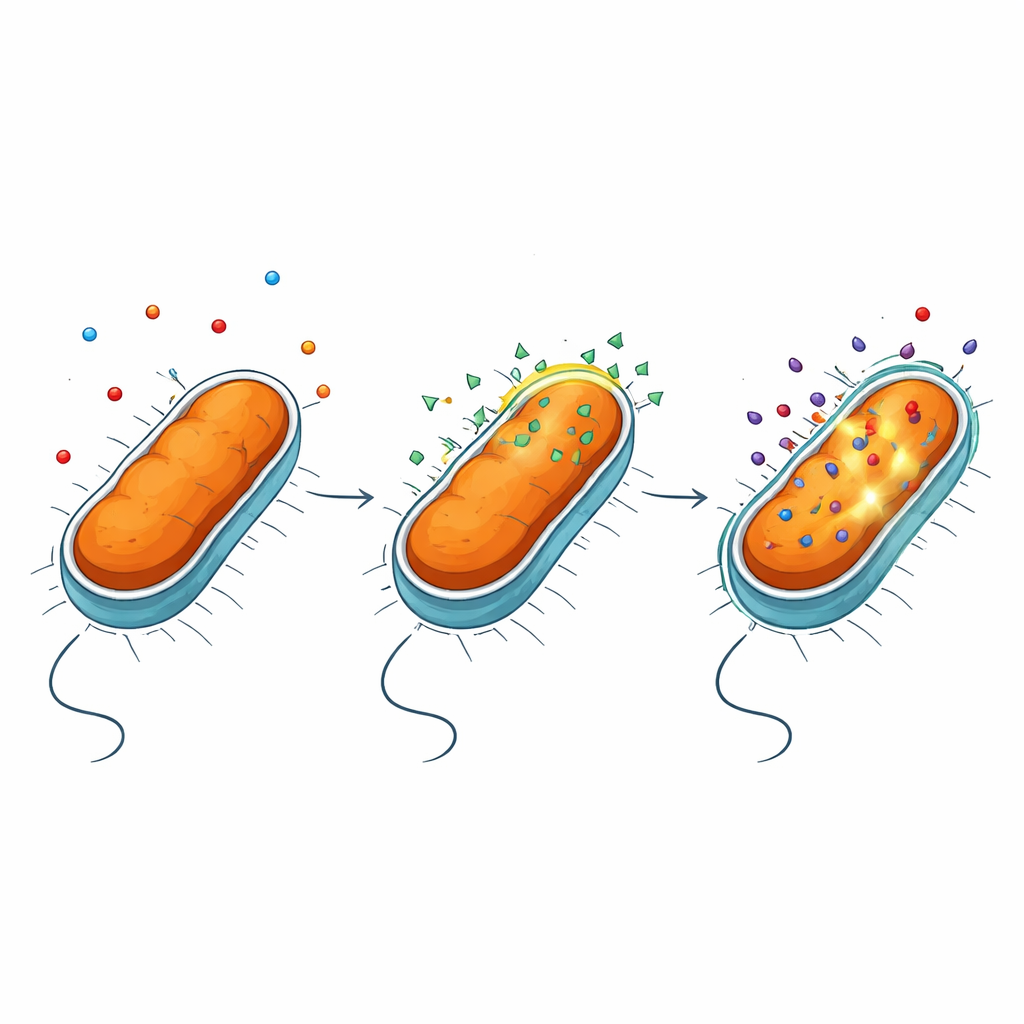
Otwarcie zewnętrznej osłony bez rozrywania komórki
Bakterie Gram‑ujemne są chronione przez błonę zewnętrzną bogatą w złożony związek zwany lipopolisacharydem, czyli LPS. Ta warstwa działa jak wysoce selektywny filtr, blokując wiele leków. Przy użyciu serii testów fluorescencyjnych i szczepów mutantów autorzy odkryli, że NV716 nie hamuje w zauważalny sposób pomp wypompowujących antybiotyki—molekularnych maszyn usuwających leki. Zamiast tego NV716 zmienia zachowanie samej błony zewnętrznej. Wiąże się z LPS na powierzchni komórki i poluzowuje upakowanie tych cząsteczek, szczególnie gdy "rdzeń" cukrowy LPS jest skrócony, a odsłonięta zostaje część lipidowa. To kontrolowane zaburzenie ułatwia przejście doksycykliny i niektórych innych antybiotyków przez błonę, bez rozerwania komórki czy uszkodzenia błony wewnętrznej, gdzie zachodzą kluczowe procesy życiowe.
Wizualizacja stresu błonowego i zrzucania pęcherzykowatego
Aby zobaczyć, jak bakterie fizycznie reagują na NV716, zespół sięgnął po metody obrazowania o wysokiej rozdzielczości, w tym mikroskopię elektronową i miękką tomografię rentgenowską. Po ekspozycji na NV716 P. aeruginosa prezentowała małe wypukłości i odszczepy na powierzchni, tworzące liczne zewnątrzkomórkowe pęcherzyki błonowe—malutkie sferyczne bąbelki zbudowane z tego samego materiału co powłoka zewnętrzna. Pomiary na poziomie populacji potwierdziły, że produkcja pęcherzyków wzrosła mniej więcej o rząd wielkości. Szczegółowe obrazy i analizy białek wykazały, że te pęcherzyki zawierają składniki błony zewnętrznej, takie jak białka porinowe i LPS, ale niewiele wykrywalnego DNA, co wskazuje, że pączkują z powierzchni, a nie pękają ze środka. Jednocześnie wersja NV716 znakowana miedzią ujawniła, że związek koncentruje się w rejonie błony, a nie swobodnie dyfunduje do wnętrza komórki.
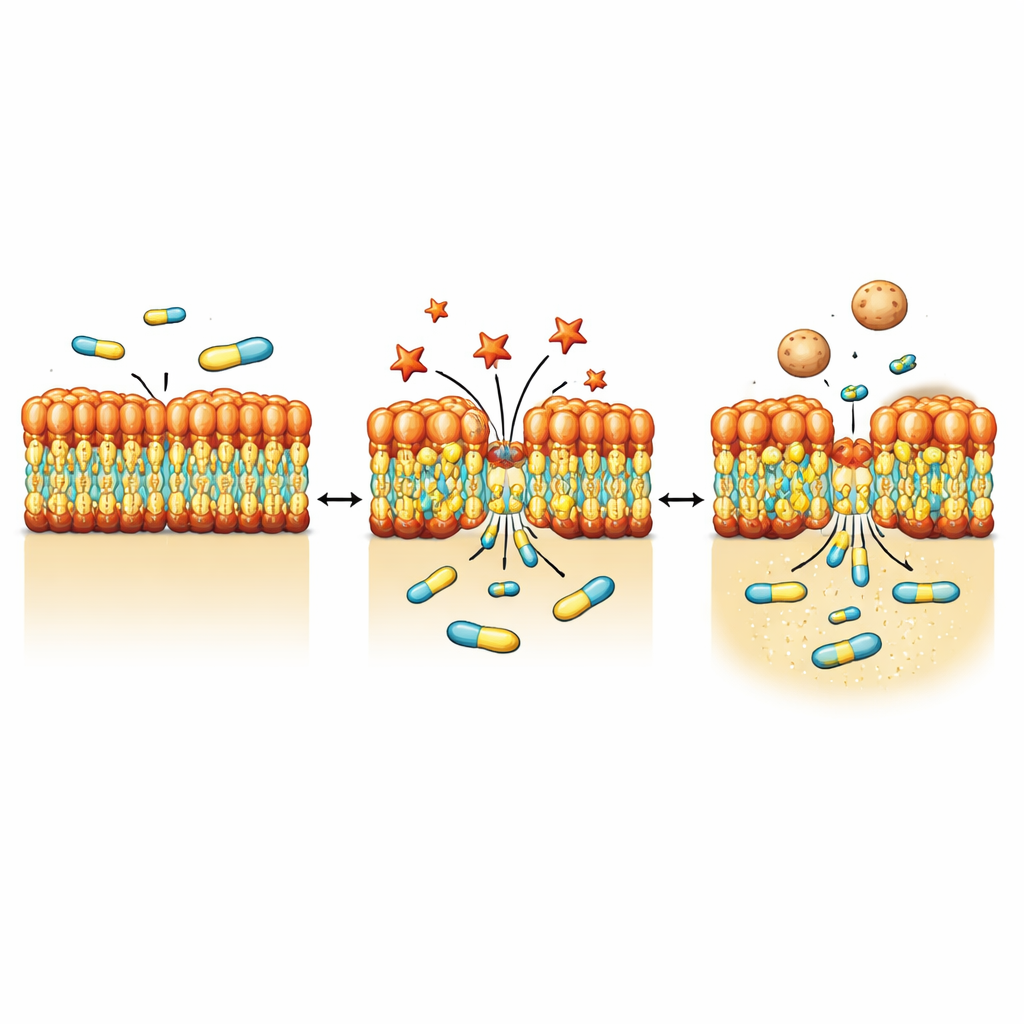
Ze szalek laboratoryjnych do żywych organizmów
Ponieważ silne efekty w probówkach nie zawsze przekładają się na żywe organizmy, badacze ocenili połączenie NV716 i doksycykliny w modelu infekcji z użyciem larw ćmy woskowej Galleria mellonella. Larwy leczone kombinacją wykazały tendencję do lepszych przeżyć w porównaniu z samą doksycykliną, chociaż poprawa nie była statystycznie istotna w testowanych warunkach. Predykcje komputerowe dotyczące właściwości podobnych do leków sugerują, że NV716 ma cechy zgodne z oddziaływaniem z błonami i może być tolerowany u zwierząt, ale konieczne są szczegółowe badania bezpieczeństwa i dawkowania. Autorzy traktują NV716 głównie jako dowód koncepcji: cząsteczkę, która pokazuje, co jest możliwe, gdy osłonę bakteryjną selektywnie się modyfikuje zamiast niszczyć.
Co to oznacza w walce z trudnymi zakażeniami
Mówiąc prostymi słowami, praca ta pokazuje, że można "zdjąć zamek" twardo przenikalnej bakterii takiej jak P. aeruginosa bez rozwalania drzwi. NV716 wkleja się w zewnętrzną powłokę mikroba, subtelnie przestawiając jej strukturę, dzięki czemu niektóre antybiotyki, zwłaszcza doksycyklina, mogą szybciej i w większej ilości przedostać się do środka. Bakterie odpowiadają zrzucaniem dodatkowych fragmentów powłoki w postaci pęcherzyków—oznak stresu, ale nie całkowitego załamania. Choć pierwsze testy na zwierzętach są umiarkowane, badanie dostarcza ilościowego planu działania dla projektowania nowych cząsteczek wspomagających i leków hybrydowych ukierunkowanych na błonę zewnętrzną. Takie strategie mogłyby wydłużyć użyteczność istniejących antybiotyków i dać klinicystom nowe opcje przeciw niektórym z najbardziej uciążliwych zakażeń szpitalnych.
Cytowanie: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Słowa kluczowe: oporność na leki przeciwbakteryjne, Pseudomonas aeruginosa, błona zewnętrzna, adjuwant antybiotykowy, doksycyklina