Clear Sky Science · sv
NV716 fungerar som ett hölje-aktivt adjuvans som ökar antibiotikaackumulering i Pseudomonas aeruginosa
Varför denna forskning är viktig för framtida antibiotika
Läkemedelsresistenta bakterieinfektioner ökar snabbare än nya antibiotika kan upptäckas, och några av de svåraste förövarna är gramnegativa bakterier som Pseudomonas aeruginosa. Dessa mikrober omger sig med ett formidabelt yttre skal som håller många mediciner ute. Denna studie undersöker en hjälpsubstans, kallad NV716, som inte dödar bakterierna själv men gör dem mycket mer sårbara för vissa befintliga antibiotika. Att förstå hur en sådan hjälpare fungerar kan öppna en praktisk väg för att rädda läkemedel vi redan har i stället för att vänta årtionden på helt nya.
En kemisk partner som hjälper antibiotika att ta sig in
Forskarna fokuserade på NV716, en positivt laddad molekyl som söker sig till membraner och som tidigare varit känd för att öka aktiviteten hos flera antibiotika mot gramnegativa bakterier. De testade NV716 tillsammans med läkemedel från olika familjer, såsom tetracykliner och fluorokinoloner, mot P. aeruginosa och Escherichia coli. Den mest dramatiska effekten syntes med antibiotikan doxycyklin: när den kombinerades med NV716 minskade mängden doxycyklin som behövdes för att stoppa bakteriell tillväxt med mer än hundrafalt i P. aeruginosa. Genom att mäta antibiotikans fluorescens inne i bakteriecellerna visade teamet att denna ökade dödlighet korrelerar starkt med en ökning av hur mycket doxycyklin som faktiskt ackumuleras i mikroberna.
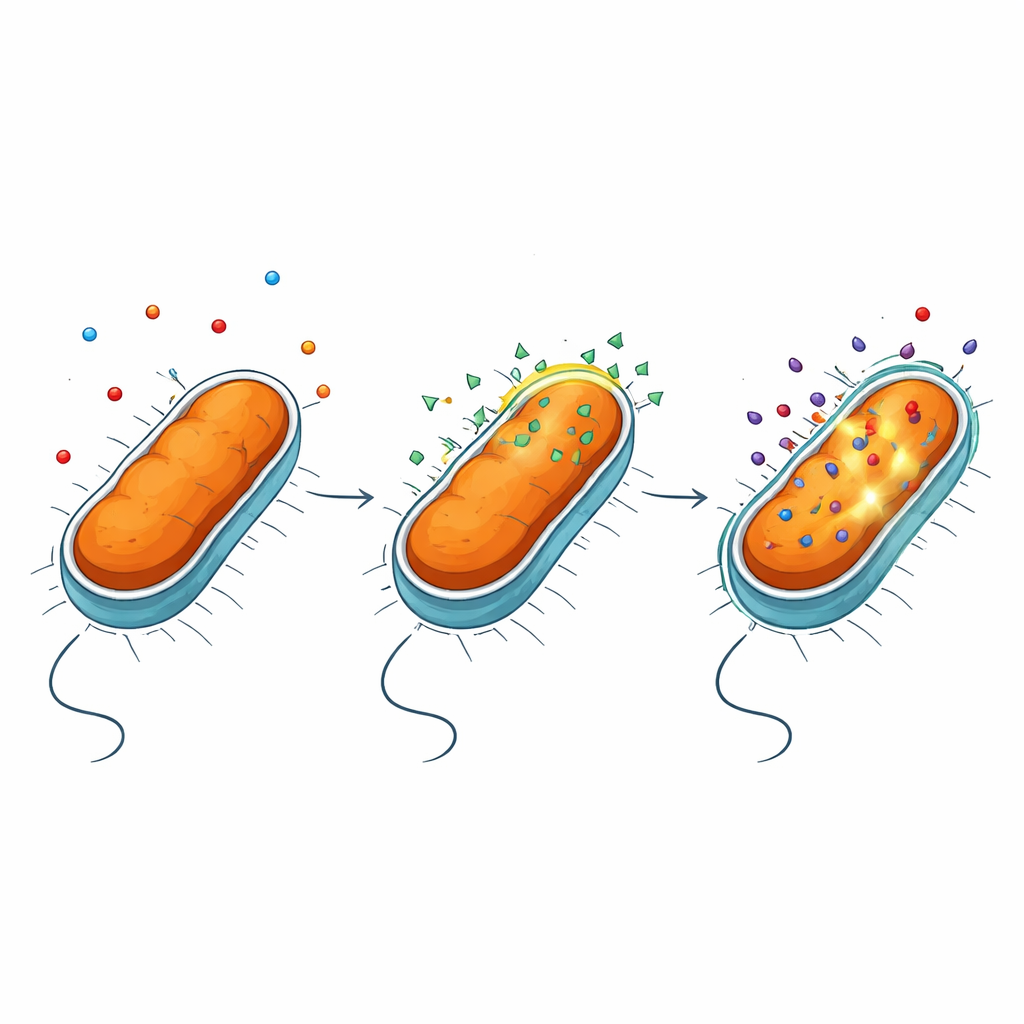
Öppna det yttre skyddet utan att brista cellen
Gramnegativa bakterier skyddas av ett yttre membran rikt på en komplex molekyl kallad lipopolysackarid, eller LPS. Detta lager fungerar som ett mycket selektivt filter och blockerar många läkemedel. Med hjälp av en serie fluorescensanalyser och mutanter fann författarna att NV716 inte märkbart stänger ner bakteriernas effluxpumpar—de molekylära maskiner som pumpar ut antibiotika. Istället förändrar NV716 beteendet hos själva yttre membranet. Det binder till LPS vid cellytan och luckrar upp packningen av dessa molekyler, särskilt när sockerkärnan i LPS är förkortad och den underliggande lipiddelen blir mer exponerad. Denna kontrollerade störning gör membranet lättare för doxycyklin och vissa andra antibiotika att korsa, utan att slita sönder cellen eller skada det inre membranet där viktiga processer sker.
Visualisering av membranstress och bubbelliknande avknoppning
För att se hur bakterier fysiskt svarar på NV716 använde teamet högupplösta bildmetoder inklusive elektronmikroskopi och mjuk röntgentomografi. Efter exponering för NV716 visade P. aeruginosa små utskott och ytor som knoppade av från ytan och bildade ett stort antal yttre membranvesiklar—små sfäriska bubblor gjorda av samma material som höljet. Mätningar på populationsnivå bekräftade att vesikelproduktionen ökade med ungefär en storleksordning. Detaljerad bildanalys och proteinstudier indikerade att dessa vesiklar innehåller komponenter från det yttre membranet såsom porinproteiner och LPS, men lite detekterbart DNA, vilket stämmer överens med att de knoppas av från ytan snarare än att spricka inifrån. Samtidigt visade en kopparmärkt version av NV716 att föreningen själv koncentreras i membranområdet snarare än att fritt diffundera i cellens inre.
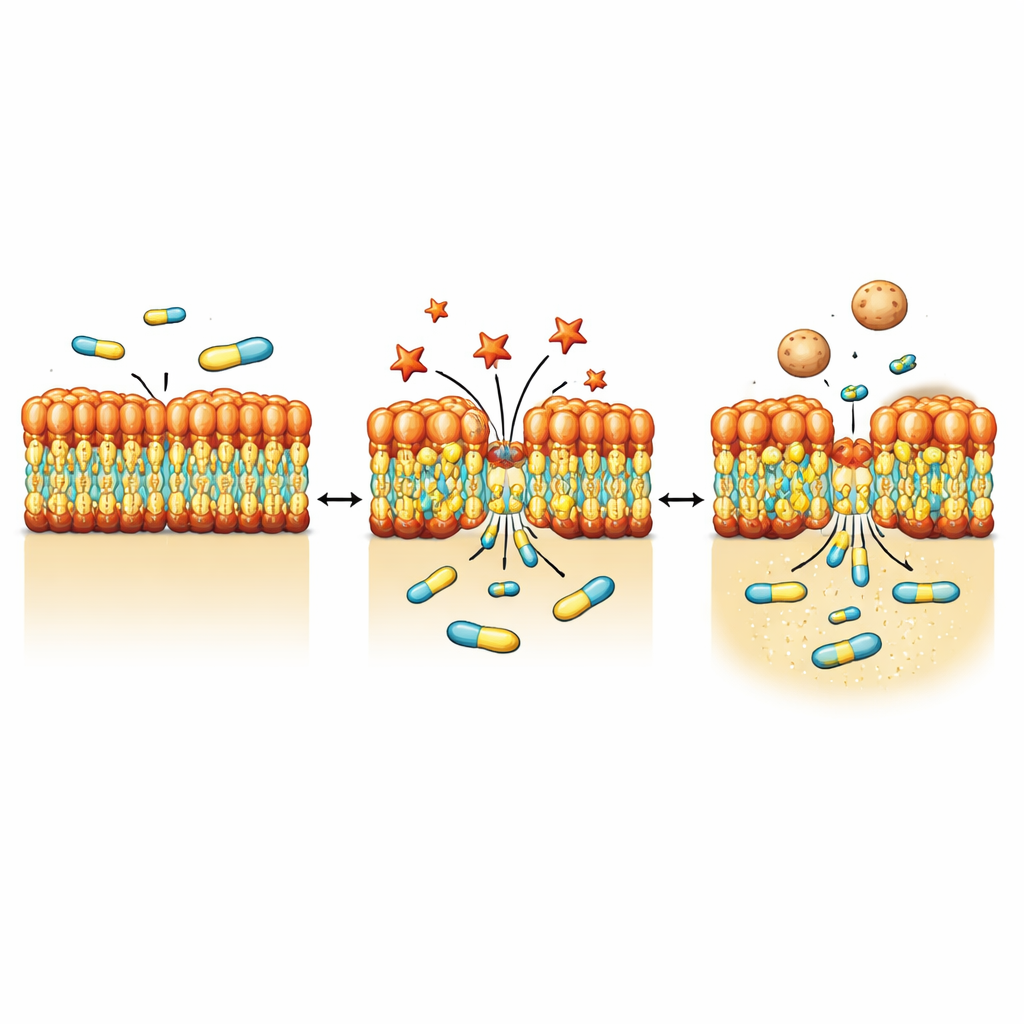
Från petriskålar till levande värdar
Där kraftiga effekter i provrör inte alltid överförs till levande organismer, bedömde forskarna NV716–doxycyklin‑kombinationen i en infektionsmodell med larver av vaxmott Galleria mellonella. Larver som behandlades med kombinationen visade en tendens till bättre överlevnad jämfört med enbart doxycyklin, även om förbättringen inte var statistiskt signifikant under de testade förhållandena. Datorbaserade förutsägelser av läkemedelslika egenskaper antyder att NV716 har drag som överensstämmer med interaktioner med membraner och kan tolereras i djur, men noggranna säkerhets‑ och dosstudier återstår att genomföra. Författarna ser NV716 främst som ett konceptbevis: en molekyl som visar vad som är möjligt när det bakteriella höljet selektivt moduleras snarare än förstörs.
Vad detta betyder för att tackla svåra infektioner
I vardagstermer visar detta arbete att det är möjligt att ”låsa upp” en svårgenomtränglig bakterie som P. aeruginosa utan att slå sönder dörren. NV716 lägger sig i mikrobernas yttre skal och omarrangerar subtilt dess struktur så att vissa antibiotika, framför allt doxycyklin, kan smita in snabbare och i större mängder. Bakterierna svarar genom att skala av extra delar av sitt yttre hölje i form av vesiklar—tecken på stress men inte ett fullständigt sammanbrott. Även om de första djurförsöken är återhållsamma ger studien en kvantitativ ritning för att designa nya hjälpmolekyler och hybrida läkemedel som riktar sig mot det yttre membranet. Sådana strategier kan förlänga livslängden för befintliga antibiotika och ge kliniker nya alternativ mot några av de mest envisa sjukhusinfektionerna.
Citering: Draveny, M., Chauvet, H., De Pauw, A. et al. NV716 acts as an envelope-active adjuvant that enhances antibiotic accumulation in Pseudomonas aeruginosa. npj Antimicrob Resist 4, 29 (2026). https://doi.org/10.1038/s44259-026-00203-w
Nyckelord: antimikrobiell resistens, Pseudomonas aeruginosa, yttre membran, antibiotiskt adjuvans, doxycyklin