Clear Sky Science · tr
Hücre-kültür odacığıyla entegre dinamik optik koherens mikroskopi: Tümör sferoid–ilaç etkileşiminin uzunlamasına ve erken safha değerlendirmesi
Kanser Hücrelerinin Gerçek Zamanlı Tepkisini İzlemek
Kanser ilaçları genellikle bir tümörü ne kadar küçülttüklerine göre değerlendirilir, ancak kitle görünür biçimde boyut değiştirdiğinde değerli saatler ya da günler geçmiş olur. Bu çalışma, ilaç eklendikten hemen sonra bile, küçük 3B meme kanseri hücre kümeleri—tümör sferoidleri—için tedaviye yanıtı izlemenin bir yolunu tanıtıyor. İleri bir ışık tabanlı mikroskopu mini hâle getirilmiş bir hücre-kültür odacığıyla birleştirerek araştırmacılar, boyayıp işaretlemeden ya da örneği yok etmeden bu sferoidlerin derinliklerindeki canlı kanser hücrelerinin davranışlarını takip edebiliyorlar.
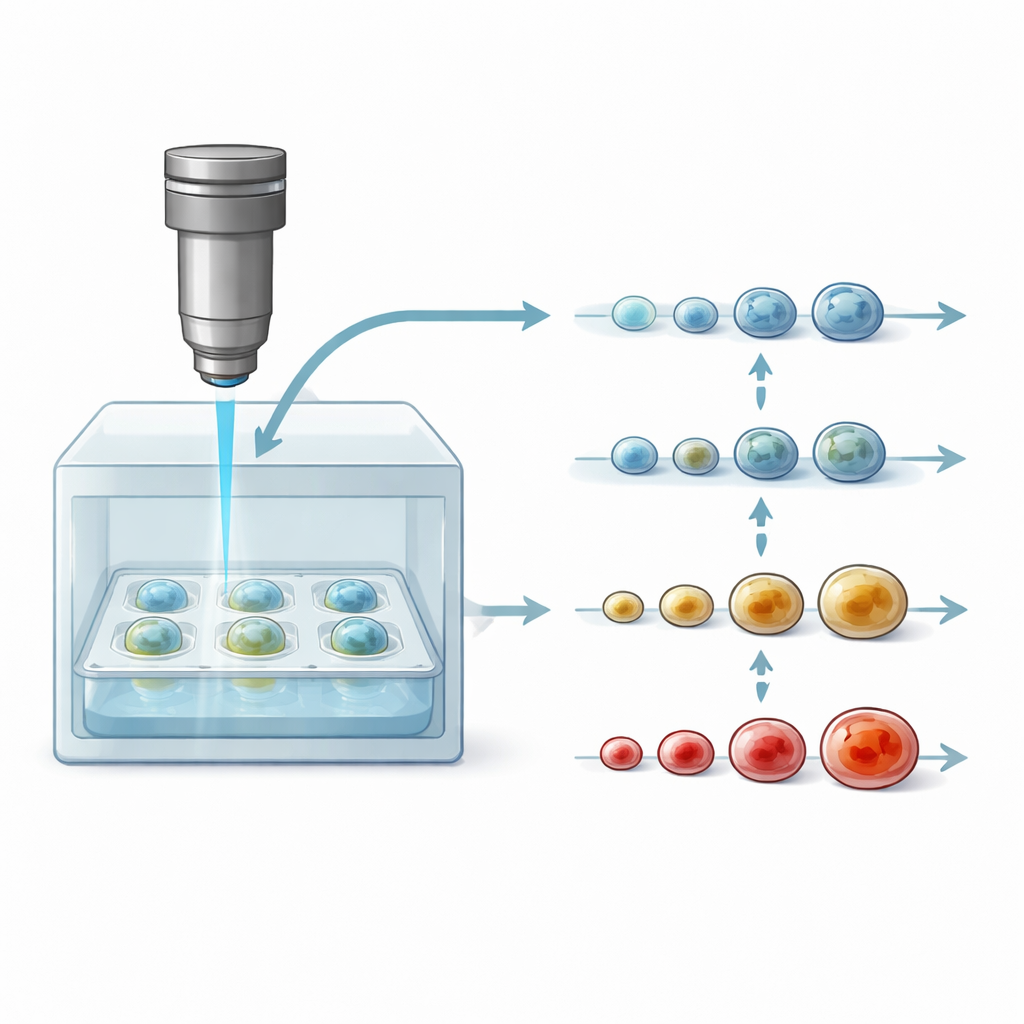
Canlı Kanser Modellerine Yeni Bir Pencere
Araştırmacılar, düz hücre katmanlarından veya bazı hayvan modellerinden daha iyi tümör özelliklerini taklit ettikleri için giderek daha fazla tümör sferoidleri yetiştiriyor. Ancak boyama ve floresan görüntüleme gibi standart inceleme araçları genellikle dokuya dilimleme ya da kimyasal müdahale gerektirir. Bu da her sferoidin yalnızca bir kez test edilebildiği ve zaman içinde ayrıntılı izlemelerin imkansız olduğu anlamına gelir. Göz kliniklerinde kullanılan, invazif olmayan 3B bir görüntüleme yöntemi olan geleneksel optik koherens tomografi (OCT) sferoidlerin içini görebilir, ancak çoğunlukla şekil ve boyutu gösterir. Bu yapısal değişiklikler genellikle geç ortaya çıkar; ilaç hücre sağlığını etkilemeye başladıktan çok sonra görünür hâle gelir.
Hareketi Hayati Bir Belirtiye Çevirmek
Araştırma ekibi OCT’yi, sadece yapıları haritalandırmayan; hücre içindeki küçük hareketlerden kaynaklanan ışık sinyalindeki ince dalgalanmaları ölçen dinamik bir versiyon olan DOCT ile geliştirdi. Sinyalin zaman içindeki değişkenliğini izleyen bir yöntem ile ne kadar hızlı korelasyonunun kaybolduğunu izleyen bir diğer yöntem, birlikte harekete duyarlı bir stetoskop gibi çalışır. Hücreler sağlıklı ve aktif olduğunda iç bileşenleri hareket eder ve yeniden düzenlenir, bu da canlı bir DOCT sinyali yaratır. Hücreler yavaşladığında, strese girdiğinde veya öldüğünde bu iç hareketlilik azalır. Her sferoidin içindeki “yüksek-dinamik” ve “düşük-dinamik” bölgeleri nicelleştirerek sistem, 3B’de canlı ve yaşamsız hücrelerin nerede olduğunu ve bu desenlerin nasıl evrildiğini tahmin eder.
İzlerken Hücreleri Rahatta Tutmak
Aynı sferoidin günler boyunca izlenebilmesi için araştırmacılar DOCT mikroskobunu 37°C ve kontrollü karbondioksit gibi vücut benzeri koşulları koruyan kompakt bir yetiştirme odacığıyla entegre ettiler. Çok sayıda sferoidin bulunduğu standart 96 kuyucuklu plaka görüntüleme kafasının altında yer alır ve kontaminasyonu önlemek için bir kapakla korunur. Işın ince cam katmanlardan geçerek örneğe ulaşır ve tarama, dokudaki her noktanın yalnızca kısa süreliğine ışınlanacak kadar hızlı ve naziktir. Bu düzenek iki tarz deney yapılmasına olanak verdi: biri onlarca sferoidin farklı dozlarda üç yaygın meme kanseri ilacıyla muamele edilip yaklaşık dört gün boyunca her dört saatte bir görüntülendiği; diğeri ise tek tek sferoidlerin aynı süre boyunca otomatik olarak her 30 dakikada bir takip edildiği deneyler.
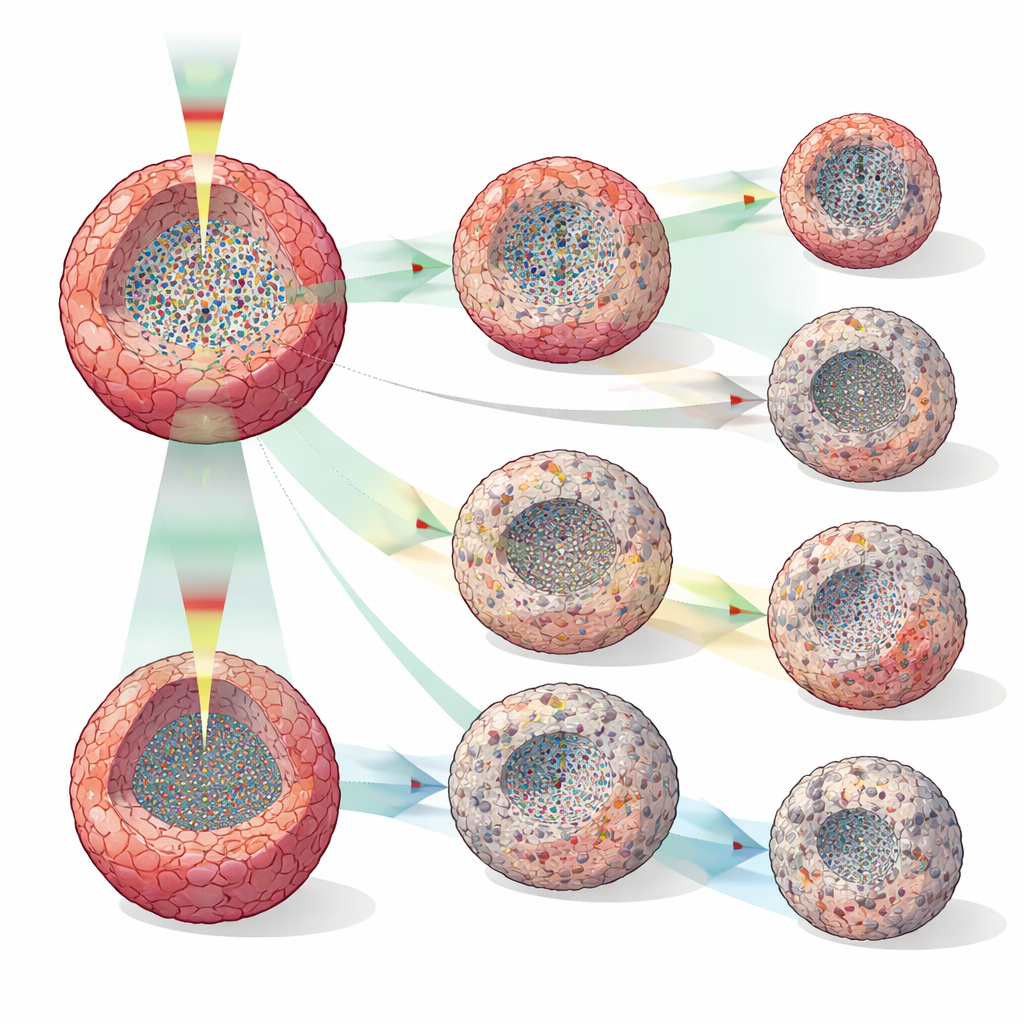
Boyut Değişikliğinden Çok Önce İlaç Etkilerini Görmek
Grup, insan meme kanseri sferoidlerini (MCF-7) çeşitli konsantrasyonlarda doksorubisin, tamoksifen veya paklitaksel ile tedavi etti ve DOCT okumalarını basit hacim ölçümleriyle karşılaştırdı. Sferoid boyutu birçok saat boyunca dozlar arasında sıklıkla benzer görünürken, DOCT metrikleri çok daha erken ayrıştı—bazen tedaviden sadece iki saat sonra ve tutarlı şekilde 12 saat içinde. Farklı ilaçlar farklı iç desenler üretti: yüksek doz doksorubisin sferoidlerin büzüşmesine ve hücre ölümüyle ilişkilendirilebilecek merkezî düşük aktivite zonlarına yol açtı; tamoksifen ağırlıklı olarak büyümeyi yavaşlattı, bazen çevrede büyüme durması veya periferik apoptosu yansıtabilecek sessiz bir dış kabuk oluşturdu; paklitaksel ise hücre bölünmesi ve hücre içi taşımanın bilinen bozulmasına uygun yayılmış düşük-aktivite yamaları üretti. 30 dakikalık yüksek-zaman çözünürlüklü çalışmalarda, sessiz çekirdeklerin kaybolup tekrar ortaya çıktığı veya düşük-aktivite katmanlarının oluştuğu geçiş noktaları ortaya çıktı; bu tür değişiklikler seyrek ve yıkıcı testlerde görünmez olurdu.
Geleceğin Kanser İlaç Testleri İçin Anlamı
Bir uzman olmayan için ana mesaj şu: entegre DOCT–odacık sistemi, tümöre benzer hücre kümelerinin ilaçlara içeriden dışarıya nasıl tepki verdiğini, büyüme veya küçülme belirginleşmeden saatler önce “dinleyebiliyor”. Bir tedavinin işe yarayıp yaramadığını görmek için günler beklemek yerine, araştırmacılar boya eklemeden veya örnekleri yok etmeden hücre aktivitesindeki erken, doza bağımlı değişiklikleri tespit edebilir. Bu, ilaçları karşılaştırmayı, dozları ayarlamayı ve bazı tümörlerin neden tedaviye dirençli olduğunu çalışmayı kolaylaştırır. Henüz laboratuvar aracı olmasına karşın, bu yaklaşım daha hızlı, daha açıklayıcı preklinik ilaç test platformlarına işaret ediyor; nihayetinde umut vadeden kanser tedavilerini daha verimli belirlemeye ve hayvan deneylerine daha az bağımlı olmaya yardımcı olabilir.
Atıf: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
Anahtar kelimeler: dinamik optik koherens tomografi, tümör sferoidleri, kanser ilaç yanıtı, etiketsiz görüntüleme, uzunlamasına hücre kültürü