Clear Sky Science · ja
細胞培養チャンバーを統合した動的光干渉顕微鏡による腫瘍スフェロイドと薬剤の相互作用の長期・早期評価
がん細胞の反応をリアルタイムで観察する
がん薬剤は通常、腫瘍がどれだけ縮小するかで評価されますが、目に見えるサイズ変化が現れる頃には貴重な時間が何時間もまたは数日も経ってしまいます。本研究は、薬剤を添加して間もなく、乳がん細胞の小さな3次元クラスター(腫瘍スフェロイド)が治療にどう反応するかを観察する手法を示します。高度な光学顕微鏡と小型の細胞培養チャンバーを組み合わせることで、染色や標識を用いず、試料を破壊することなく、スフェロイド内部にいる生きたがん細胞の挙動を深部まで追跡できます。
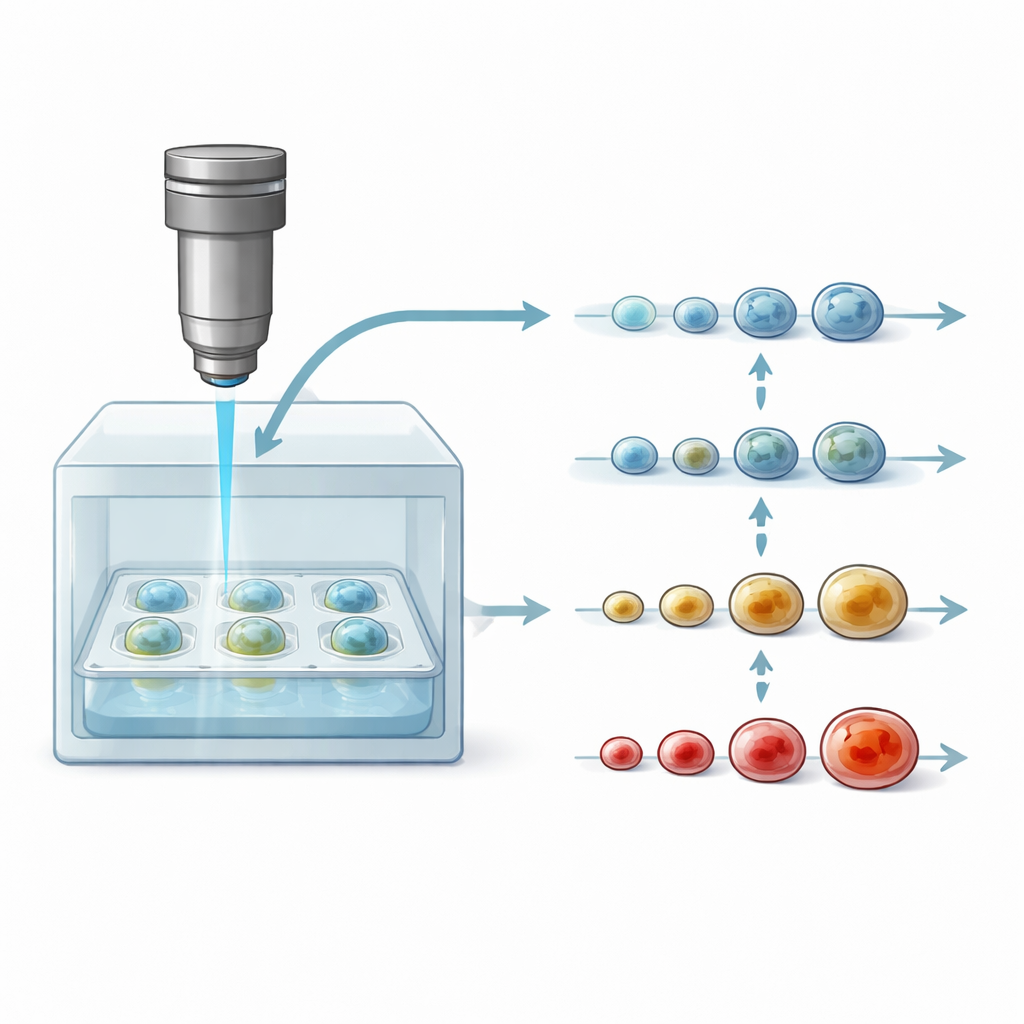
生きたがんモデルへの新たな窓
研究者は平板状の培養や一部の動物モデルよりも実際の腫瘍の特徴をよく模倣するため、スフェロイドを育てることが増えています。しかし、染色や蛍光イメージングといった標準的な検査法は、しばしば組織の切片化や化学的な処理を必要とします。つまり各スフェロイドは一度しか評価できず、時間を通した細かな追跡は不可能になります。従来の光コヒーレンス断層撮影(OCT)は非侵襲で3Dイメージングが可能でスフェロイド内部を可視化できますが、主に形状や大きさを示すにとどまります。これらの構造変化は通常、薬剤が細胞機能に影響を与え始めてからかなり後に現れます。
動きをバイタルサインに変える
研究チームはOCTを基に、動的光コヒーレンス断層撮影(DOCT)という手法を用いました。DOCTは構造を写すだけでなく、細胞内部でのごく小さな運動によって生じる光信号の微細なゆらぎを測定します。時間的に信号がどれだけ変動するかを追跡する方法と、信号の相関がどれほど速く失われるかを追う方法の2つの解析が組み合わされ、動きに敏感な聴診器のように機能します。細胞が健康で活性的なときは、内部構造が動き回りDOCT信号は活発になります。細胞が減速し、ストレスを受けたり死んだりすると、その内部のざわめきは減衰します。“高ダイナミクス”領域と“低ダイナミクス”領域を定量化することで、スフェロイド内部の生存細胞と非生存細胞の配置を3Dで推定し、それらのパターンが時間とともにどう変化するかを示せます。
観察中も細胞を快適に保つ
同じスフェロイドを数日間追跡するため、研究者らはDOCT顕微鏡を37°Cと制御された二酸化炭素濃度で体内に近い状態を維持するコンパクトな培養チャンバーと統合しました。多数のスフェロイドを収めた標準的な96ウェルプレートが撮像ヘッドの下に置かれ、コンタミネーションを避けるために蓋で保護されています。光ビームは薄いガラス層を透過して試料に到達し、走査は迅速かつ穏やかで、組織の各ポイントへの露光は短時間に抑えられます。このセットアップにより2種類の実験が可能になりました。1つは複数のスフェロイドを異なる用量の3種類の乳がん薬で処理し、約4日間にわたって約4時間ごとに撮像する方法。もう1つは個々のスフェロイドを同期間で30分ごとに自動的に追跡する方法です。
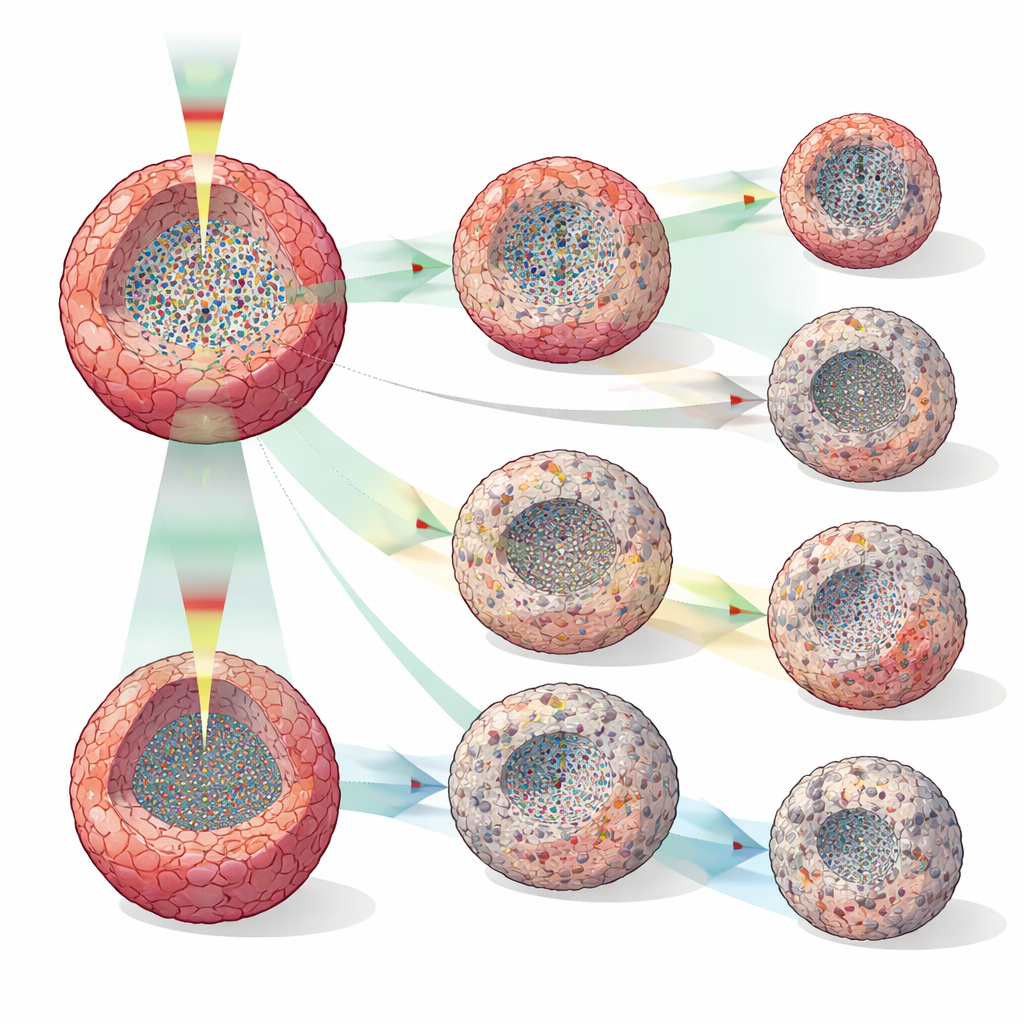
サイズ変化よりずっと早く薬剤効果を検出する
研究グループはヒト乳がんスフェロイド(MCF-7)をドキソルビシン、タモキシフェン、パクリタキセルの複数濃度で処理し、DOCTの指標と単純な体積測定を比較しました。スフェロイドのサイズは多くの場合、投与後何時間も類似して見えましたが、DOCTの指標ははるかに早く分岐しました—場合によっては投与後わずか2時間で、遅くとも12時間で一貫して差が現れました。薬剤ごとに内部パターンは異なりました:高用量のドキソルビシンはスフェロイドの縮小と中心部の活動低下領域をもたらし、細胞死を示唆しました。タモキシフェンは主に増殖を遅らせ、周辺で増殖停止やアポトーシスに相当する静かな外側層を形成することがありました。パクリタキセルは分裂や細胞内輸送の撹乱と一致する点在する低活動パッチを生じました。30分間隔の高時間分解能測定では、静かなコアが消失して再出現する瞬間や低活動層が形成される移行点など、破壊的で間隔の広い検査では見逃されるであろう変化が明らかになりました。
今後のがん薬試験にとっての意義
専門外の読者にとっての主なメッセージは、この統合されたDOCT–チャンバーシステムが腫瘍様クラスターの内側から外側へと薬剤に対する反応を「聴く」ことができ、成長や縮小が目に見えるようになる何時間も前に検出できるという点です。治療が効くかどうかを数日待つ代わりに、染色や試料破壊を行わずに用量依存的な早期の細胞活動変化を検出できます。これにより薬剤の比較、用量の調整、特定の腫瘍が治療に耐性を示す理由の研究が容易になります。現時点では研究室向けのツールですが、このアプローチはより迅速で情報量の多い前臨床薬剤評価プラットフォームの道を開き、有望な治療候補の効率的な同定や動物実験への依存の低減につながる可能性があります。
引用: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
キーワード: 動的光コヒーレンス断層撮影, 腫瘍スフェロイド, がん薬剤反応, 無標識イメージング, 長期細胞培養