Clear Sky Science · nl
Dynamische optische coherentie-microscoop geïntegreerd met celkweekkamer maakt longitudinale en vroegtijdige beoordeling van tumor-sferoïde–medicijninteractie mogelijk
Het in realtime volgen van de reactie van kankercellen
Kankergeneesmiddelen worden meestal beoordeeld op hoeveel ze een tumor doen krimpen, maar tegen de tijd dat een massa zichtbaar van omvang verandert, zijn er kostbare uren of dagen verstreken. Deze studie introduceert een manier om kleine driedimensionale clusters van borstkankercellen — zogeheten tumor-sferoïden — vrijwel meteen te volgen nadat een middel is toegevoegd. Door een geavanceerde lichtmicroscoop te combineren met een miniatuur celkweekkamer volgen de onderzoekers het gedrag van levende kankercellen diep binnenin deze sferoïden zonder kleurstoffen, labels of het vernietigen van het monster.
Een nieuw venster op levende kankermodellen
Onderzoekers kweken steeds vaker tumor-sferoïden omdat ze veel eigenschappen van echte tumoren beter nabootsen dan platte cellagen of sommige diermodellen. Standaardinstrumenten om ze te onderzoeken, zoals kleuring en fluorescentiebeeldvorming, vereisen vaak het in plakjes snijden of chemisch veranderen van het weefsel. Dat betekent dat elk sferoïde meestal maar éénmaal getest kan worden en dat gedetailleerde tijdsgebonden opvolging onmogelijk is. Traditionele optische coherentiëtomografie (OCT) — een niet-invasieve, driedimensionale beeldvormingstechniek die in oogklinieken wordt gebruikt — kan in sferoïden kijken, maar toont vooral vorm en grootte. Die structurele veranderingen treden meestal laat op, lang nadat een middel al invloed op de celgezondheid heeft gekregen.
Beweging omzetten in een vitale indicator
Het team bouwde voort op OCT door een dynamische variant te gebruiken, DOCT genoemd, die niet alleen structuren afbeeldt maar ook subtiele fluctuaties in het lichtsignaal meet veroorzaakt door kleine bewegingen binnenin cellen. Twee analysemethoden — één die bijhoudt hoeveel het signaal over de tijd varieert en een andere die volgt hoe snel het decoheret — werken samen als een bewegingsgevoelige stethoscoop. Wanneer cellen gezond en actief zijn, bewegen en herschikken hun interne componenten zich, wat een levendig DOCT-signaal oplevert. Wanneer cellen vertraagd raken, gestrest zijn of afsterven, neemt dat interne rumoer af. Door “hoog-dynamische” en “laag-dynamische” regio’s binnen elk sferoïde te kwantificeren, schat het systeem in waar levensvatbare en niet-levende cellen zich in 3D bevinden en hoe die patronen zich ontwikkelen.
Cellen comfortabel houden terwijl we kijken
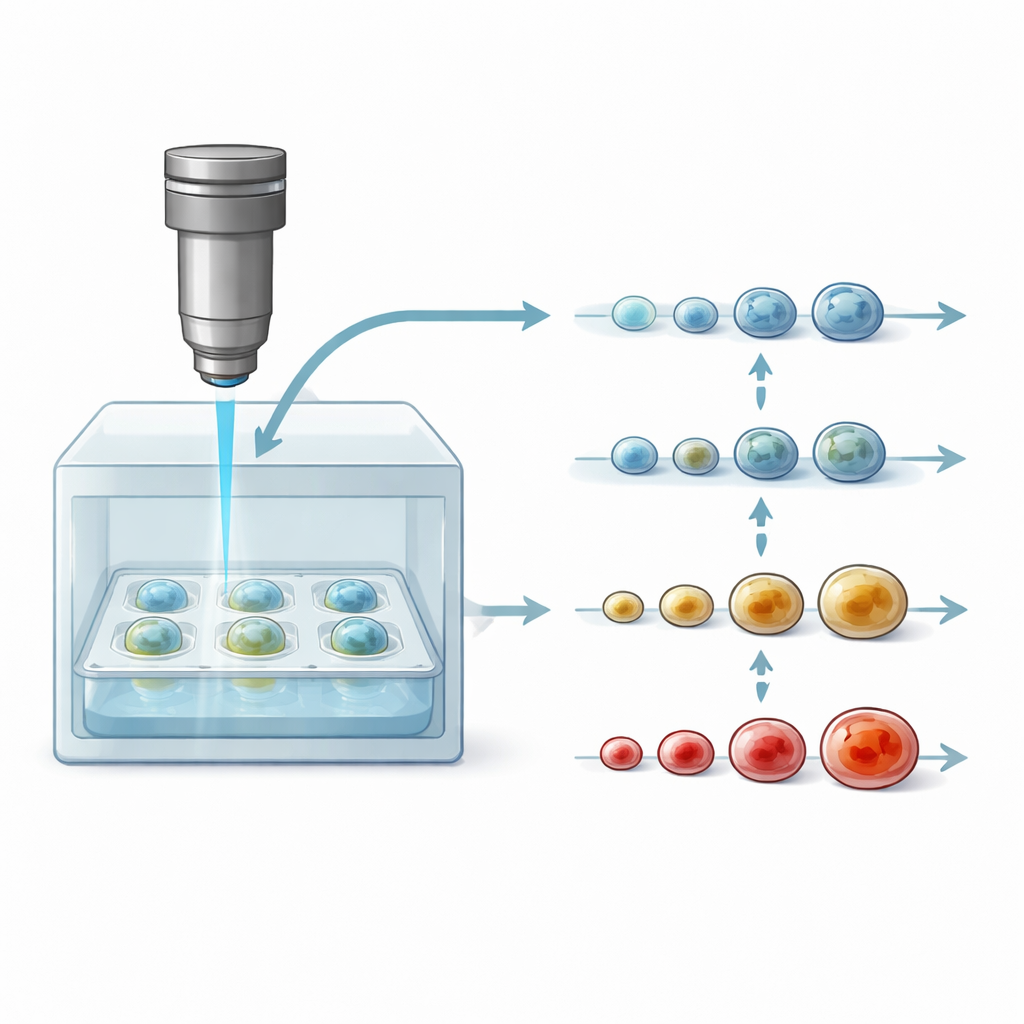
Om hetzelfde sferoïde dagenlang te volgen, integreerden de onderzoekers hun DOCT-microscoop met een compacte kweekkamer die lichaamsachtige omstandigheden handhaaft: 37 °C en gecontroleerde kooldioxide. Een standaard 96-wells plaat met veel sferoïden bevindt zich onder de beeldkop, beschermd door een deksel om verontreiniging te voorkomen. De lichtbundel gaat door dunne glaslagen om het monster te bereiken, en het scannen is snel en voorzichtig genoeg dat elk punt in het weefsel slechts kort wordt belicht. Deze opstelling maakte twee soorten experimenten mogelijk: één waarbij tientallen sferoïden, behandeld met verschillende doseringen van drie veelgebruikte borstkankergeneesmiddelen, om de vier uur gedurende ongeveer vier dagen werden afgebeeld, en een andere waarbij individuele sferoïden automatisch elke 30 minuten over dezelfde periode werden gevolgd.
Medicijneffecten zien lang voordat grootte verandert
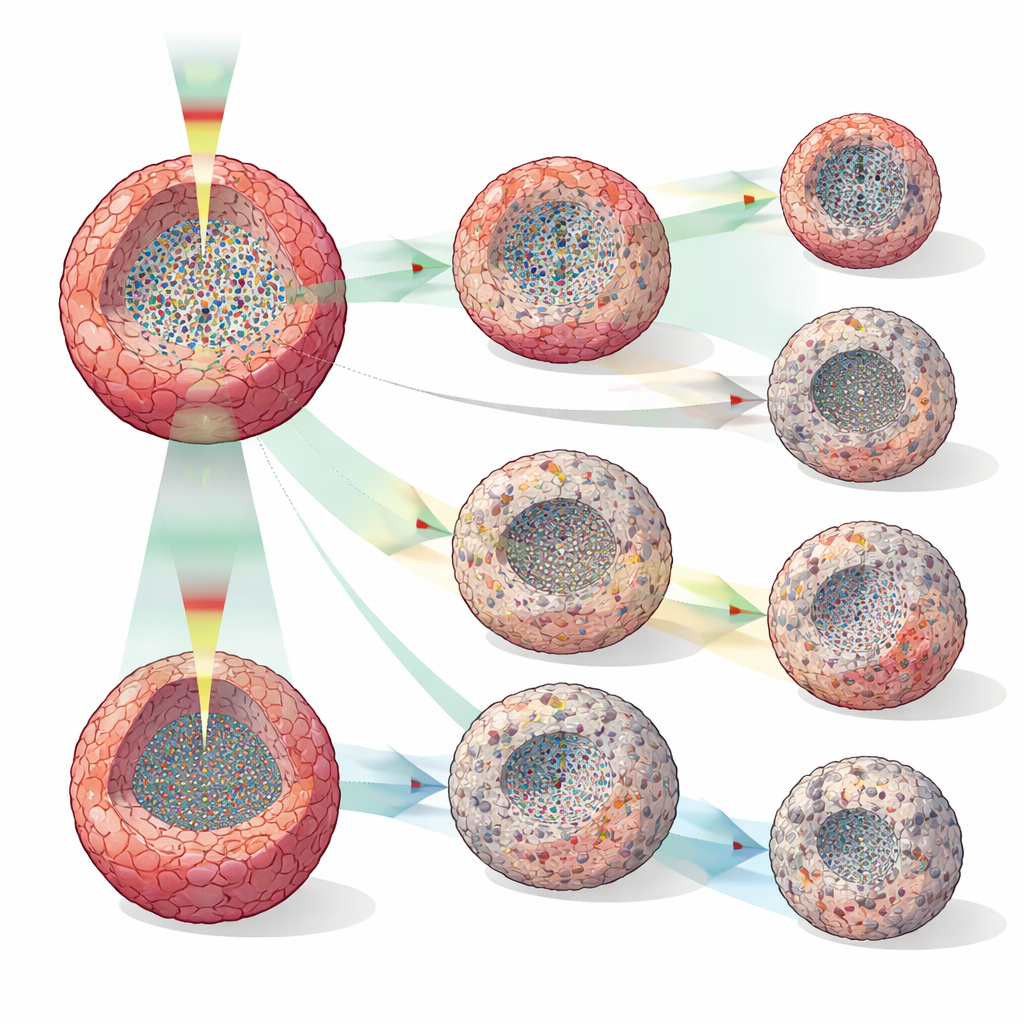
De groep behandelde humane borstkanker-sferoïden (MCF-7) met doxorubicine, tamoxifen of paclitaxel in verschillende concentraties en vergeleek DOCT-uitkomsten met eenvoudige volumemetingen. Terwijl de sferoïde-grootte vaak urenlang vergelijkbaar leek over verschillende doses, weekten de DOCT-metrieken veel eerder af — soms al twee uur na behandeling en consequent binnen 12 uur. Verschillende middelen produceerden onderscheidende interne patronen: hoge doses doxorubicine leidden tot krimpende sferoïden en centrale zones met verminderde activiteit die op celdood wijzen; tamoxifen vertraagde voornamelijk de groei en vormde soms een rustige buitenlaag die mogelijk wijst op groeistilstand of apoptose aan de periferie; en paclitaxel veroorzaakte verspreide laag-activiteitsvlekken, consistent met de bekende verstoring van celdeling en intracellulair transport. Experimenten met hoge temporele resolutie om de 30 minuten toonden overgangspunten — wanneer stille kernen verdwenen en vervolgens herleefden, of wanneer laag-activiteitslagen gevormd werden — die onzichtbaar zouden blijven in sparsere, destructieve testen.
Wat dit betekent voor toekomstig kankermedicijntesten
Voor niet-specialisten is de kernboodschap dat dit geïntegreerde DOCT–kweekkamer-systeem als het ware kan "luisteren" naar hoe tumorgelijke celclusters van binnenuit reageren op medicijnen, uren voordat ze merkbaar groeien of krimpen. In plaats van dagen te wachten om te zien of een behandeling werkt, kunnen onderzoekers vroege, dosisafhankelijke veranderingen in celactiviteit detecteren zonder kleurstoffen toe te voegen of monsters op te offeren. Dat maakt het eenvoudiger om middelen te vergelijken, doses bij te stellen en te bestuderen waarom bepaalde tumoren therapieresistent zijn. Hoewel het nog een laboratoriuminstrument is, wijst deze benadering op snellere, informatieverere preklinische testplatforms voor geneesmiddelen die uiteindelijk kunnen helpen veelbelovende kankerbehandelingen efficiënter te identificeren en het gebruik van dierproeven te verminderen.
Bronvermelding: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
Trefwoorden: dynamische optische coherentiëtomografie, tumor-sferoïden, kankermedicijnrespons, labelvrije beeldvorming, longitudinale celkweek