Clear Sky Science · pl
Dynamiczny mikroskop koherencji optycznej zintegrowany z komorą hodowli komórek umożliwiający długofalową i wczesną ocenę interakcji sferoidów nowotworowych z lekiem
Obserwowanie reakcji komórek nowotworowych w czasie rzeczywistym
Leki przeciwnowotworowe zwykle ocenia się po tym, o ile zmniejszają guz, lecz w momencie, gdy masa zmienia rozmiar w sposób widoczny, upłynęły już cenne godziny lub dni. W tym badaniu przedstawiono sposób obserwacji małych, trójwymiarowych skupisk komórek piersi — zwanych sferoidami nowotworowymi — reagujących na leczenie niemal natychmiast po dodaniu leku. Łącząc zaawansowany mikroskop oparty na świetle z miniaturową komorą do hodowli komórek, badacze śledzą zachowanie żywych komórek głęboko wewnątrz tych sferoidów bez użycia barwników, znaczników czy niszczenia próbki.
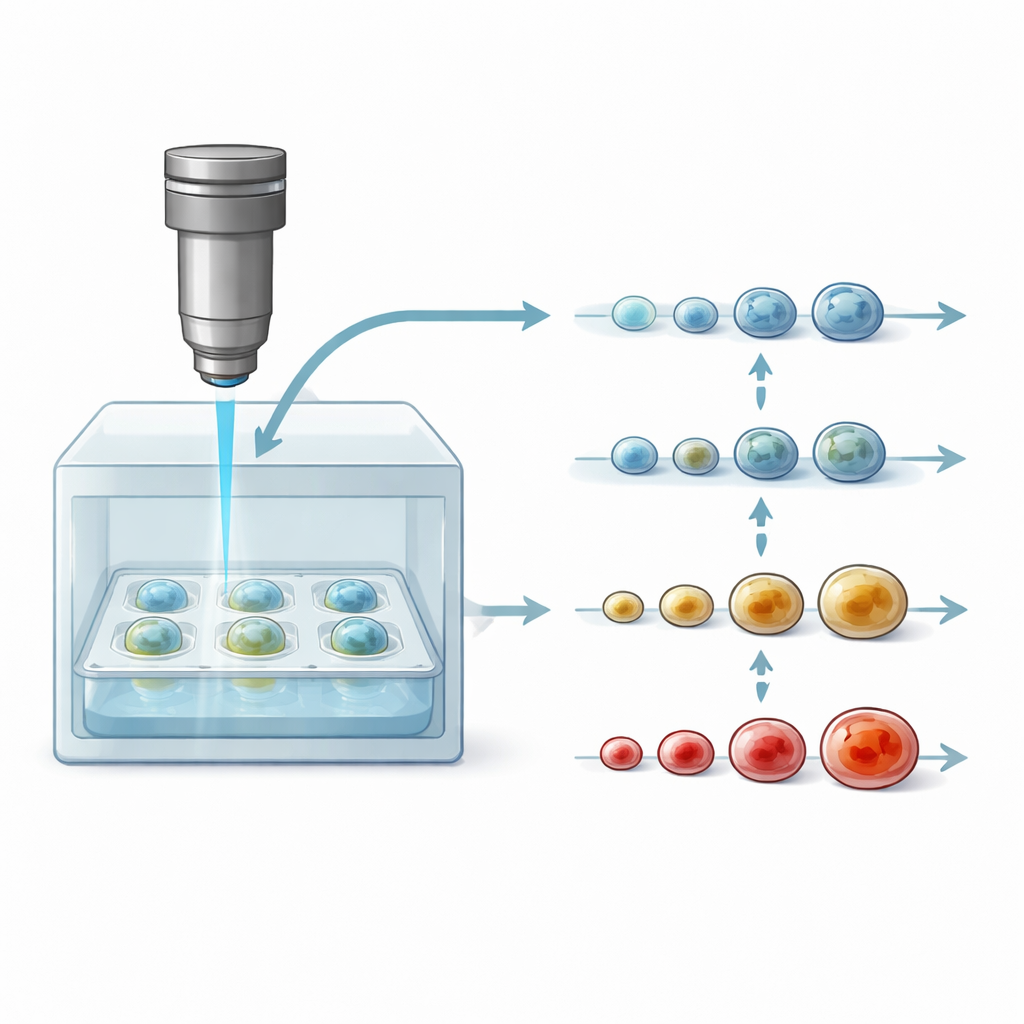
Nowe spojrzenie na żywe modele nowotworowe
Badacze coraz częściej hodują sferoidy nowotworowe, ponieważ odtwarzają one wiele cech prawdziwych guzów lepiej niż płaskie monowarstwy czy niektóre modele zwierzęce. Jednak standardowe narzędzia do ich badania, takie jak barwienie czy obrazowanie fluorescencyjne, często wymagają krojenia lub chemicznej modyfikacji tkanki. Oznacza to, że każdy sferoid można przebadać tylko raz, a śledzenie subtelnych zmian w czasie jest niemożliwe. Tradycyjna optyczna tomografia koherencyjna (OCT) — nieinwazyjna, trójwymiarowa metoda obrazowania stosowana w klinikach okulistycznych — potrafi zajrzeć do wnętrza sferoidów, ale pokazuje głównie kształt i rozmiar. Te strukturalne zmiany pojawiają się zwykle późno, długo po tym, jak lek zaczął wpływać na stan komórek.
Przekształcanie ruchu w oznakę żywotności
Zespół rozwinął OCT, stosując jego dynamiczną wersję zwaną DOCT, która nie tylko mapuje struktury, lecz mierzy subtelne fluktuacje sygnału świetlnego spowodowane drobnymi ruchami wewnątrz komórek. Dwie metody analizy — jedna śledząca, jak bardzo sygnał zmienia się w czasie, a druga mierząca, jak szybko traci korelację — działają razem jak czuły stetoskop na ruch wewnętrzny. Gdy komórki są zdrowe i aktywne, ich wewnętrzne składniki poruszają się i przearanżowują, generując żywy sygnał DOCT. Gdy komórki zwalniają, są zestresowane lub umierają, to wewnętrzne zamieszanie maleje. Poprzez ilościowe określanie obszarów o „wysokiej dynamice” i „niskiej dynamice” wewnątrz każdego sferoidu, system szacuje, gdzie w 3D znajdują się żywe, a gdzie niezdolne do życia komórki, i jak te wzory się zmieniają.
Utrzymanie komfortu komórek podczas obserwacji
Aby obserwować ten sam sferoid przez kilka dni, badacze zintegrowali mikroskop DOCT z kompaktową komorą hodowlaną, która utrzymuje warunki zbliżone do ciała: 37°C i kontrolowane stężenie dwutlenku węgla. Standardowa płytka 96-dołkowa z wieloma sferoidami znajduje się pod głowicą obrazującą, chroniona pokrywą przed zanieczyszczeniem. Wiązka światła przechodzi przez cienkie warstwy szkła, by dotrzeć do próbki, a skanowanie jest na tyle szybkie i łagodne, że każdy punkt tkanki jest tylko krótko naświetlany. Układ ten umożliwił dwa rodzaje eksperymentów: jeden, w którym dziesiątki sferoidów traktowanych różnymi dawkami trzech powszechnych leków przeciwko rakowi piersi obrazowano co cztery godziny przez około cztery dni, oraz drugi, w którym pojedyncze sferoidy śledzono automatycznie co 30 minut przez ten sam okres.
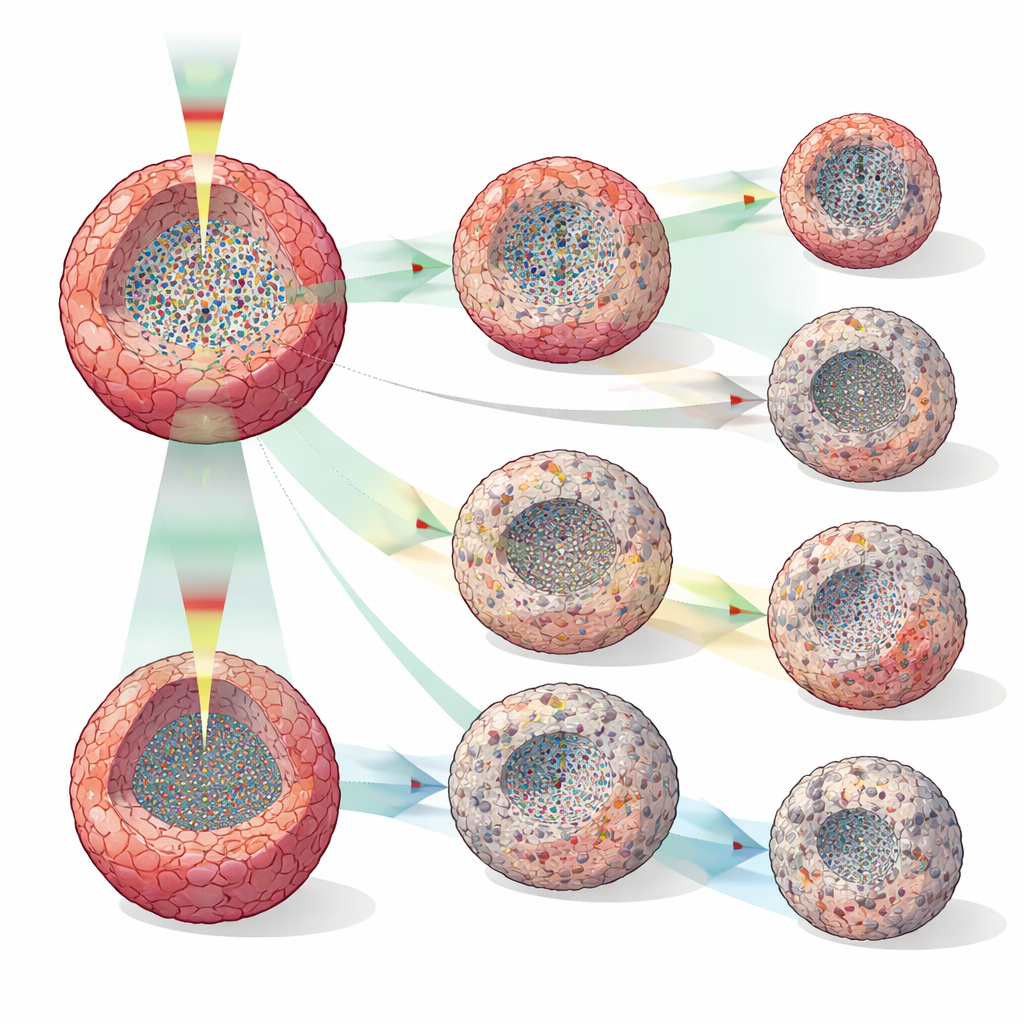
Widzenie efektów leku na długo przed zmianą rozmiaru
Zespół leczył ludzkie sferoidy raka piersi (MCF-7) doxorubicyną, tamoksyfenem lub paklitakselem w kilku stężeniach i porównywał odczyty DOCT z prostymi pomiarami objętości. Podczas gdy rozmiar sferoidu często wyglądał podobnie przy różnych dawkach przez wiele godzin, metryki DOCT rozchodziły się znacznie wcześniej — czasami już po dwóch godzinach od podania leku, a konsekwentnie po 12 godzinach. Różne leki wywoływały odmienne wewnętrzne wzory: wysokie dawki doxorubicyny prowadziły do kurczących się sferoidów i centralnych stref o zmniejszonej aktywności sugerujących śmierć komórek; tamoksyfen głównie spowalniał wzrost, czasem tworząc cichą zewnętrzną warstwę, co może odzwierciedlać zahamowanie wzrostu lub apoptozę na obwodzie; a paklitaksel powodował rozrzucone obszary niskiej aktywności, zgodne z jego znanym zaburzeniem podziału komórek i transportu wewnątrzkomórkowego. Pomiary o wysokiej rozdzielczości czasowej co 30 minut ujawniły punkty przejścia — kiedy ciche jądra znikały i potem znów się pojawiały, lub kiedy tworzyły się warstwy o niskiej aktywności — które pozostałyby niewidoczne w rzadkich, destrukcyjnych testach.
Co to oznacza dla przyszłych testów leków przeciwnowotworowych
Dla osoby niezwiązanej ze specjalistyczną dziedziną kluczowe przesłanie jest takie, że zintegrowany system DOCT–komora potrafi „nasłuchiwać”, jak skupiska komórek przypominające guzy reagują na leki od wewnątrz, wiele godzin przed tym, gdy zauważalnie rosną lub kurczą się. Zamiast czekać dni, by stwierdzić skuteczność terapii, badacze mogą wykrywać wczesne, zależne od dawki zmiany aktywności komórek bez dodawania barwników czy poświęcania próbek. Ułatwia to porównywanie leków, dostrajanie dawek i badanie, dlaczego niektóre guzy są oporne na terapię. Choć obecnie jest to narzędzie laboratoryjne, podejście to wskazuje drogę ku szybszym, bardziej informatywnym platformom przedklinicznym testowania leków, które ostatecznie mogą pomóc szybciej identyfikować obiecujące terapie przeciwnowotworowe i zmniejszać zależność od eksperymentów na zwierzętach.
Cytowanie: Abd El-Sadek, I., Morishita, R., Guo, Y. et al. Dynamic optical coherence microscope integrated with cell-cultivation chamber enabled longitudinal and early-stage assessment of tumor spheroid-drug interaction. Sci Rep 16, 14254 (2026). https://doi.org/10.1038/s41598-026-44296-9
Słowa kluczowe: dynamiczna optyczna tomografia koherencyjna, sferoidy nowotworowe, reakcja nowotworu na leki, obrazowanie bez znaczników, dlugofalowa hodowla komórek